Clear Sky Science · nl
Mutaties in KIF11 die verstandelijke beperkingen veroorzaken, verstoren microtubulusdynamiek en dendritische vertakking
Hoe piepkleine cellulaire motoren denken vormgeven
Onze hersenen berusten op miljarden zenuwcellen die met grote precisie met elkaar moeten verbinden. Deze studie onderzoekt hoe één moleculaire motor, KIF11 genoemd, helpt bij het vormen van de vertakkende “boom” van uitlopers van zenuwcellen die signalen ontvangen, en hoe ziekt veroorzakende veranderingen in deze motor kunnen leiden tot verstandelijke beperkingen. Door levende neuronen onder de microscoop te volgen en KIF11’s mechaniek in reageerbuizen en in muizen te onderzoeken, laten de auteurs zien hoe dit eiwit het interne steigerwerk van neuronen verfijnt en daarmee hun vermogen om te communiceren beïnvloedt.
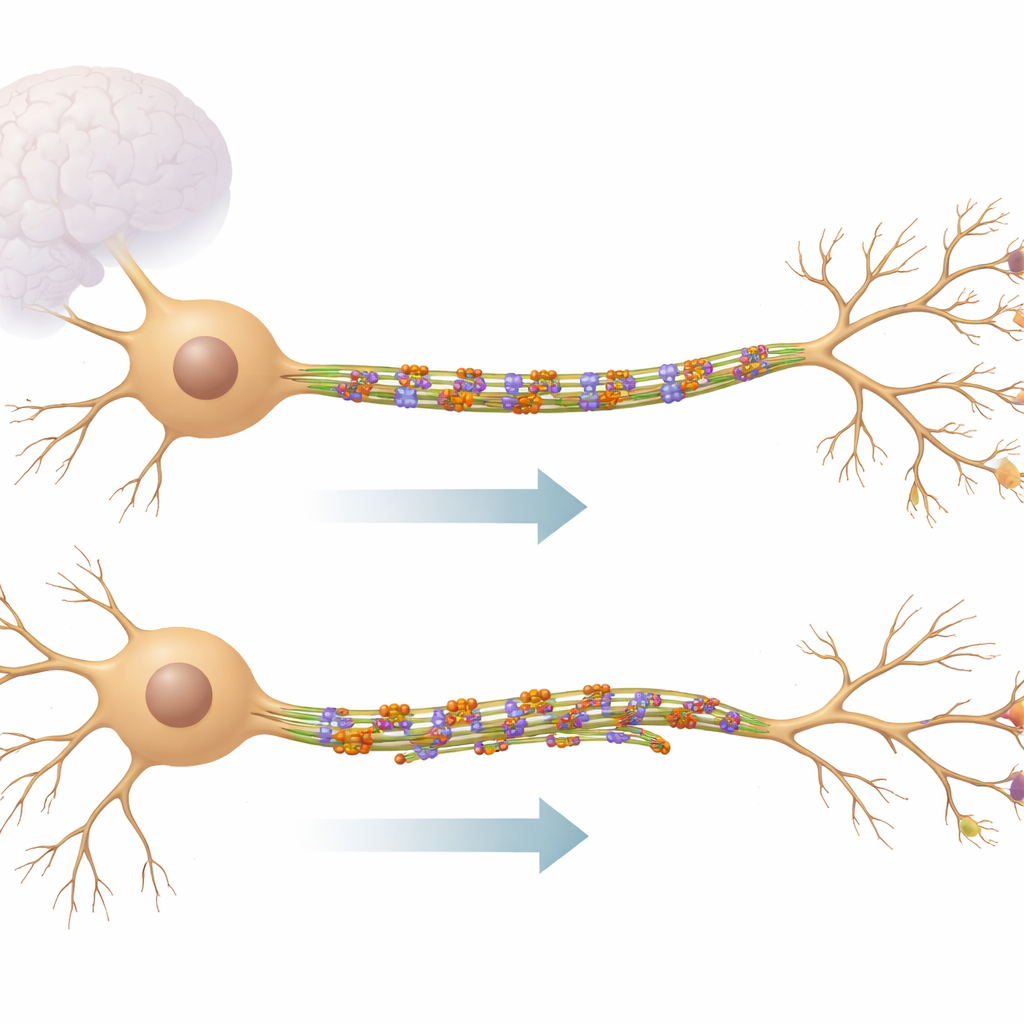
Het binnenste spoorwegsysteem van de neuron
Neuronen zenden informatie uit en ontvangen die via lange, kabelachtige uitlopers. In deze kabels lopen microtubuli, stijve eiwitstaven die fungeren als spoorrails voor het verplaatsen van materiaal en bijdragen aan de vorm van de cel. In de hoofdinkomstenvertakkingen, dendrieten genaamd, lopen microtubuli in beide richtingen en vormen zo een gemengd, dynamisch netwerk. KIF11 behoort tot een familie van kleine motoren die meestal actief zijn tijdens celdeling, maar dit werk toont aan dat het ook actief blijft in volledig ontwikkelde hersencellen. In plaats van vracht te vervoeren, verbindt KIF11 aangrenzende microtubuli met elkaar en werkt het meer als een rem en stabilisator dan als een transportwagen.
Groeibalans bewaren
Met behulp van live‑imaging van muizen‑hippocampusneuronen verlaagden de onderzoekers KIF11‑niveaus of blokkeerden ze de activiteit met geneesmiddelen en volgden ze de tips van groeiende microtubuli. Ze vonden dat wanneer KIF11 werd geremd, een specifieke klasse microtubuli — degene met hun “min‑uiteinde” naar buiten gericht — actiever werd, vooral in secundaire en tertiaire dendritische takken. Dit bevorderde het verschijnen en de groei van deze sporen en stimuleerde de vorming van nieuwe vertakkingen, waardoor de dendritische boom uitgebreider werd. Omgekeerd, wanneer KIF11 werd overgeproduceerd, vertraagde de microtubulusdynamiek, werden dendrieten minder complex en raakten de interne sporen soms gedraaid en gelusterd, wat suggereert dat overmatige kracht van KIF11 het steigerwerk kan buigen en belasten.
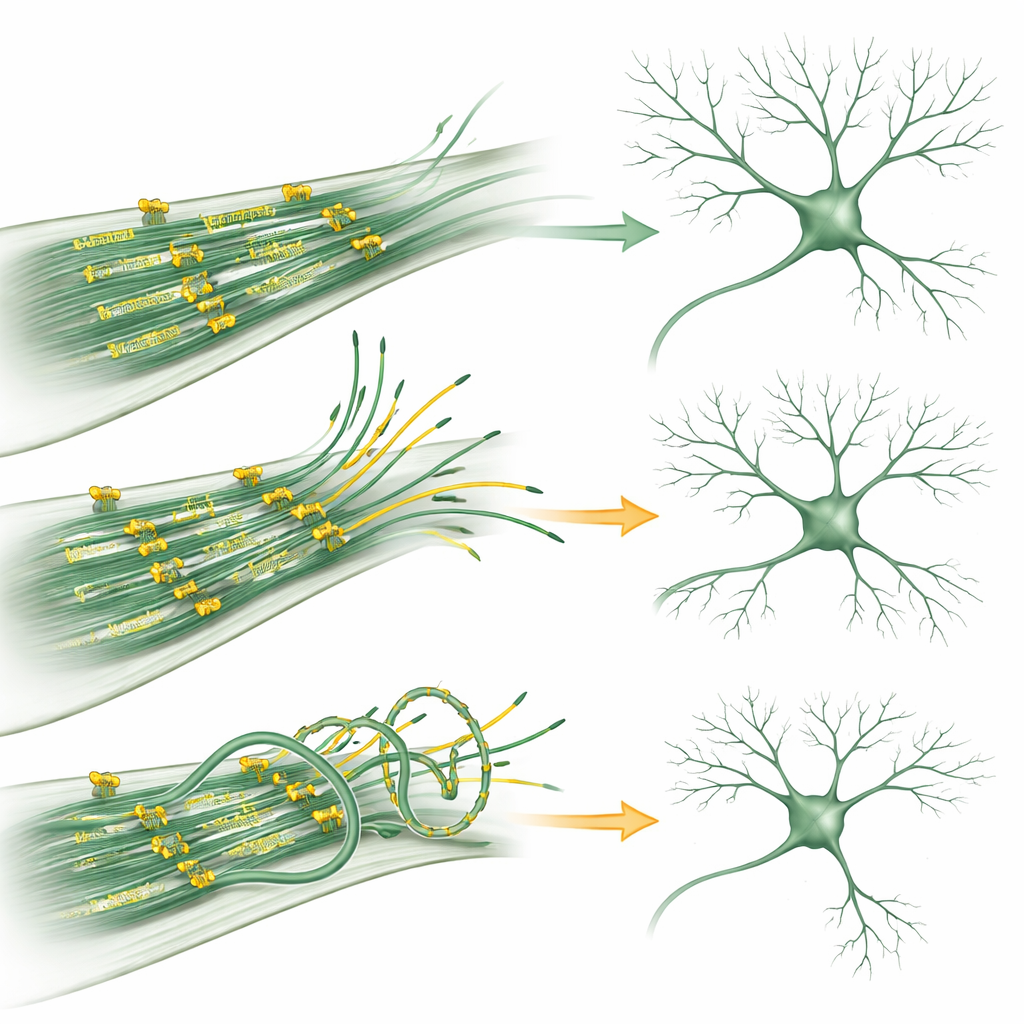
Wanneer een motor faalt
Bepaalde families die getroffen zijn door een zeldzame aandoening genaamd MCLID — gekenmerkt door een kleine hoofdomvang, oogproblemen, zwelling van ledematen en verstandelijke beperking — dragen mutaties in het KIF11‑gen. Het team reconstrueerde twee van dergelijke mutaties in het laboratorium. In neuronen dempten beide gewijzigde vormen van KIF11 de microtubulusdynamiek en verminderden ze dendritische vertakking, vergelijkbaar met KIF11‑overproductie. Gedetailleerde biochemische tests toonden hoe dit gebeurde: de ene mutant verstoorde KIF11’s vermogen om in zijn normale viervoudige structuur samen te zetten, waardoor zijn capaciteit om microtubuli te koppelen verzwakte; de andere vormde nog wel het juiste complex maar schoof veel langzamer langs microtubuli en had een lagere affiniteit voor de brandstofmolecule ATP. Ondanks deze verschillen oefenden beide mutanten afwijkende krachten op microtubuli uit, waardoor de fijne balans tussen stabiliteit en flexibiliteit die neuronen nodig hebben werd verstoord.
Van celvorm naar hersensignalen
De auteurs vroegen vervolgens of deze structurele veranderingen van belang zijn voor de communicatie tussen neuronen. Door piepkleine spontane elektrische gebeurtenissen in gekweekte cellen op te nemen, toonden ze aan dat het verhogen van normaal KIF11 of van beide mutanten de frequentie waarmee synaptische blaasjes hun chemische berichten vrijgaven aanzienlijk verminderde, hoewel de grootte van elke gebeurtenis gelijk bleef. In levende muizen leidde het introduceren van de humaan‑achtige KIF11‑varianten in zich ontwikkelende hippocampusneuronen tot kortere en minder vertakte dendritische bomen, met een ernst die afhankelijk was van de specifieke mutatie en de ontwikkelingsfase. Gezamenlijk koppelen deze bevindingen defecte KIF11‑activiteit aan zowel de fysieke architectuur van neuronen als aan de informatieoverdracht in hersencircuits.
Met licht bestuurbare motoren en een nieuw ziektebeeld
Om te testen of het lokaal veranderen van KIF11‑activiteit voldoende is om neuronen te herbouwen, ontwikkelden de onderzoekers een lichtgevoelige versie van de motor. Korte flitsen violet licht schakelden KIF11 uit in gekozen dendritensegmenten, wat snel de microtubulusgroei verhoogde en binnen enkele minuten de uitgroei van nieuwe vertakkingen opwekte. Tegengestelde lichtpulsen schakelden KIF11 weer in en verminderden de groei terwijl ze knikken en lussen in de microtubulusbundels veroorzaakten. Deze experimenten ondersteunen een eenvoudig beeld: KIF11 fungeert als een rheostaat, of dimmer, voor de interne rails van de neuron — te weinig activiteit laat vertakkingen overgroeien, terwijl te veel activiteit of het verkeerde soort kracht ze verstevigt of vervormt. Bij MCLID lijken gemuteerde KIF11‑eiwitten onevenwichtige krachten op microtubuli uit te oefenen, wat leidt tot instabiele dendritische bomen en verzwakte synaptische communicatie, wat waarschijnlijk bijdraagt aan leer‑ en cognitieve problemen.
Bronvermelding: Wingfield, J.L., Niese, L., Avchalumov, Y. et al. Intellectual disability-causing mutations in KIF11 impair microtubule dynamics and dendritic arborization. Nat Commun 17, 4125 (2026). https://doi.org/10.1038/s41467-026-70522-z
Trefwoorden: neurale microtubuli, dendritische vertakking, kinesine-motorproteïnes, verstandelijke beperking, synaptische transmissie