Clear Sky Science · fr
Les mutations causant un handicap intellectuel dans KIF11 altèrent la dynamique des microtubules et l’arborisation dendritique
Comment de minuscules moteurs cellulaires façonnent la pensée
Notre cerveau dépend de milliards de neurones qui doivent se connecter avec une précision remarquable. Cette étude examine comment un seul moteur moléculaire, appelé KIF11, contribue à sculpter l’« arbre » ramifié des prolongements neuronaux qui reçoivent les signaux, et comment des altérations pathogènes de ce moteur peuvent conduire à une déficience intellectuelle. En observant des neurones vivants au microscope et en sondant la mécanique de KIF11 in vitro et chez la souris, les auteurs révèlent comment cette protéine ajuste le échafaudage interne des neurones et, par conséquent, leur capacité à communiquer.
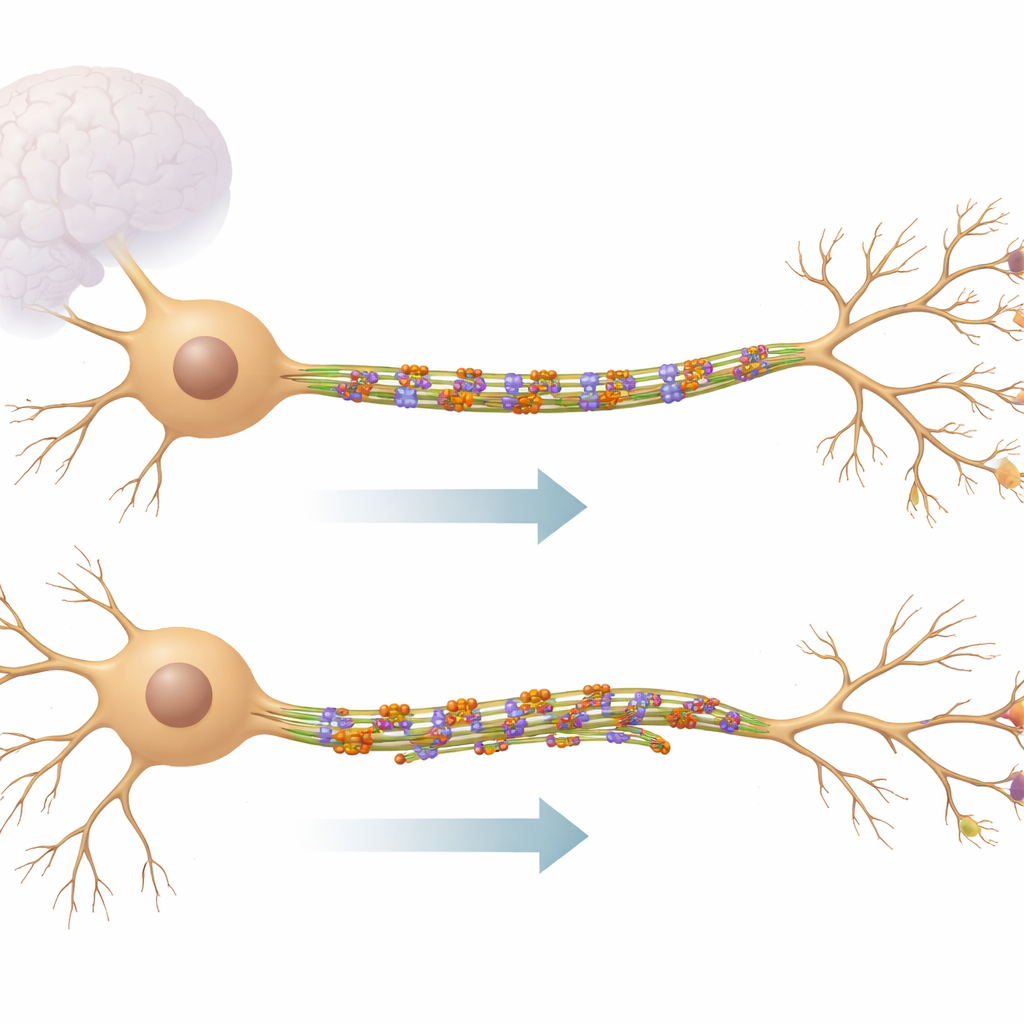
Le réseau ferroviaire intérieur du neurone
Les neurones envoient et reçoivent des informations via de longs prolongements en forme de câbles. À l’intérieur de ces câbles circulent les microtubules, des bâtonnets protéiques rigides qui servent de rails pour le transport des approvisionnements et aident à définir la forme de la cellule. Dans les principales branches réceptrices, appelées dendrites, les microtubules sont orientés dans les deux sens, formant un réseau mixte et dynamique. KIF11 appartient à une famille de minuscules moteurs qui agissent généralement lors de la division cellulaire, mais ce travail montre qu’il reste également actif dans les cellules cérébrales pleinement développées. Plutôt que de tracter des cargaisons, KIF11 relie les microtubules voisins, jouant davantage le rôle d’un frein et d’un stabilisateur que celui d’un camion de livraison.
Maintenir la croissance en équilibre
En utilisant l’imagerie en direct de neurones hippocampiques de souris, les chercheurs ont réduit les niveaux de KIF11 ou bloqué son activité avec des médicaments et suivi les extrémités des microtubules en croissance. Ils ont constaté que lorsque KIF11 était inhibé, une classe particulière de microtubules — ceux dont l’« extrémité moins » pointe vers l’extérieur — devenait plus active, en particulier dans les branches dendritiques secondaires et tertiaires. Cela a favorisé l’apparition et la croissance de ces rails et encouragé la formation de nouvelles branches, rendant l’arbre dendritique plus élaboré. À l’inverse, lorsque KIF11 était surproduit, la dynamique des microtubules ralentissait, les dendrites perdaient de leur complexité et les rails internes se tordaient parfois en boucles, suggérant qu’une force excessive exercée par KIF11 peut plier et contraindre l’échafaudage.
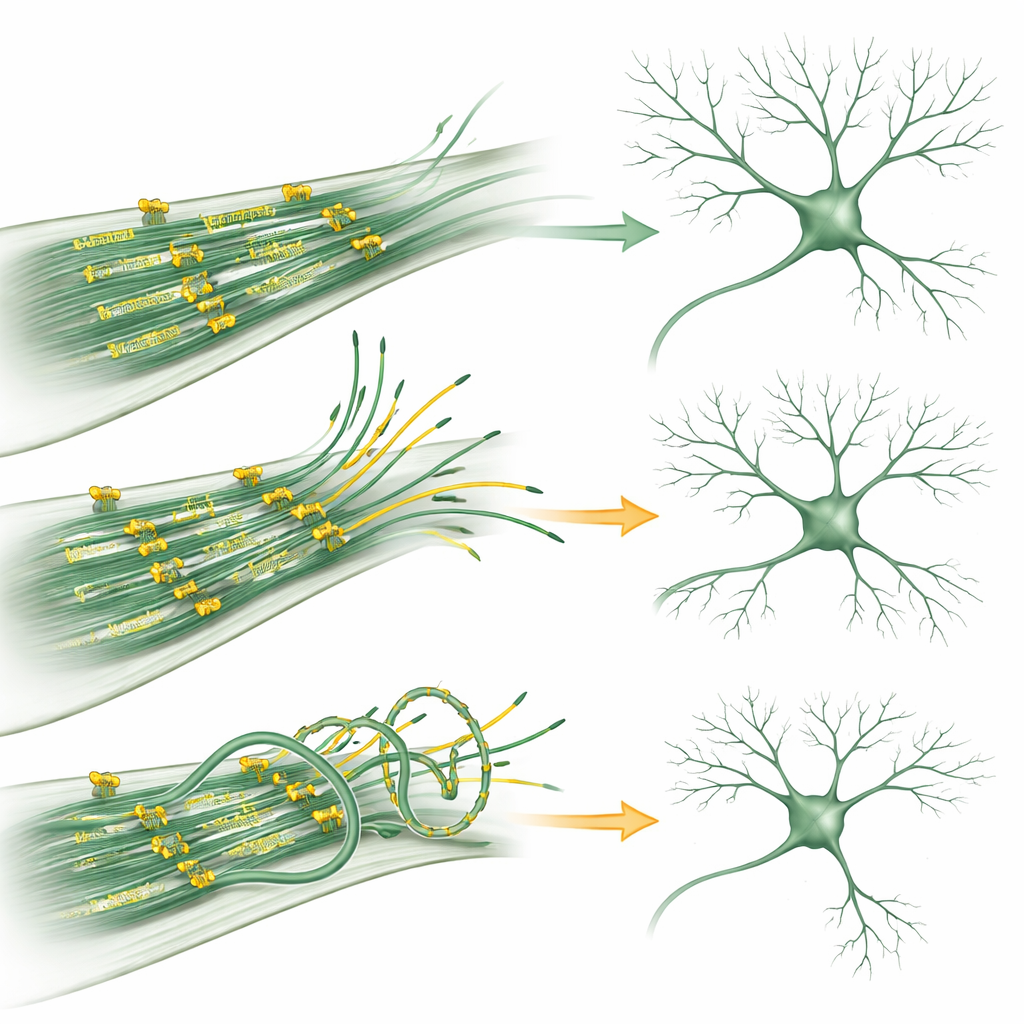
Quand un moteur déraille
Certaines familles affectées par une affection rare appelée MCLID — caractérisée par une petite taille crânienne, des problèmes oculaires, un gonflement des membres et une déficience intellectuelle — portent des mutations dans le gène KIF11. L’équipe a recréé deux de ces mutations en laboratoire. Dans les neurones, les deux formes altérées de KIF11 ont atténué la dynamique des microtubules et réduit la ramification dendritique, de manière similaire à la surproduction de KIF11. Des tests biochimiques détaillés ont révélé le mécanisme : une mutation perturbait la capacité de KIF11 à s’assembler en sa structure normale à quatre unités, affaiblissant sa capacité à relier les microtubules ; l’autre formait correctement le complexe mais glissait le long des microtubules beaucoup plus lentement et avait une affinité réduite pour la molécule d’énergie ATP. Malgré ces différences, les deux mutants exerçaient des forces anormales sur les microtubules, perturbant le fin équilibre entre stabilité et flexibilité dont les neurones ont besoin.
De la forme cellulaire aux signaux cérébraux
Les auteurs se sont ensuite demandé si ces changements structurels affectaient la communication entre neurones. En enregistrant de minuscules événements électriques spontanés dans des cultures cellulaires, ils ont montré qu’augmenter KIF11 normal ou introduire l’un ou l’autre mutant réduisait significativement la fréquence de libération des vésicules synaptiques, même si l’amplitude de chaque événement restait la même. Chez des souris vivantes, l’introduction de variantes humaines de KIF11 dans des neurones hippocampiques en développement conduisait à des arbres dendritiques plus courts et moins ramifiés, la sévérité dépendant de la mutation spécifique et du stade de développement. Ensemble, ces résultats relient une activité KIF11 défectueuse à la fois à l’architecture physique des neurones et au flux d’information à travers les circuits cérébraux.
Moteurs contrôlés par la lumière et nouvelle vision de la maladie
Pour tester si modifier localement l’activité de KIF11 suffit à remodeler les neurones, les chercheurs ont conçu une version du moteur sensible à la lumière. De brefs éclairs de lumière violette désactivaient KIF11 dans des segments dendritiques choisis, augmentant rapidement la croissance des microtubules et déclenchant l’émergence de nouvelles branches en quelques minutes. Des impulsions lumineuses inverses réactivaient KIF11 et réduisaient la croissance tout en induisant des coudes et des boucles dans les faisceaux de microtubules. Ces expériences appuient une image simple : KIF11 agit comme un rhéostat, ou variateur, pour les rails internes du neurone — une activité trop faible laisse les branches proliférer, tandis qu’une activité trop élevée ou une force inappropriée rigidifie ou déforme ces structures. Dans la MCLID, les protéines KIF11 mutantes semblent appliquer des forces déséquilibrées sur les microtubules, entraînant des arbres dendritiques instables et une communication synaptique affaiblie, ce qui contribue probablement aux troubles d’apprentissage et de cognition.
Citation: Wingfield, J.L., Niese, L., Avchalumov, Y. et al. Intellectual disability-causing mutations in KIF11 impair microtubule dynamics and dendritic arborization. Nat Commun 17, 4125 (2026). https://doi.org/10.1038/s41467-026-70522-z
Mots-clés: microtubules neuronaux, ramification dendritique, protéines motrices kinésines, déficience intellectuelle, transmission synaptique