Clear Sky Science · it
Mutazioni di KIF11 che causano disabilità intellettiva compromettono la dinamica dei microtubuli e l’arborizzazione dendritica
Come minuscoli motori cellulari modellano il pensiero
I nostri cervelli dipendono da miliardi di cellule nervose che devono connettersi con precisione estrema. Questo studio esplora come un singolo motore molecolare, chiamato KIF11, contribuisca a scolpire l’albero ramificato dei processi neuronali che ricevono segnali, e come variazioni patologiche in questo motore possano portare a disabilità intellettiva. Osservando neuroni vivi al microscopio e studiando la meccanica di KIF11 in provetta e in topi, gli autori mostrano come questa proteina regoli finemente l’impalcatura interna dei neuroni e, di conseguenza, la loro capacità di comunicare.
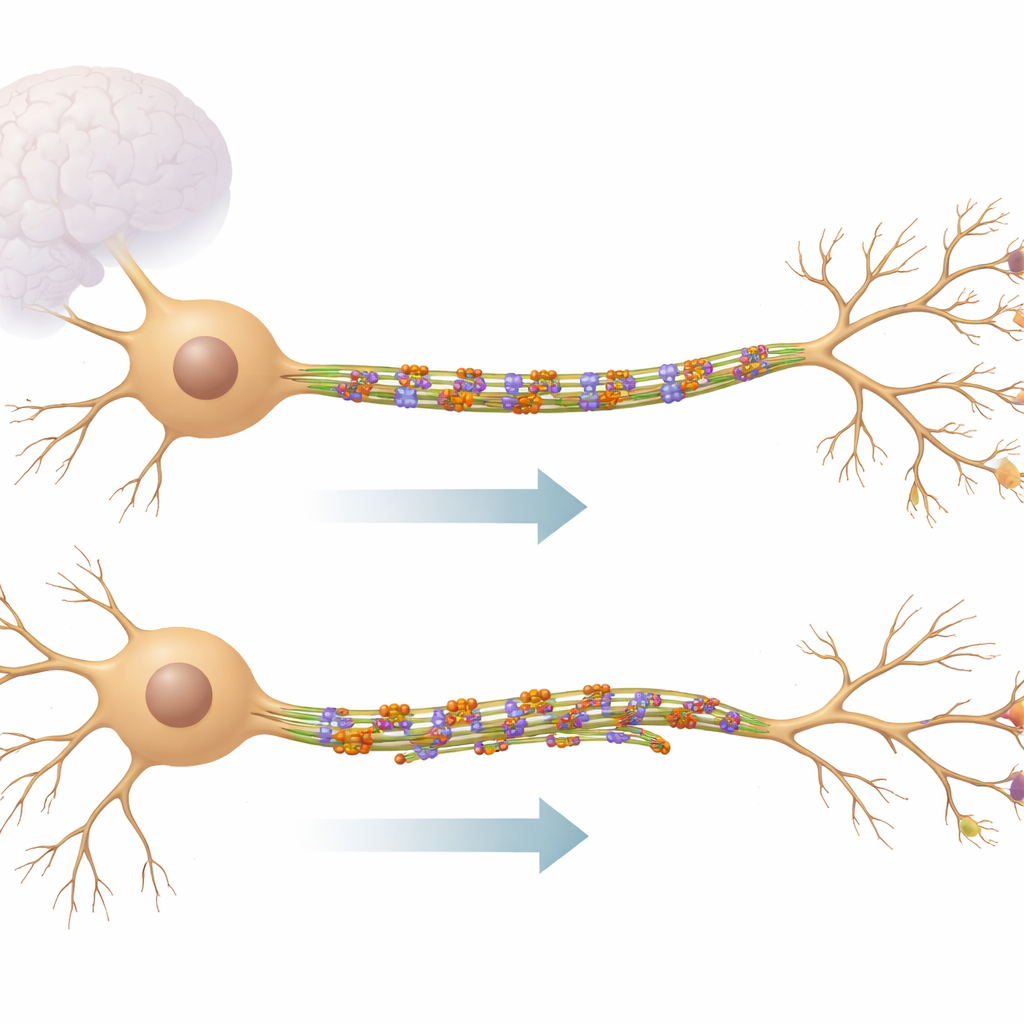
Il sistema ferroviario interno del neurone
I neuroni inviano e ricevono informazioni attraverso estensioni lunghe e simili a cavi. All’interno di questi cavi scorrono i microtubuli, aste proteiche rigide che fungono da binari per il trasporto di materiali e contribuiscono a determinare la forma della cellula. Nei principali rami riceventi, chiamati dendriti, i microtubuli corrono in entrambe le direzioni, creando una rete mista e dinamica. KIF11 appartiene a una famiglia di minuscoli motori che di solito agiscono durante la divisione cellulare, ma questo lavoro dimostra che restano attivi anche nei neuroni completamente sviluppati. Invece di trasportare carichi, KIF11 collega i microtubuli vicini, comportandosi più come un freno e uno stabilizzatore che come un camion da consegna.
Mantenere l’equilibrio della crescita
Utilizzando immagini live di neuroni ippocampali murini, i ricercatori hanno ridotto i livelli di KIF11 o bloccato la sua attività con farmaci e hanno tracciato le punte dei microtubuli in crescita. Hanno scoperto che quando KIF11 era inibito, una classe particolare di microtubuli—quelli con il «capo meno» rivolto verso l’esterno—diventava più attiva, soprattutto nei rami dendritici secondari e terziari. Ciò incrementava la comparsa e la crescita di questi binari e favoriva la formazione di nuovi rami, rendendo l’albero dendritico più elaborato. Al contrario, quando KIF11 veniva sovraespresso, la dinamica dei microtubuli rallentava, i dendriti diventavano meno complessi e i binari interni a volte si attorcigliavano e formavano anse, suggerendo che una forza eccessiva da parte di KIF11 può piegare e sollecitare l’impalcatura.
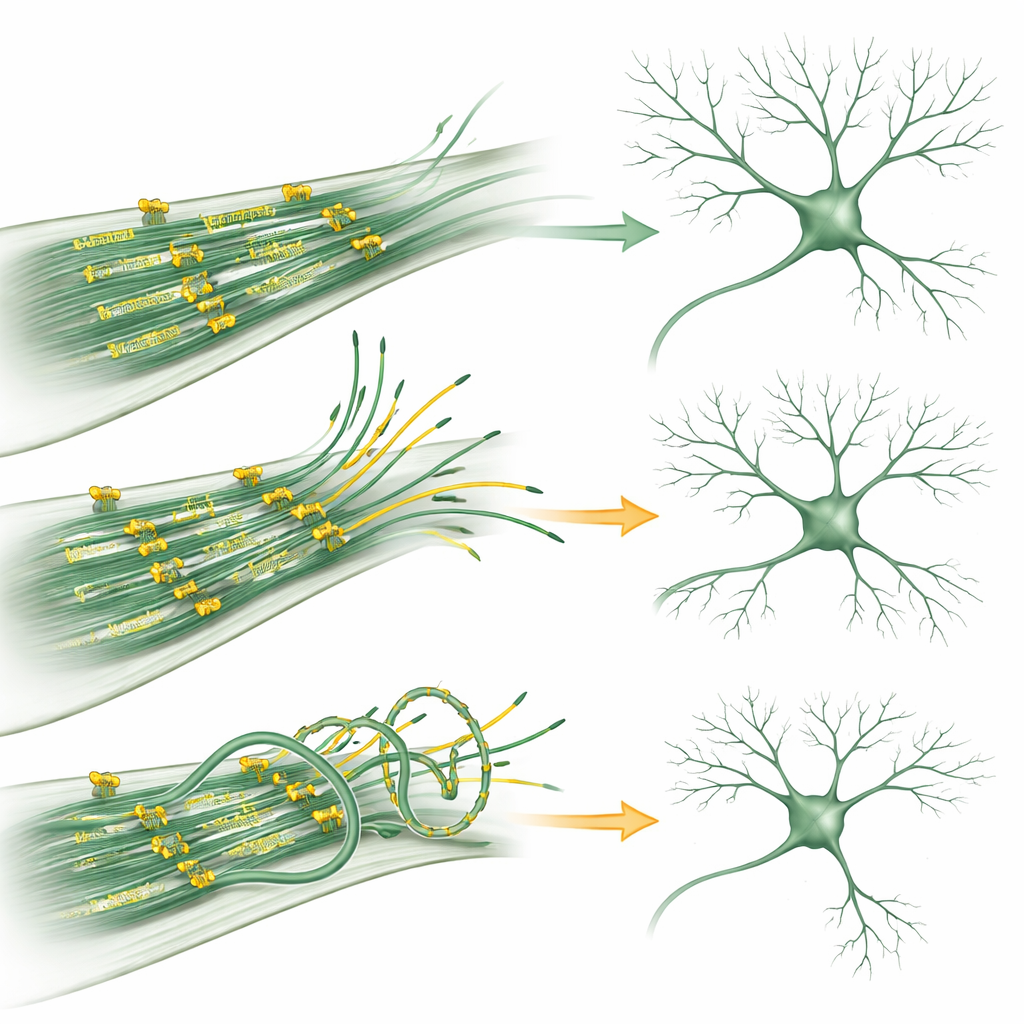
Quando un motore si guasta
Alcune famiglie colpite da una rara condizione chiamata MCLID—caratterizzata da microcefalia, problemi oculari, gonfiore degli arti e disabilità intellettiva—presentano mutazioni nel gene KIF11. Il gruppo ha ricreato in laboratorio due di queste mutazioni. Nei neuroni, entrambe le forme alterate di KIF11 attenuavano la dinamica dei microtubuli e riducevano la ramificazione dendritica, in modo simile alla sovraespressione di KIF11. Test biochimici dettagliati hanno rivelato il meccanismo: un mutante comprometteva la capacità di KIF11 di assemblarsi nella sua struttura normale a quattro unità, indebolendo la sua capacità di collegare i microtubuli; l’altro formava ancora il complesso corretto ma scivolava lungo i microtubuli molto più lentamente e mostrava minore affinità per la molecola energetica ATP. Nonostante queste differenze, entrambi i mutanti continuavano a esercitare forze anomale sui microtubuli, squilibrando l’equilibrio sottile tra stabilità e flessibilità necessario ai neuroni.
Dalla forma cellulare ai segnali cerebrali
Gli autori si sono poi chiesti se questi cambiamenti strutturali avessero importanza per la comunicazione tra neuroni. Registrando piccoli eventi elettrici spontanei in cellule coltivate, hanno mostrato che aumentare la quantità di KIF11 normale o introdurre uno dei due mutanti riduceva significativamente la frequenza con cui le vescicole sinaptiche rilasciavano i loro messaggi chimici, anche se l’ampiezza di ciascun evento rimaneva invariata. In topi vivi, l’introduzione delle varianti umane di KIF11 in neuroni ippocampali in sviluppo ha portato ad alberi dendritici più corti e meno ramificati, con la gravità degli effetti dipendente dalla mutazione specifica e dalla fase di sviluppo. Nel loro insieme, questi risultati collegano un’attività anomala di KIF11 sia all’architettura fisica dei neuroni sia al flusso di informazioni attraverso i circuiti cerebrali.
Motori controllati dalla luce e una nuova visione della malattia
Per verificare se modificare localmente l’attività di KIF11 fosse sufficiente a rimodellare i neuroni, i ricercatori hanno ingegnerizzato una versione sensibile alla luce del motore. Brevi lampi di luce violetta spegnevano KIF11 in porzioni scelte di dendrite, aumentando rapidamente la crescita dei microtubuli e inducendo la germinazione di nuovi rami in pochi minuti. Impulsi di luce opposti riaccendevano KIF11 e riducevano la crescita, inducendo nel contempo piegature e anse nei fasci di microtubuli. Questi esperimenti supportano un quadro semplice: KIF11 agisce come un reostato, o un dimmer, per i binari interni del neurone—troppa poca attività lascia proliferare i rami, mentre troppa attività o forze del tipo sbagliato irrigidiscono o deformano la struttura. Nella MCLID, le proteine KIF11 mutanti sembrano applicare forze sbilanciate sui microtubuli, portando a alberi dendritici instabili e a una comunicazione sinaptica indebolita, fattori che probabilmente contribuiscono ai problemi di apprendimento e cognizione.
Citazione: Wingfield, J.L., Niese, L., Avchalumov, Y. et al. Intellectual disability-causing mutations in KIF11 impair microtubule dynamics and dendritic arborization. Nat Commun 17, 4125 (2026). https://doi.org/10.1038/s41467-026-70522-z
Parole chiave: microtubuli neuronali, ramificazione dendritica, proteine motrici chinesine, disabilità intellettiva, trasmissione sinaptica