Clear Sky Science · de
Mutationen im KIF11, die geistige Behinderung verursachen, beeinträchtigen die Dynamik von Mikrotubuli und die dendritische Verästelung
Wie winzige zelluläre Motoren Denken formen
Unser Gehirn beruht auf Milliarden von Nervenzellen, die mit höchster Präzision verschaltet werden müssen. Diese Studie untersucht, wie ein einzelner molekularer Motor, genannt KIF11, die Verzweigung des „Baums“ von Nervenfortsätzen, die Signale empfangen, mitgestaltet und wie krankheitsauslösende Veränderungen in diesem Motor zu geistiger Behinderung führen können. Indem die Autoren lebende Neuronen unter dem Mikroskop beobachteten und KIF11s Mechanik in Reagenzgläsern und in Mäusen untersuchten, zeigen sie, wie dieses Protein das innere Gerüst der Neuronen feinjustiert und damit deren Kommunikationsfähigkeit beeinflusst.
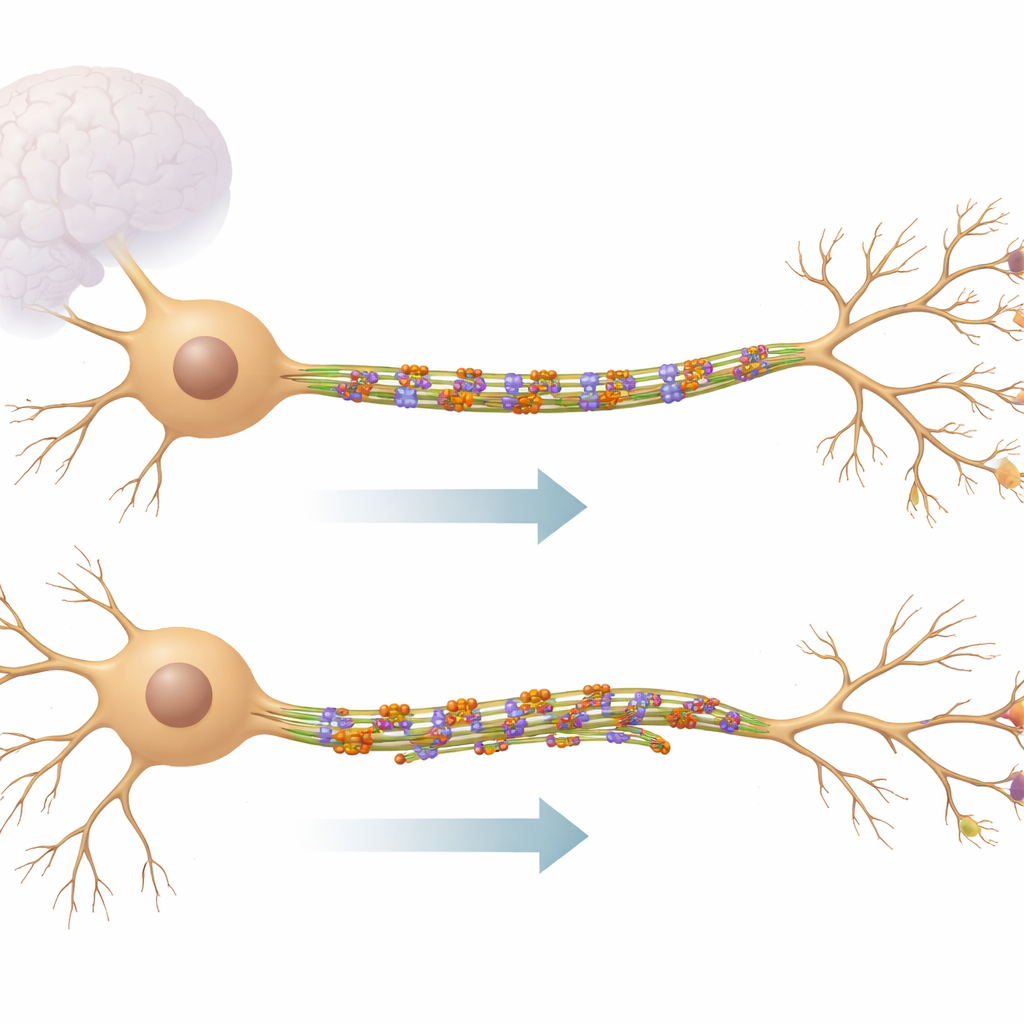
Das innere Eisenbahnsystem der Nervenzelle
Neuronen senden und empfangen Informationen über lange, kabelartige Fortsätze. Innerhalb dieser Kabel verlaufen Mikrotubuli, steife Proteinstäbe, die wie Gleise für den Transport von Material dienen und die Form der Zelle mitbestimmen. In den hauptsächlichen Eingangsästen, den Dendriten, verlaufen Mikrotubuli in beide Richtungen und bilden ein gemischtes, dynamisches Netzwerk. KIF11 gehört zu einer Familie winziger Motoren, die normalerweise während der Zellteilung arbeiten, aber diese Arbeit zeigt, dass es auch in ausgereiften Gehirnzellen aktiv bleibt. Anstatt Fracht zu transportieren, verbindet KIF11 benachbarte Mikrotubuli miteinander und wirkt eher wie eine Bremse und Stabilisator als wie ein Lieferwagen.
Wachstum im Gleichgewicht halten
Mithilfe von Live‑Aufnahmen hippocampaler Mausneuronen reduzierten die Forschenden KIF11‑Spiegel oder blockierten seine Aktivität mit Medikamenten und verfolgten die Spitzen wachsender Mikrotubuli. Sie stellten fest, dass bei Hemmung von KIF11 eine bestimmte Klasse von Mikrotubuli – jene mit dem „Minusende“ nach außen – aktiver wurde, besonders in sekundären und tertiären dendritischen Ästen. Das förderte das Entstehen und Wachstum dieser Schienen und begünstigte neue Verzweigungen, wodurch der dendritische Baum komplexer wurde. Umgekehrt verlangsamte Überexpression von KIF11 die Mikrotubuli‑Dynamik, Dendriten wurden weniger verzweigt, und die inneren Tracks verdrehten und schlängelten sich mitunter, was darauf hindeutet, dass zu starke Kräfte durch KIF11 das Gerüst biegen und belasten können.
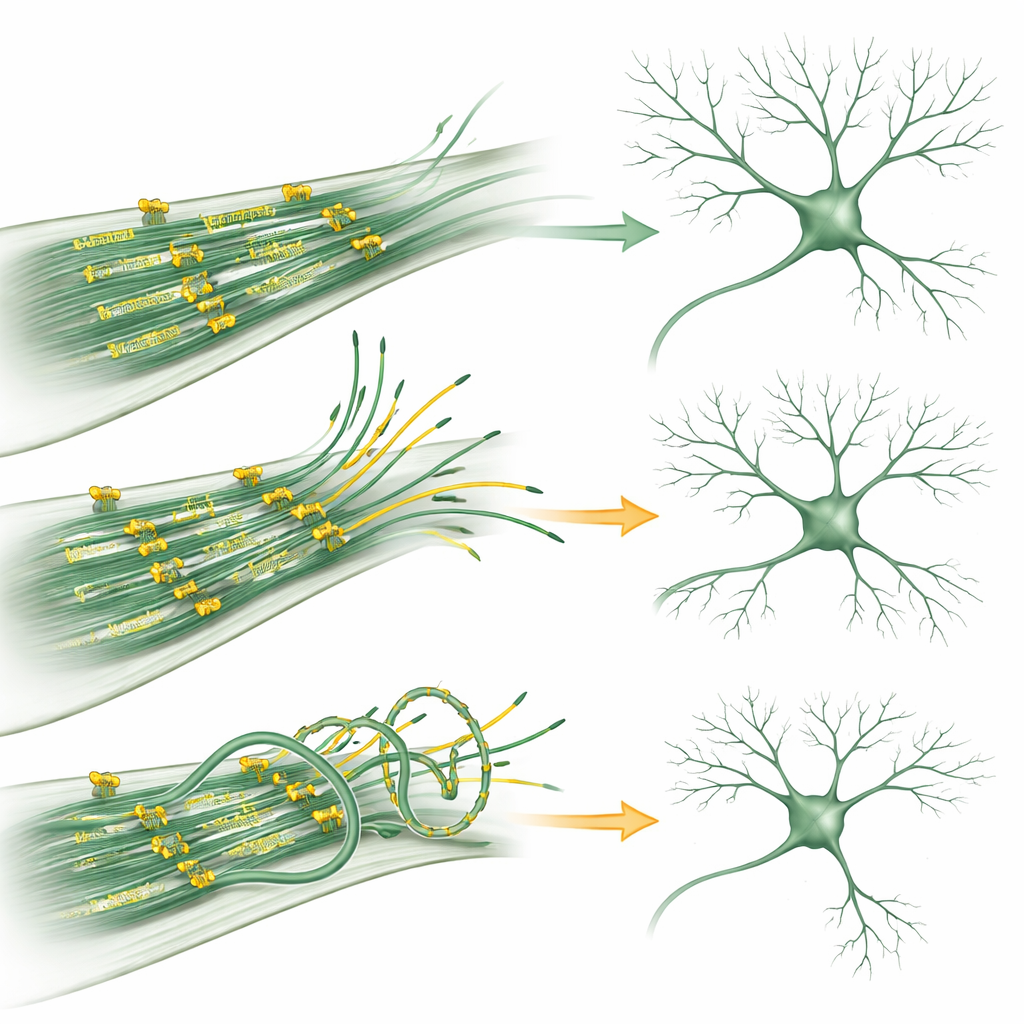
Wenn ein Motor fehlerhaft wird
Bestimmte Familien, die von einer seltenen Erkrankung namens MCLID betroffen sind – gekennzeichnet durch kleinen Kopf, Augenprobleme, Schwellungen der Gliedmaßen und geistige Behinderung – tragen Mutationen im KIF11‑Gen. Das Team rekonstruierte zwei solche Mutationen im Labor. In Neuronen dämpften beide veränderten Formen von KIF11 die Mikrotubuli‑Dynamik und reduzierten die dendritische Verzweigung, ähnlich wie bei KIF11‑Überproduktion. Detaillierte biochemische Tests zeigten wie: Ein Mutant störte die Fähigkeit von KIF11, sich zu seiner normalen Viererstruktur zusammenzufügen, und schwächte damit seine Kapazität, Mikrotubuli zu verbinden; der andere bildete zwar den korrekten Komplex, glitt aber deutlich langsamer entlang der Mikrotubuli und wies eine geringere Affinität zum Energieträger ATP auf. Trotz dieser Unterschiede übten beide Mutanten weiterhin abnorme Kräfte auf Mikrotubuli aus und störten das feine Gleichgewicht von Stabilität und Flexibilität, das Neuronen benötigen.
Von Zellform zu Gehirnsignalen
Die Autoren fragten dann, ob diese strukturellen Veränderungen für die Kommunikation zwischen Neuronen von Bedeutung sind. Durch Aufzeichnen kleiner spontaner elektrischer Ereignisse in kultivierten Zellen zeigten sie, dass die Erhöhung von normalem KIF11 oder das Vorhandensein eines der Mutanten die Häufigkeit der Freisetzung synaptischer Vesikelbotschaften deutlich verringerte, obwohl die Größe einzelner Ereignisse gleich blieb. In lebenden Mäusen führte die Einführung der humanähnlichen KIF11‑Varianten in sich entwickelnde hippocampale Neuronen zu kürzeren und weniger verzweigten dendritischen Bäumen, wobei der Schweregrad von der jeweiligen Mutation und dem Entwicklungsstadium abhing. Gemeinsam verknüpfen diese Befunde fehlerhafte KIF11‑Aktivität sowohl mit der physischen Architektur von Neuronen als auch mit dem Informationsfluss in Hirnschaltkreisen.
Lichtgesteuerte Motoren und ein neuer Krankheitsblick
Um zu prüfen, ob die lokale Veränderung der KIF11‑Aktivität ausreicht, um Neuronen umzustrukturieren, konstruierten die Forschenden eine lichtempfindliche Version des Motors. Kurze violette Lichtblitze schalteten KIF11 in ausgewählten Dendritensegmenten aus, steigerten rasch das Mikrotubuli‑Wachstum und lösten innerhalb von Minuten das Auskeimen neuer Verzweigungen aus. Entgegengesetzte Lichtpulse schalteten KIF11 ein und reduzierten das Wachstum, während sie Kinken und Schleifen in den Mikrotubuli‑Bündeln induzierten. Diese Experimente stützen ein einfaches Bild: KIF11 wirkt wie ein Rheostat oder Dimmschalter für die inneren Schienen der Nervenzelle – zu wenig Aktivität lässt Äste überwachsen, zu viel oder falsche Kräfte verhärten oder verformen sie. Bei MCLID scheinen mutierte KIF11‑Proteine unausgewogene Kräfte auf Mikrotubuli auszuüben, was zu instabilen dendritischen Bäumen und abgeschwächter synaptischer Kommunikation führt und wahrscheinlich zu Lern‑ und kognitiven Problemen beiträgt.
Zitation: Wingfield, J.L., Niese, L., Avchalumov, Y. et al. Intellectual disability-causing mutations in KIF11 impair microtubule dynamics and dendritic arborization. Nat Commun 17, 4125 (2026). https://doi.org/10.1038/s41467-026-70522-z
Schlüsselwörter: neurale Mikrotubuli, dendritische Verzweigung, Kinesin‑Motorproteine, geistige Behinderung, synaptische Übertragung