Clear Sky Science · pt
Espectrometria de massas revela a conservação evolutiva dos complexos de ficobiliproteínas
Micróbios antigos com impacto nos dias de hoje
Cianobactérias — micróbios fotossintéticos minúsculos — ajudaram a transformar a atmosfera primitiva da Terra ao liberar oxigênio e ainda sustentam hoje os ciclos globais do carbono e do nitrogênio. Elas prosperam desde fontes termais escaldantes até lagos gelados, e ainda assim muitas compartilham o mesmo tipo de maquinaria de captura de luz. Este estudo faz uma pergunta simples, porém profunda: como essas peças coletoras de luz permaneceram tão eficientes por mais de três bilhões de anos, mesmo quando as cianobactérias se espalharam por ambientes extremamente diferentes?
Como esses micróbios captam a luz
As cianobactérias usam grandes estruturas moleculares em forma de “antena”, chamadas ficoibilissomos, para captar a luz solar e transferir a energia para os motores fotossintéticos centrais dentro da célula. Os ficoibilissomos são formados por proteínas coloridas conhecidas como ficobiliproteínas, sobretudo ficocianina e aloficocianina, que se organizam como rosquinhas empilhadas. Cada “rosquinha” é feita de pares repetidos de cadeias protéicas que ligam moléculas pigmentares. O tamanho e a forma gerais da antena podem variar bastante entre espécies, mas os blocos de construção individuais têm aparência surpreendentemente similar, sugerindo um desenho profundamente conservado.
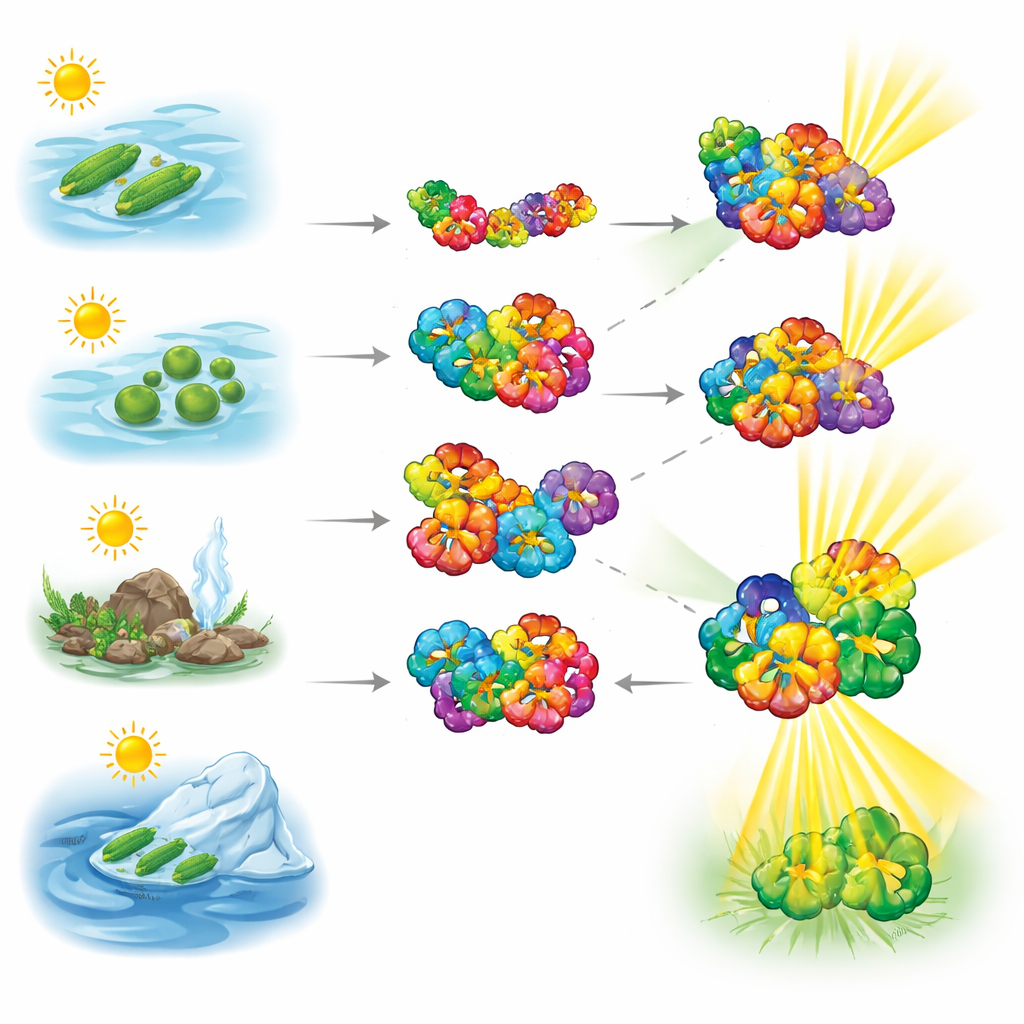
Examinando blocos flexíveis com pesagem de precisão
Para ver como essas proteínas captadoras de luz se comportam, os pesquisadores usaram espectrometria de massas em estado nativo, uma técnica que pesa delicadamente complexos protéicos intactos sem fragmentá-los. Eles examinaram ficobiliproteínas de cianobactérias coletadas em habitats muito diferentes — águas hipersalinas, água doce, ambientes quentes e regiões frias. As medições mostraram que a ficocianina alterna facilmente entre pares menores e hexâmeros maiores em forma de rosquinha, revelando uma natureza altamente dinâmica. A aloficocianina, por outro lado, tendia muito mais a permanecer em sua forma hexamérica, sugerindo um núcleo mais robusto que ancora o sistema de antena.
Misturando partes de espécies diferentes
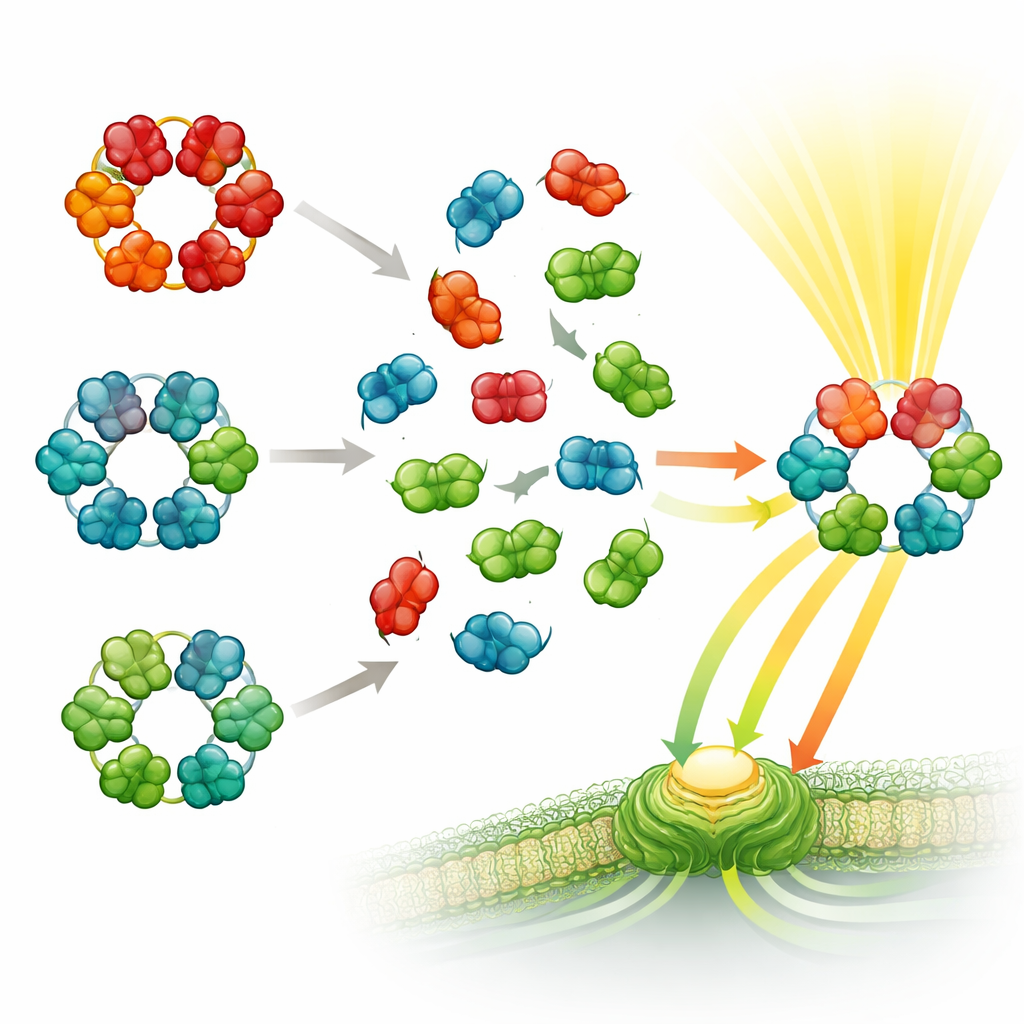
A equipe então realizou um experimento molecular de “misturar e combinar”. Eles combinaram ficobiliproteínas purificadas de pares de espécies que vivem em ambientes distintos ou pertencem a ramos distantes da árvore genealógica das cianobactérias. A espectrometria de massas revelou que as proteínas se montaram rapidamente em complexos híbridos: hexâmeros formados por subunidades originárias de duas espécies diferentes. Isso ocorreu mesmo quando as espécies eram apenas remotamente relacionadas, e mesmo quando as proteínas foram purificadas, afastadas da maioria de seus componentes auxiliares habituais. Contudo, uma regra manteve-se firme: partes de ficocianina só se misturaram com outras ficocianinas, e aloficocianina com aloficocianina — não foram detectadas “rosquinhas” mistas contendo ambos os tipos.
Pistas ao nível atômico a partir de predição estrutural
Para entender por que algumas misturas se formam facilmente e outras nunca aparecem, os pesquisadores recorreram ao AlphaFold2, uma avançada ferramenta de predição de estruturas protéicas. Eles modelaram hexâmeros puros e híbridos e examinaram quão bem as superfícies protéicas previstas se encaixavam. Complexos híbridos feitos do mesmo tipo de ficobiliproteína, mas de espécies diferentes, mostraram interfaces apertadas e confiáveis, em acordo com a evidência experimental de que esses montagens são estáveis. Em contraste, hexâmeros hipotéticos contendo uma mistura de ficocianina e aloficocianina apresentaram encaixes piores e menos contatos, indicando que tais combinações são estruturalmente desfavorecidas. A comparação detalhada das posições de aminoácidos nas zonas de contato revelou um punhado de resíduos conservados que atuam como chaves de forma, garantindo que apenas tipos compatíveis se encaixem bem.
O que isso significa para a vida e para a tecnologia
Os achados sugerem que o desenho central das ficobiliproteínas foi fortemente preservado ao longo de bilhões de anos, permitindo que subunidades de cianobactérias distantes funcionem quase de forma intercambiável. Ao mesmo tempo, mudanças sutis nas superfícies de contato impedem combinações desencontradas de diferentes tipos de ficobiliproteínas, mantendo o fluxo de energia pela antena altamente eficiente. Esse equilíbrio entre flexibilidade e especificidade provavelmente ajudou as cianobactérias a colonizar muitos habitats ao mesmo tempo em que mantinham uma fotossíntese confiável. Em termos práticos, o trabalho indica que pode ser possível projetar novos sistemas de captura de luz — trocando subunidades compatíveis de diferentes espécies — para ajustar quais cores de luz são capturadas, com aplicações potenciais em bioenergia, biotecnologia e materiais sustentáveis.
Citação: Sound, J.K., Bianchini, G., Ashok, T.A. et al. Mass spectrometry reveals the evolutionary conservation of phycobiliprotein complexes. Nat Commun 17, 2834 (2026). https://doi.org/10.1038/s41467-026-69558-y
Palavras-chave: cianobactérias, fotossíntese, captura de luz, evolução de proteínas, espectrometria de massas