Clear Sky Science · it
La spettrometria di massa rivela la conservazione evolutiva dei complessi di ficobiliproteine
Microbi antichi con un impatto tuttora attuale
I cianobatteri—minuscoli microbi fotosintetici—hanno contribuito a trasformare l’atmosfera primordiale della Terra rilasciando ossigeno e tuttora sostengono i cicli globali del carbonio e dell’azoto. Prosperano da sorgenti caldissime a laghi ghiacciati, eppure molti condividono lo stesso tipo di meccanismi per catturare la luce. Questo studio pone una domanda semplice ma profonda: come hanno fatto questi componenti raccoglitori di luce a rimanere così efficaci nel loro ruolo per oltre tre miliardi di anni, mentre i cianobatteri si sono espansi in ambienti drasticamente diversi?
Come questi microbi catturano la luce
I cianobatteri utilizzano grandi strutture molecolari “antenna”, chiamate ficobilisomi, per catturare la luce solare e trasferire l’energia ai motori fotosintetici centrali all’interno della cellula. I ficobilisomi sono costruiti da proteine colorate note come ficobiliproteine, principalmente ficocianina e alloficocianina, che si assemblano come ciambelle impilate. Ogni ciambella è composta da coppie ripetute di catene proteiche che legano molecole di pigmento. La dimensione e la forma complessiva dell’antenna possono variare molto tra le specie, ma i singoli mattoni strutturali appaiono sorprendentemente simili, suggerendo un progetto profondamente conservato.
Esplorare mattoni flessibili con pesature di precisione
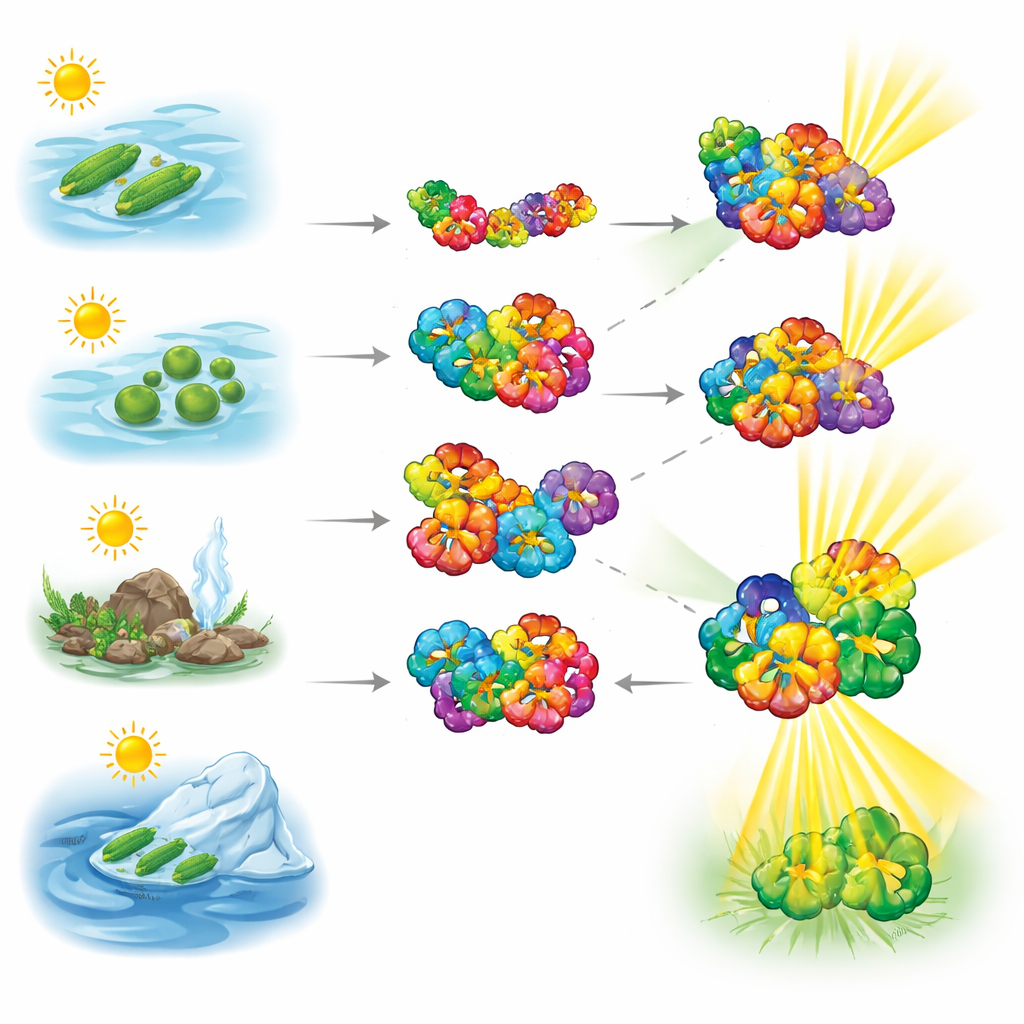
Per capire come si comportano queste proteine raccoglitrici di luce, i ricercatori hanno usato la spettrometria di massa nativa, una tecnica che pesa delicatamente complessi proteici intatti senza disassemblarli. Hanno esaminato ficobiliproteine provenienti da cianobatteri raccolti in habitat molto diversi—acque ipersaline, acque dolci, ambienti caldi e regioni fredde. Le misurazioni hanno mostrato che la ficocianina passa facilmente tra coppie più piccole e ciambelle più grandi a forma di esameri, rivelando una natura altamente dinamica. L’alloficocianina, al contrario, tendeva molto più a restare nella sua forma esamerica, suggerendo un nucleo più stabile che ancoraa il sistema antenna.
Mischiare parti provenienti da specie diverse
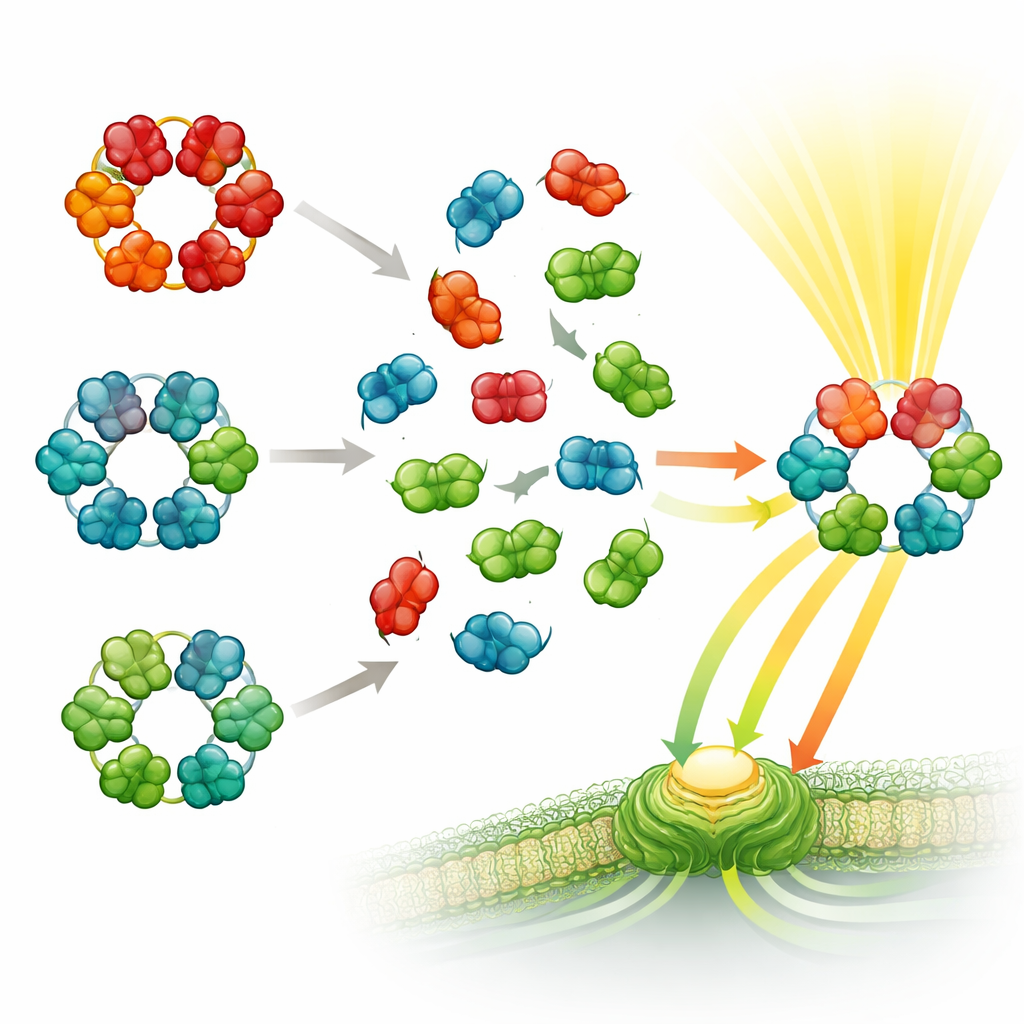
Il gruppo ha quindi eseguito un esperimento molecolare di «mix-and-match». Hanno combinato ficobiliproteine purificate da coppie di specie che vivono in ambienti diversi o appartengono a rami distanti dell’albero filogenetico dei cianobatteri. La spettrometria di massa ha rivelato che le proteine si assemblavano rapidamente in complessi ibridi: esameri costruiti da subunità provenienti da due specie diverse. Ciò avveniva anche quando le specie erano solo lontanamente correlate, e anche quando le proteine erano purificate dalla maggior parte dei loro componenti ausiliari abituali. Tuttavia, una regola rimaneva ferma: le parti di ficocianina si mescolavano solo con altre ficocianine, e le alloficocianine solo con altre alloficocianine—non sono state rilevate ciambelle miste contenenti entrambi i tipi.
Indizi a livello atomico dalla predizione strutturale
Per capire perché alcune miscele si formano facilmente e altre non compaiono mai, i ricercatori si sono rivolti ad AlphaFold2, uno strumento avanzato di predizione della struttura proteica. Hanno modellato sia esameri puri sia ibridi e hanno esaminato quanto strettamente si incastrassero le superfici proteiche predette. I complessi ibridi costituiti dallo stesso tipo di ficobiliproteina ma provenienti da specie diverse mostravano interfacce compatte e affidabili, in accordo con le evidenze sperimentali che questi assemblaggi sono stabili. Al contrario, gli esameri ipotetici contenenti un misto di ficocianina e alloficocianina mostravano adattamenti peggiori e meno contatti, indicando che tali combinazioni sono sfavorite strutturalmente. Il confronto dettagliato delle posizioni degli aminoacidi nelle zone di contatto ha rivelato una manciata di residui conservati che agiscono come chiavi di forma, assicurando che solo tipi corrispondenti si leghino bene fra loro.
Cosa significa per la vita e per la tecnologia
I risultati suggeriscono che il progetto di base delle ficobiliproteine è stato fortemente preservato per miliardi di anni, permettendo a subunità di cianobatteri lontani tra loro di funzionare quasi in modo intercambiabile. Allo stesso tempo, cambiamenti sottili alle superfici di contatto impediscono combinazioni scorrette di diversi tipi di ficobiliproteine, mantenendo il flusso di energia attraverso l’antenna molto efficiente. Questo equilibrio tra flessibilità e specificità probabilmente ha aiutato i cianobatteri a colonizzare molti habitat pur mantenendo una fotosintesi affidabile. In termini pratici, il lavoro suggerisce che potrebbe essere possibile progettare nuovi sistemi di raccolta della luce—scambiando subunità compatibili provenienti da specie diverse—to modulare quali colori di luce vengono catturati, con potenziali applicazioni in bioenergia, biotecnologia e materiali sostenibili.
Citazione: Sound, J.K., Bianchini, G., Ashok, T.A. et al. Mass spectrometry reveals the evolutionary conservation of phycobiliprotein complexes. Nat Commun 17, 2834 (2026). https://doi.org/10.1038/s41467-026-69558-y
Parole chiave: cianobatteri, fotosintesi, cattura della luce, evoluzione delle proteine, spettrometria di massa