Clear Sky Science · fr
La spectrométrie de masse révèle la conservation évolutive des complexes de phycobiliprotéines
Microbes anciens au rôle contemporain
Les cyanobactéries — minuscules microbes photosynthétiques — ont contribué à transformer l’atmosphère primitive de la Terre en libérant de l’oxygène et soutiennent encore aujourd’hui les cycles globaux du carbone et de l’azote. Elles prospèrent aussi bien dans des sources chaudes que dans des lacs glacés, et beaucoup partagent pourtant le même type de machinerie de capture de la lumière. Cette étude pose une question simple mais profonde : comment ces éléments collecteurs de lumière sont-ils restés aussi efficaces pendant plus de trois milliards d’années, alors que les cyanobactéries ont colonisé des environnements si divers ?
Comment ces microbes captent la lumière
Les cyanobactéries utilisent de grandes structures moléculaires « antennes », appelées phycobilisomes, pour capter la lumière du soleil et transmettre l’énergie aux moteurs photosynthétiques centraux à l’intérieur de la cellule. Les phycobilisomes sont constitués de protéines colorées appelées phycobiliprotéines, principalement la phycocyanine et l’allophycocyanine, qui s’assemblent comme des beignets empilés. Chaque beignet est composé de paires répétées de chaînes protéiques qui lient des pigments. La taille et la forme globales de l’antenne peuvent beaucoup varier selon les espèces, mais les blocs de construction individuels présentent une grande similarité, suggérant un plan profondément conservé.
Explorer des éléments flexibles par un pesage précis
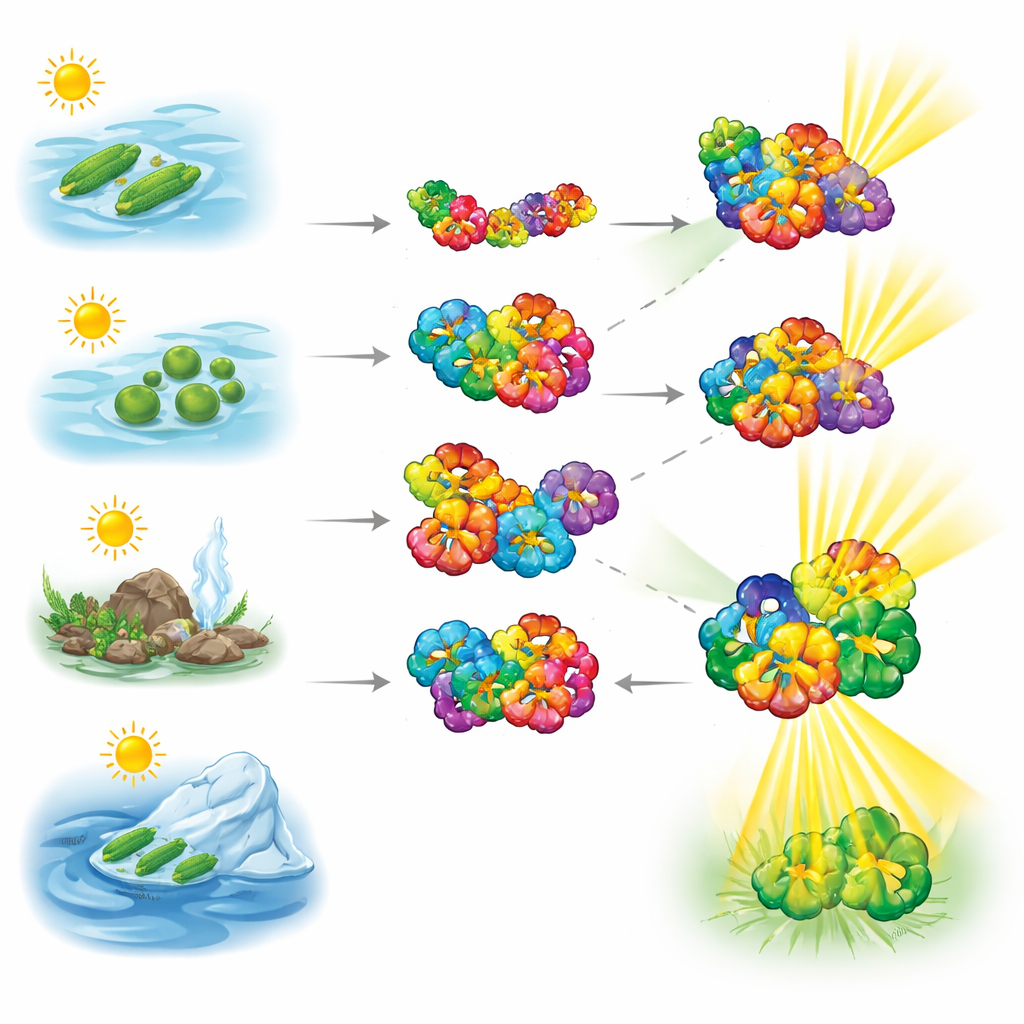
Pour voir comment ces protéines collectrices de lumière se comportent, les chercheurs ont utilisé la spectrométrie de masse native, une technique qui pèse délicatement des complexes protéiques intacts sans les dissocier. Ils ont examiné des phycobiliprotéines provenant de cyanobactéries collectées dans des habitats très différents — eaux hypersalines, eau douce, environnements chauds et régions froides. Les mesures ont montré que la phycocyanine bascule facilement entre de petites paires et de plus grands hexamères en forme de beignet, révélant une grande dynamique. L’allophycocyanine, en revanche, avait beaucoup plus tendance à rester sous forme hexamérique, suggérant un noyau plus robuste qui ancre le système d’antenne.
Mélanger des pièces provenant d’espèces différentes
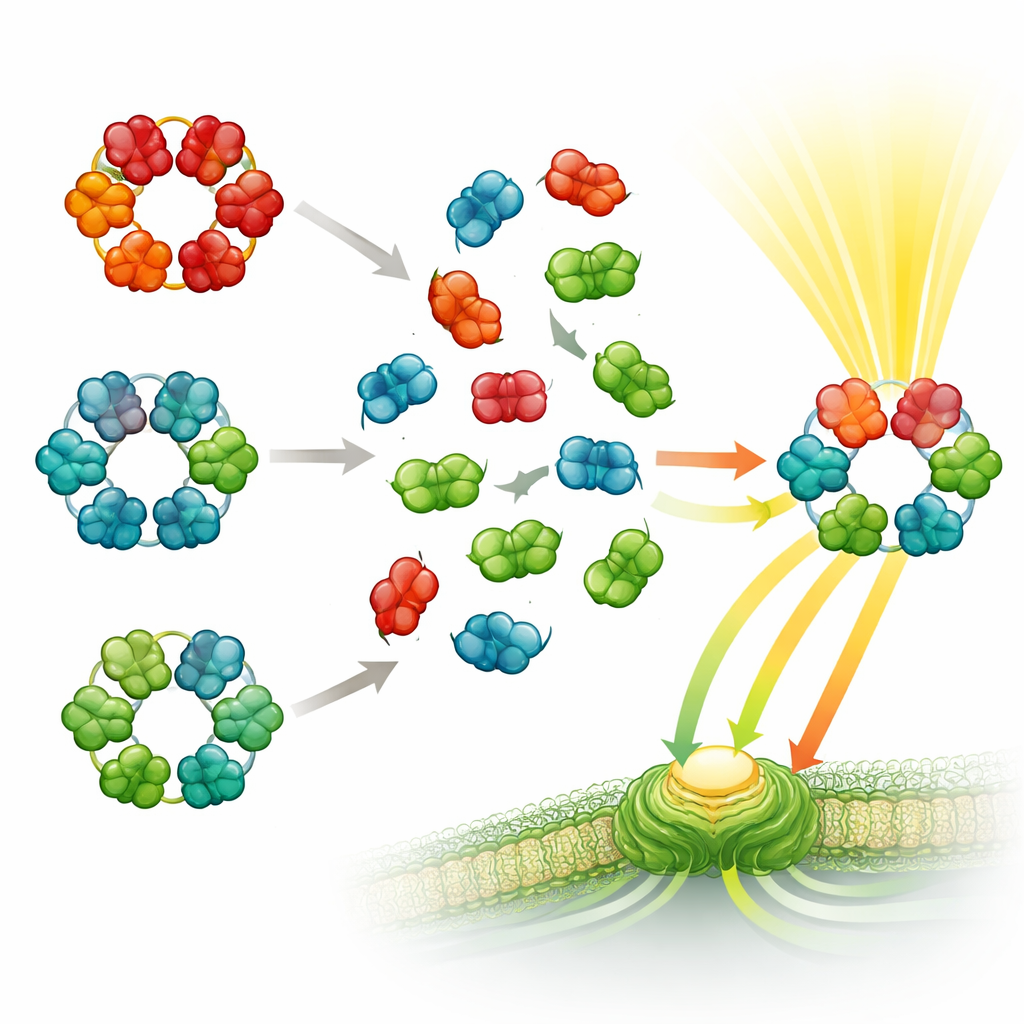
L’équipe a ensuite réalisé une expérience moléculaire de « mix-and-match ». Ils ont combiné des phycobiliprotéines purifiées par paires d’espèces vivant dans des environnements différents ou appartenant à des branches éloignées de l’arbre phylogénétique des cyanobactéries. La spectrométrie de masse a révélé que les protéines s’assemblaient rapidement en complexes hybrides : des hexamères construits à partir de sous-unités provenant de deux espèces différentes. Cela s’est produit même lorsque les espèces étaient seulement faiblement apparentées, et même lorsque les protéines étaient purifiées et séparées de la plupart de leurs composants auxiliaires habituels. Cependant, une règle est restée ferme : les éléments de phycocyanine ne se mélangeaient qu’avec d’autres phycocyanines, et l’allophycocyanine avec l’allophycocyanine — aucun beignet mixte contenant les deux types n’a été détecté.
Indices atomiques grâce à la prédiction de structure
Pour comprendre pourquoi certains mélanges se forment facilement et d’autres n’apparaissent jamais, les chercheurs se sont tournés vers AlphaFold2, un outil avancé de prédiction de structure protéique. Ils ont modélisé des hexamères purs et hybrides et examiné la concordance des surfaces protéiques prédites. Les complexes hybrides constitués du même type de phycobiliprotéine mais issus d’espèces différentes montraient des interfaces serrées et confiantes, en accord avec les preuves expérimentales que ces assemblages sont stables. En revanche, les hexamères hypothétiques contenant un mélange de phycocyanine et d’allophycocyanine présentaient de moins bons ajustements et moins de contacts, indiquant que de telles combinaisons sont structurellement défavorisées. La comparaison détaillée des positions d’acides aminés aux zones de contact a révélé une poignée de résidus conservés agissant comme des clés de forme, garantissant que seuls les types correspondants s’emboîtent correctement.
Ce que cela signifie pour la vie et la technologie
Les résultats suggèrent que le design central des phycobiliprotéines a été fortement préservé au cours de milliards d’années, permettant à des sous-unités provenant de cyanobactéries éloignées de fonctionner presque de manière interchangeable. Parallèlement, des changements subtils à leurs surfaces de contact empêchent les combinaisons inappropriées entre différents types de phycobiliprotéines, maintenant ainsi un flux d’énergie efficace à travers l’antenne. Cet équilibre entre flexibilité et spécificité a probablement aidé les cyanobactéries à coloniser de nombreux habitats tout en conservant une photosynthèse fiable. Sur le plan pratique, ce travail laisse entendre qu’il pourrait être possible d’ingénier de nouveaux systèmes de capture de lumière — en échangeant des sous-unités compatibles entre espèces — pour ajuster les couleurs de lumière captées, avec des applications potentielles en bioénergie, biotechnologie et matériaux durables.
Citation: Sound, J.K., Bianchini, G., Ashok, T.A. et al. Mass spectrometry reveals the evolutionary conservation of phycobiliprotein complexes. Nat Commun 17, 2834 (2026). https://doi.org/10.1038/s41467-026-69558-y
Mots-clés: cyanobactéries, photosynthèse, capture de la lumière, évolution des protéines, spectrométrie de masse