Clear Sky Science · es
La espectrometría de masas revela la conservación evolutiva de los complejos de ficobiliproteínas
Microbios antiguos con impacto en la actualidad
Las cianobacterias —microbios fotosintéticos minúsculos— ayudaron a transformar la atmósfera primitiva de la Tierra liberando oxígeno y siguen sosteniendo los ciclos globales del carbono y del nitrógeno. Prosperan desde manantiales termales abrasadores hasta lagos helados, pero muchas comparten el mismo tipo de maquinaria para captar la luz. Este estudio plantea una pregunta simple pero profunda: ¿cómo han permanecido tan eficaces estas partes recolectoras de luz durante más de tres mil millones de años, incluso cuando las cianobacterias se han expandido a entornos tan dispares?
Cómo captan la luz estos microbios
Las cianobacterias usan grandes estructuras moleculares «antena», llamadas ficobilisomas, para capturar la luz solar y transferir la energía a los motores fotosintéticos centrales dentro de la célula. Los ficobilisomas están formados por proteínas coloreadas conocidas como ficobiliproteínas, sobre todo ficocianina y aloficocianina, que se ensamblan como donuts apilados. Cada donut está compuesto por pares repetidos de cadenas proteicas que enlazan moléculas pigmentarias. El tamaño y la forma global de la antena pueden variar mucho entre especies, pero los bloques de construcción individuales se parecen sorprendentemente, lo que sugiere un diseño profundamente conservado.
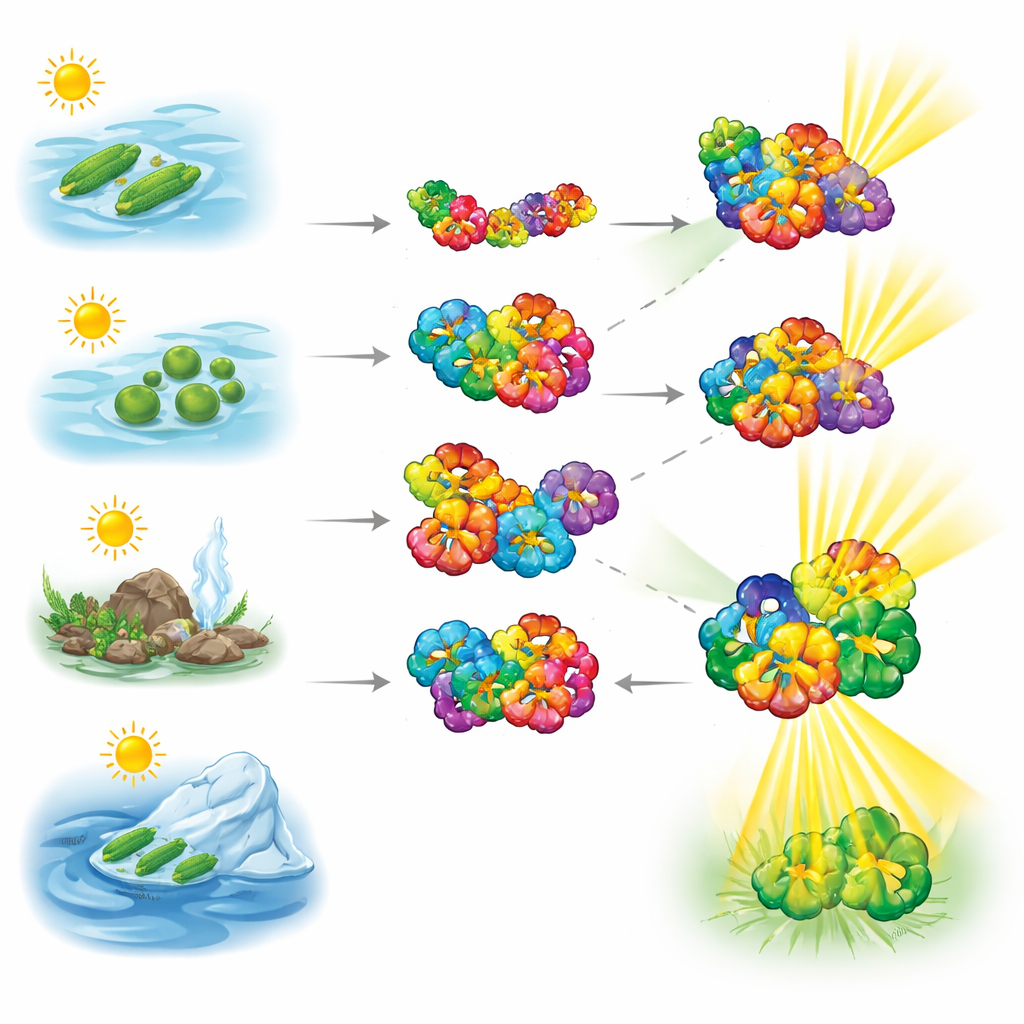
Explorar bloques flexibles con pesadas mediciones de precisión
Para ver cómo se comportan estas proteínas captadoras de luz, los investigadores usaron espectrometría de masas nativa, una técnica que pesa con delicadeza complejos proteicos intactos sin desarmarlos. Examinaron ficobiliproteínas de cianobacterias recogidas en hábitats muy distintos —aguas hipersalinas, agua dulce, ambientes calientes y regiones frías—. Las mediciones mostraron que la ficocianina cambia fácilmente entre pares más pequeños y hexámeros en forma de donut, revelando una naturaleza altamente dinámica. La aloficocianina, en cambio, tendió mucho más a permanecer en su forma hexamérica, lo que sugiere un núcleo más robusto que ancla el sistema de la antena.
Mezclar partes de diferentes especies
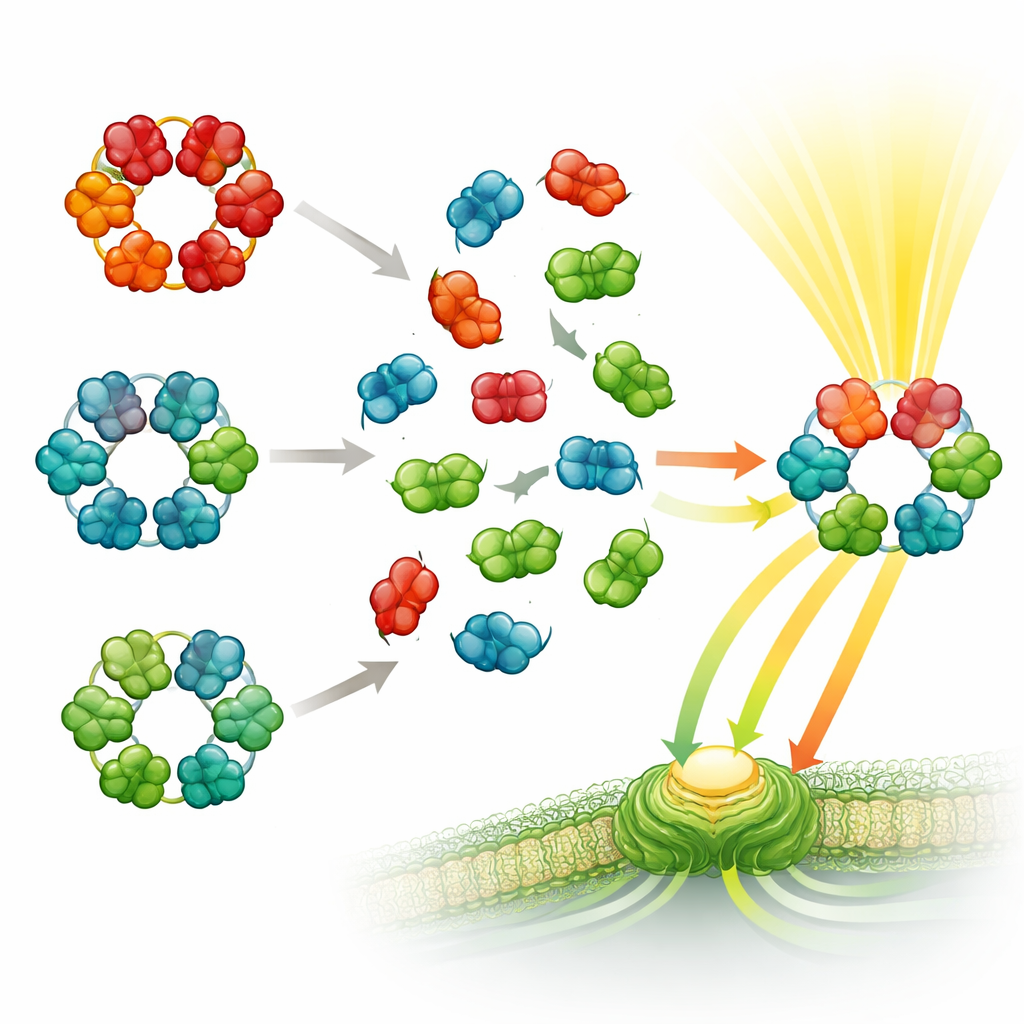
El equipo realizó entonces un experimento molecular de «mezcla y emparejamiento». Combinó ficobiliproteínas purificadas de pares de especies que viven en entornos distintos o pertenecen a ramas lejanas del árbol familiar de las cianobacterias. La espectrometría de masas reveló que las proteínas se ensamblaron rápidamente en complejos híbridos: hexámeros formados por subunidades originarias de dos especies diferentes. Esto ocurrió incluso cuando las especies estaban solo remotamente emparentadas e incluso cuando las proteínas se purificaron lejos de la mayoría de sus componentes auxiliares habituales. Sin embargo, una regla se mantuvo firme: las partes de ficocianina solo se mezclaron con otras ficocianinas, y las de aloficocianina con aloficocianina —no se detectaron donuts mixtos que contuvieran ambos tipos.
Pistas a nivel atómico desde la predicción estructural
Para entender por qué algunas mezclas se forman con facilidad y otras nunca aparecen, los investigadores recurrieron a AlphaFold2, una avanzada herramienta de predicción de estructuras proteicas. Modelaron hexámeros puros e híbridos y examinaron qué tan bien encajaban las superficies proteicas predichas. Los complejos híbridos formados por el mismo tipo de ficobiliproteína pero procedentes de distintas especies mostraron interfaces apretadas y seguras, en concordancia con la evidencia experimental de que estos ensamblajes son estables. En contraste, los hexámeros hipotéticos que contenían una mezcla de ficocianina y aloficocianina mostraron encajes peores y menos contactos, lo que indica que tales combinaciones están estructuralmente desfavorecidas. La comparación detallada de las posiciones de aminoácidos en las zonas de contacto reveló un puñado de residuos conservados que actúan como llaves de forma, asegurando que solo los tipos coincidentes encajen bien entre sí.
Qué significa esto para la vida y la tecnología
Los hallazgos sugieren que el diseño central de las ficobiliproteínas se ha preservado con fuerza durante miles de millones de años, permitiendo que las subunidades de cianobacterias muy dispersas funcionen casi de forma intercambiable. Al mismo tiempo, cambios sutiles en sus superficies de contacto impiden combinaciones desajustadas de distintos tipos de ficobiliproteínas, manteniendo el flujo de energía a través de la antena muy eficiente. Este equilibrio entre flexibilidad y especificidad probablemente ayudó a las cianobacterias a colonizar muchos hábitats mientras mantenían una fotosíntesis fiable. En términos prácticos, el trabajo sugiere que podría ser posible diseñar nuevos sistemas de captura de luz —intercambiando subunidades compatibles de diferentes especies— para ajustar qué colores de luz se capturan, con aplicaciones potenciales en bioenergía, biotecnología y materiales sostenibles.
Cita: Sound, J.K., Bianchini, G., Ashok, T.A. et al. Mass spectrometry reveals the evolutionary conservation of phycobiliprotein complexes. Nat Commun 17, 2834 (2026). https://doi.org/10.1038/s41467-026-69558-y
Palabras clave: cianobacterias, fotosíntesis, captación de luz, evolución de proteínas, espectrometría de masas