Clear Sky Science · de
Massenspektrometrie zeigt die evolutionäre Konservierung phycobiliprotein‑Komplexe
Uralte Mikroben mit heutiger Wirkung
Cyanobakterien — winzige, photosynthetische Mikroben — halfen, die frühe Erdatmosphäre durch Sauerstofffreisetzung zu verändern und bilden noch heute die Grundlage globaler Kohlenstoff‑ und Stickstoffkreisläufe. Sie gedeihen von kochend heißen Quellen bis zu eisigen Seen, und doch besitzen viele dieselbe Art von lichtsammelnder Maschinerie. Diese Studie stellt eine einfache, aber tiefgehende Frage: Wie konnten diese lichtsammelnden Bauteile über mehr als drei Milliarden Jahre so leistungsfähig bleiben, während sich Cyanobakterien in immer unterschiedlichere Lebensräume ausbreiteten?
Wie diese Mikroben Licht einfangen
Cyanobakterien nutzen große molekulare „Antenne“-Strukturen, sogenannte Phycobilisomen, um Sonnenlicht einzufangen und die Energie an die zentralen photosynthetischen Triebwerke in der Zelle weiterzuleiten. Phycobilisomen bestehen aus farbigen Proteinen, den Phycobiliproteinen, vor allem Phycocyanin und Allophycocyanin, die sich wie gestapelte Ringe zusammenlagern. Jeder Ring besteht aus sich wiederholenden Paaren von Proteinketten, die Pigmentmoleküle binden. Größe und Form der Antenne können zwischen den Arten stark variieren, doch die einzelnen Bausteine sehen auffallend ähnlich aus — ein Hinweis auf ein tief konserviertes Design.
Flexible Bausteine mit präzisem Wiegen untersuchen
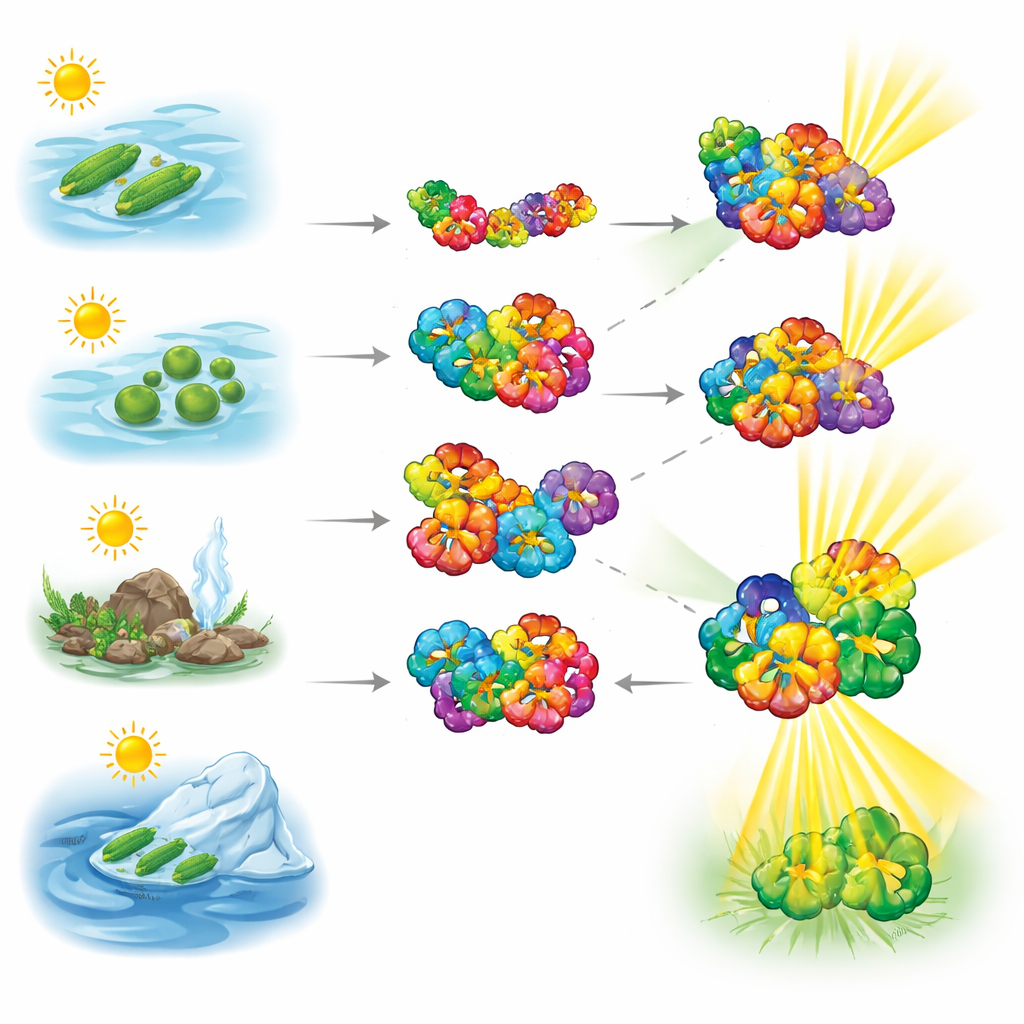
Um zu sehen, wie sich diese lichtsammelnden Proteine verhalten, nutzten die Forscher native Massenspektrometrie, eine Technik, die intakte Proteinkomplexe schonend wiegt, ohne sie zu zerlegen. Sie untersuchten Phycobiliproteine aus Cyanobakterien, die aus sehr unterschiedlichen Habitaten stammen — hypersaline Gewässer, Süßwasser, heiße Umgebungen und kalte Regionen. Die Messungen zeigten, dass Phycocyanin bereitwillig zwischen kleineren Paaren und größeren ringförmigen Hexameren wechselt, was auf eine hochdynamische Natur hinweist. Allophycocyanin dagegen blieb viel häufiger in seiner hexameren Form, was auf einen stabileren Kern schließen lässt, der das Antennensystem verankert.
Teile verschiedener Arten mischen
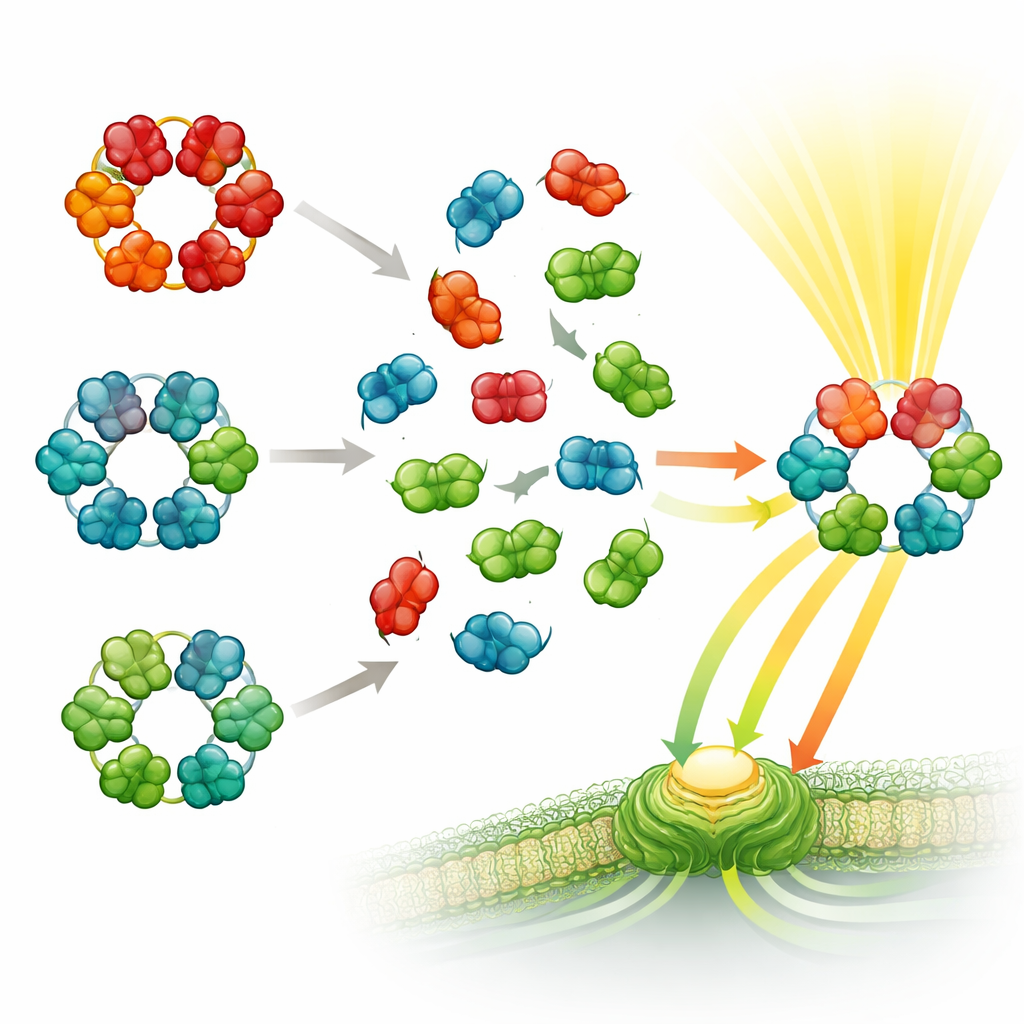
Das Team führte dann ein molekulares „Mix‑und‑Match“-Experiment durch. Sie kombinierten gereinigte Phycobiliproteine aus Paaren von Arten, die in unterschiedlichen Umgebungen leben oder weit auseinander im Stammbaum der Cyanobakterien stehen. Die Massenspektrometrie zeigte, dass sich die Proteine schnell zu hybriden Komplexen zusammenfügten: Hexamere, die aus Untereinheiten zweier verschiedener Arten aufgebaut waren. Das geschah selbst bei weit entfernt verwandten Arten und selbst wenn die Proteine von den meisten ihrer üblichen Helferkomponenten gereinigt waren. Eine Regel blieb jedoch stabil: Phycocyanin‑Teile mischten sich nur mit anderem Phycocyanin, Allophycocyanin nur mit Allophycocyanin — gemischte Ringe mit beiden Typen wurden nicht nachgewiesen.
Atomare Hinweise durch Strukturvorhersage
Um zu verstehen, warum sich einige Mischungen leicht bilden und andere nie auftreten, griffen die Forscher zu AlphaFold2, einem fortgeschrittenen Werkzeug zur Proteinstrukturvorhersage. Sie modellierten sowohl reine als auch hybride Hexamere und untersuchten, wie gut die vorhergesagten Proteinoberflächen zusammenpassen. Hybride Komplexe, die aus demselben Phycobiliprotein‑Typ, aber aus verschiedenen Arten entstanden, zeigten enge, vertrauenswürdige Schnittstellen, was den experimentellen Befunden entspricht, dass diese Assemblies stabil sind. Im Gegensatz dazu zeigten hypothetische Hexamere, die Phycocyanin und Allophycocyanin mischten, schlechtere Passungen und weniger Kontakte, was darauf hindeutet, dass solche Kombinationen strukturell ungünstig sind. Ein detaillierter Vergleich von Aminosäurepositionen an den Kontaktzonen offenbart eine Handvoll konservierter Reste, die wie Form‑Schlüssel wirken und sicherstellen, dass nur passende Typen gut ineinandergreifen.
Was das für Leben und Technik bedeutet
Die Ergebnisse legen nahe, dass das Kerndesign der Phycobiliproteine über Milliarden von Jahren stark erhalten blieb, sodass Untereinheiten entfernter Cyanobakterien nahezu austauschbar funktionieren. Zugleich verhindern subtile Änderungen an ihren Kontaktflächen unpassende Kombinationen unterschiedlicher Phycobiliprotein‑Typen und halten den Energiefluss durch die Antenne hocheffizient. Dieses Gleichgewicht aus Flexibilität und Spezifität half vermutlich den Cyanobakterien, viele Lebensräume zu besiedeln und gleichzeitig eine verlässliche Photosynthese zu bewahren. Praktisch betrachtet deutet die Arbeit darauf hin, dass es möglich sein könnte, neue lichtsammelnde Systeme zu konstruieren — durch Austausch kompatibler Untereinheiten verschiedener Arten — um gezielt einzustellen, welche Lichtfarben erfasst werden, mit potenziellen Anwendungen in Bioenergie, Biotechnologie und nachhaltigen Materialien.
Zitation: Sound, J.K., Bianchini, G., Ashok, T.A. et al. Mass spectrometry reveals the evolutionary conservation of phycobiliprotein complexes. Nat Commun 17, 2834 (2026). https://doi.org/10.1038/s41467-026-69558-y
Schlüsselwörter: Cyanobakterien, Photosynthese, Lichtsammlung, Proteinevolution, Massenspektrometrie