Clear Sky Science · pt
Direcionando o metabolismo mitocondrial do glioblastoma com S-Gboxin induz citotoxicidade nas condições do microambiente tumoral
Por que deixar tumores cerebrais com fome pode ser sua fraqueza
O glioblastoma é um dos cânceres cerebrais mais letais, em parte porque suas células são extraordinariamente boas em sobreviver em condições adversas, onde oxigênio e nutrientes são escassos. Este estudo explora um fármaco chamado S-Gboxin, projetado para atingir as “usinas de energia” dentro das células de glioblastoma, e faz uma pergunta simples, porém importante: esse medicamento continua funcionando nas duras condições de fome encontradas em tumores reais — e seu efeito pode ser fortalecido ao combiná-lo com outros tratamentos?
Um fármaco que ataca as usinas de energia celular
Cada célula depende de estruturas diminutas chamadas mitocôndrias para converter alimento e oxigênio em energia utilizável. S-Gboxin é uma versão refinada de um composto anterior, Gboxin, que foi encontrado bloqueando uma etapa chave da produção de energia em células de glioblastoma de forma mais intensa do que em células normais. Em placas com linhagens de células humanas de glioblastoma e células tumorais derivadas de pacientes, os pesquisadores mostram que doses baixas na faixa micromolar de S-Gboxin retardam o crescimento e desencadeiam a morte celular. Células de suporte cerebral imortalizadas (astrócitos geneticamente alterados para se dividirem indefinidamente) também respondem ao fármaco, mas astrócitos humanos normais não transformados são muito menos afetados em doses comparáveis, sugerindo que S-Gboxin prejudica preferencialmente células com características tumorais.
Condições tumorais adversas tornam o fármaco mais eficiente
Tumores reais de glioblastoma frequentemente recebem suprimento sanguíneo insuficiente, levando a baixos níveis de glicose e oxigênio — condições que às vezes atenuam o efeito de terapias direcionadas. A equipe recriou esse ambiente hostil limitando glicose e oxigênio em cultura celular. Sob essas condições de estresse, S-Gboxin tornou-se de fato mais tóxico para células de glioblastoma: doses mais baixas foram suficientes para induzir morte celular, especialmente quando tanto glicose quanto oxigênio estavam escassos. Quando as células foram forçadas a depender mais de combustíveis mitocondriais — alimentando-as com galactose em vez de glicose prontamente queimada — o efeito letal do fármaco aumentou dramaticamente. Em contraste, astrócitos primários normais permaneceram comparativamente resistentes, mesmo em condições de baixa glicose.
Reconfigurando o uso de energia e reduzindo o movimento das células cancerosas
Para entender como S-Gboxin altera o metabolismo das células tumorais, os pesquisadores mediram o consumo de oxigênio e a produção de ácido. Surpreendentemente, em vez de agir puramente como um inibidor clássico da produção de energia, S-Gboxin fez as mitocôndrias se comportarem como motores com vazamento: os padrões de consumo de oxigênio assemelharam-se aos observados quando as mitocôndrias são “desacopladas”, de modo que o combustível é consumido sem produzir energia de forma eficiente. As células responderam aumentando a glicólise — a via mais rápida e menos eficiente de gerar energia a partir da glicose — levando a maior liberação de lactato e consumo mais rápido de glicose. Ao mesmo tempo, comportamentos que demandam muita energia, como migração celular, foram reduzidos, consistente com uma crise interna de energia que deixa as células tumorais menos capazes de se mover e potencialmente se espalhar.
Sinalização de estresse ajuda pouco, mas a detecção de energia importa muito
As células cancerosas possuem programas de emergência incorporados para lidar com estresse. Um desses programas, a resposta integrada ao estresse, centra-se em uma proteína chamada ATF4, que ajuda as células a se adaptarem à falta de nutrientes e oxigênio. S-Gboxin claramente ativou essa resposta, mas bloquear ATF4 com um inibidor de pequena molécula ou reduzir sua expressão geneticamente não tornou o fármaco visivelmente mais letal, indicando que essa via de estresse não protege fortemente as células de glioblastoma contra S-Gboxin. Uma salvaguarda diferente, entretanto, provou ser crucial: AMPK, um sensor mestre de energia que ajuda as células a restaurar o equilíbrio quando os níveis de ATP caem. Quando a AMPK foi removida geneticamente ou bloqueada farmacologicamente, as células de glioblastoma tornaram-se muito mais sensíveis ao S-Gboxin, especialmente em condições de baixa glicose. Nessas circunstâncias, até doses modestas do fármaco desencadearam morte celular pronunciada, enquanto astrócitos normais foram em grande parte poupados pela combinação.
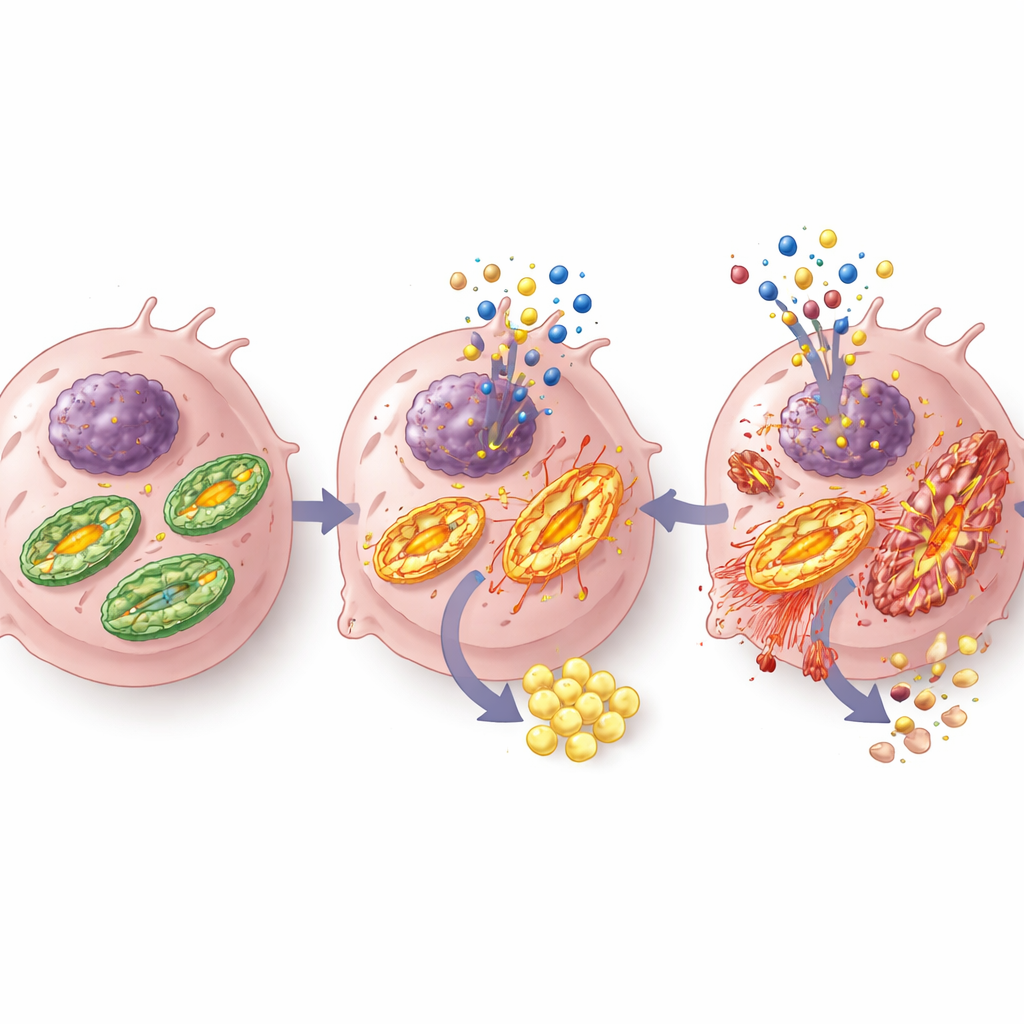
Transformando a fome do tumor em vantagem terapêutica
No geral, os achados sugerem que S-Gboxin transforma a dependência do glioblastoma por produção energética flexível em uma vulnerabilidade. Ao interromper a função mitocondrial e forçar um uso desperdiçador de glicose, o fármaco é particularmente eficaz nas condições muito pobres em nutrientes e com baixo oxigênio que definem o ambiente interno do tumor. Bloquear a via sensores de energia AMPK despoja as células tumorais de uma ferramenta chave de sobrevivência, inclinando ainda mais a balança para a morte celular sem causar dano significativo às células cerebrais normais nesses experimentos. Embora muito trabalho permaneça — especialmente para otimizar a entrega aos tumores no cérebro humano — este estudo aponta para uma estratégia em que fármacos projetados para atingir o metabolismo, combinados com inibidores de vias de detecção de energia, poderiam um dia ajudar a “matar de fome” o glioblastoma de dentro para fora.
Citação: Weinem, JB., Urban, H., Sauer, B. et al. Targeting glioblastoma mitochondrial metabolism with S-Gboxin induces cytotoxicity under conditions of the tumor microenvironment. Cell Death Discov. 12, 181 (2026). https://doi.org/10.1038/s41420-026-03072-4
Palavras-chave: glioblastoma, metabolismo do câncer, mitocôndrias, S-Gboxin, inibição de AMPK