Clear Sky Science · nl
Richting glioblastoom-mitochondriële stofwisseling met S-Gboxin veroorzaakt cytotoxiciteit onder omstandigheden van het tumormicro-omgeving
Waarom het uithongeren van hersentumoren hun zwakke plek kan zijn
Glioblastoom is een van de dodelijkste hersenkankers, deels omdat de cellen opmerkelijk goed kunnen overleven onder harde omstandigheden waarin zuurstof en voedingsstoffen schaars zijn. Deze studie onderzoekt een geneesmiddel genaamd S-Gboxin, ontworpen om de "energiecentrales" binnen glioblastoomcellen aan te pakken, en stelt een eenvoudige maar belangrijke vraag: werkt dit middel nog steeds onder de moeilijke, uitgehongerde omstandigheden die in echte tumoren voorkomen — en kan het effect worden versterkt door het te combineren met andere behandelingen?
Een geneesmiddel dat de cellulaire energiecentrales bekijkt
Elke cel is afhankelijk van kleine structuren, mitochondriën, om voedsel en zuurstof om te zetten in bruikbare energie. S-Gboxin is een verfijnde versie van een eerder verbinding, Gboxin, waarvan werd vastgesteld dat het een cruciale energieproducerende stap in glioblastoomcellen sterker blokkeert dan in normale cellen. In kweekschalen met humane glioblastoom-celijnen en tumorcellen afkomstig van patiënten tonen de onderzoekers aan dat lage micromolaire doses S-Gboxin de groei vertragen en celdood induceren. Immortaliseerde ondersteunende hersencellen (astrocyten die genetisch veranderd zijn om oneindig te delen) reageren ook op het middel, maar normale, niet-getransformeerde humane astrocyten worden bij vergelijkbare doses veel minder beïnvloed, wat suggereert dat S-Gboxin bij voorkeur tumorachtige cellen schaadt.
Harde tumoromstandigheden maken het middel effectiever
Echte glioblastoomtumoren worden vaak slecht doorbloed, wat leidt tot lage glucose- en zuurstofniveaus — omstandigheden die het effect van gerichte therapieën soms kunnen verzwakken. Het team reconstrueerde deze vijandige omgeving door glucose en zuurstof in celkweek te beperken. Onder deze stressvolle omstandigheden werd S-Gboxin feitelijk toxischer voor glioblastoomcellen: lagere doses waren voldoende om hen naar celdood te duwen, vooral wanneer zowel glucose als zuurstof schaars waren. Toen cellen gedwongen werden meer op mitochondriale brandstoffen te vertrouwen — door ze galactose te voeden in plaats van gemakkelijk verbrandbare glucose — nam het dodelijke effect van het middel dramatisch toe. Daarentegen bleven normale primaire astrocyten relatief resistent, zelfs onder lage-glucosecondities.
Hertrekken van energiegebruik en vertraging van kankercelmigratie
Om te begrijpen hoe S-Gboxin het metabolisme van tumorcellen verandert, maten de onderzoekers zuurstofgebruik en zuurgraadproductie. Verrassend genoeg gedroeg S-Gboxin de mitochondriën niet louter als een klassieke energieblokker: de mitochondriën wezen eerder op een lekende motor — het zuurstofverbruik leek op dat bij mitochondriën die “ontkoppeld” zijn, zodat brandstof wordt verbrand zonder efficiënt energie te maken. Cellen reageerden door glycolyse op te voeren — de snellere, minder efficiënte manier om energie uit glucose te halen — wat leidde tot hogere lactaatafgifte en snellere glucoseconsumptie. Tegelijkertijd werden energie-intensieve processen zoals celmigratie verminderd, wat consistent is met een interne energiecrisis waardoor tumorcellen minder in staat zijn te bewegen en mogelijk uit te zaaien.
Stresssignalering helpt weinig, maar energiewaarneming doet er veel toe
Kankercellen beschikken over ingebouwde noodprogramma’s om met stress om te gaan. Een van die programma’s, de geïntegreerde stressrespons, draait om een eiwit genaamd ATF4, dat cellen helpt zich aan te passen aan tekorten aan voedingsstoffen en zuurstof. S-Gboxin schakelde deze respons duidelijk aan, maar het blokkeren van ATF4 met een klein-moleculair remmer of genetische knockdown maakte het middel niet merkbaar dodelijker, wat aangeeft dat deze stressroute glioblastoomcellen niet sterk beschermt tegen S-Gboxin. Een andere beveiliging bleek echter cruciaal: AMPK, een hoofdregelaar van energiewaarneming die cellen helpt het evenwicht te herstellen wanneer ATP-niveaus dalen. Wanneer AMPK genetisch werd verwijderd of farmacologisch werd geblokkeerd, werden glioblastoomcellen veel gevoeliger voor S-Gboxin, vooral onder lage-glucosecondities. Onder deze omstandigheden veroorzaakten zelfs bescheiden doses van het middel uitgesproken celdood, terwijl normale astrocyten grotendeels onaangetast bleven door de combinatie.
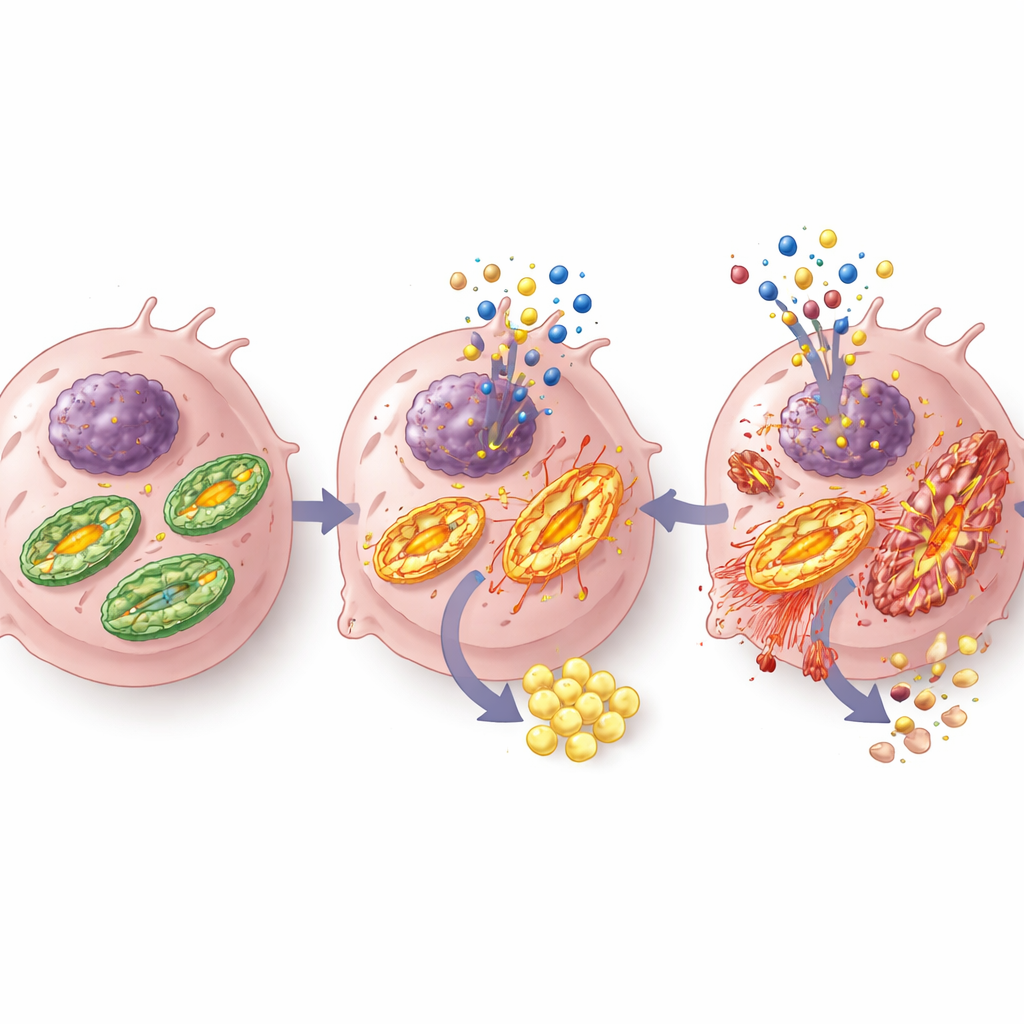
De honger van een tumor omzetten in een behandelvoordeel
Al met al suggereren de bevindingen dat S-Gboxin de afhankelijkheid van glioblastoom van flexibele energieproductie in een kwetsbaarheid verandert. Door de mitochondriale functie te verstoren en een verspilde overconsumptie van glucose af te dwingen, is het middel bijzonder effectief onder de zeer voedselarme, zuurstofarme omstandigheden die het innerlijke milieu van de tumor kenmerken. Het blokkeren van het AMPK-energiewaarschuwingssysteem berooft tumorcellen van een belangrijk overlevingstool, waarmee de balans verder naar celdood wordt gekanteld zonder in deze experimenten grote schade toe te brengen aan normale hersencellen. Terwijl er nog veel werk te doen is — vooral om de levering aan tumoren in het menselijke brein te optimaliseren — wijst deze studie op een strategie waarin zorgvuldig ontworpen, op het metabolisme gerichte middelen, gecombineerd met remmers van energiewaarnemingsroutes, op een dag kunnen helpen glioblastoom van binnenuit uit te hongeren.
Bronvermelding: Weinem, JB., Urban, H., Sauer, B. et al. Targeting glioblastoma mitochondrial metabolism with S-Gboxin induces cytotoxicity under conditions of the tumor microenvironment. Cell Death Discov. 12, 181 (2026). https://doi.org/10.1038/s41420-026-03072-4
Trefwoorden: glioblastoom, kankermetabolisme, mitochondriën, S-Gboxin, AMPK-remming