Clear Sky Science · he
כוונון מטבוליזם המיטוכונדריה של גליובלסטומה עם S-Gboxin גורם לציטוטוקסיות בתנאי מיקרו-סביבת הגידול
מדוע רעב יכול להיות נקודת התורפה של גידולי המוח
גליובלסטומה היא אחד מסוגי הסרטן הקטלניים במוח, בין השאר משום שהתאים שלה מצטיינים ביכולת לשרוד בתנאים קשים שבהם חמצן ומזון נדירים. מחקר זה בוחן תרופה בשם S-Gboxin, שתוכננה לפגוע ב"תחנות הכוח" שבתאי הגליובלסטומה, ושואל שאלה פשוטה אך חשובה: האם התרופה הזו עדיין עובדת בתנאי הרעב והקיצון שמתקיימים בתוך גידולים אמיתיים — והאם אפשר להגביר את השפעתה על ידי שילובה עם טיפולים אחרים?
תרופה שיורה על תחנות הכוח התאית
כל תא תלוי במבנים זעירים הנקראים מיטוכונדריות כדי להפוך מזון וחמצן לאנרגיה בת-שימוש. S-Gboxin היא גרסה משופרת של תרכובת מוקדמת, Gboxin, שנמצאה כחוסמת צעד חשוב ביצירת אנרגיה בתאי גליובלסטומה יותר מאשר בתאים נורמליים. בכלי תרבית של קווים תאיים אנושיים ושל תאים שמקורם בגידולים של מטופלים הציגו החוקרים כי מנות נמוכות בתחום המיקרומולרי של S-Gboxin מאטות גדילה ומפעילות מוות תאי. תאי תמיכה מוחיים הומרליים (אסטרוציטים שעברו שינוי גנטי כדי להתחלק ללא הגבלה) גם הגיבו לתרופה, אך אסטרוציטים אנושיים ראשוניים שאינם עברו טרנספורמציה הושפעו במידה פחותה בהרבה במינונים דומים, דבר המציע כי S-Gboxin פוגע בהעדפה בתאים דמויי-גידול.
תנאי גידול קשים מחזקים את השפעת התרופה
גידולי גליובלסטומה אמיתיים לעיתים קרובות מסופקים בצורה לקויה בדם, מה שמוביל לרמות נמוכות של גלוקוז וחמצן — תנאים שיכולים לעתים להחליש את השפעת הטיפולים הממוקדים. הצוות שיחזר את הסביבה העוינת הזו על ידי הגבלת גלוקוז וחמצן בתרבית התאים. בתנאי הלחץ הללו S-Gboxin הפך למעשה לרעיל יותר לתאי גליובלסטומה: מינונים נמוכים הספיקו לדחוף אותם למוות תאי, במיוחד כאשר גם הגלוקוז וגם החמצן היו במחסור. כאשר אילצו את התאים להסתמך יותר על דלקים מיטוכונדריאליים — על ידי האכלה בגלקטוז במקום גלוקוז שקל יותר לשריפה — אפקט ההרג של התרופה גדל באופן דרמטי. לעומת זאת, אסטרוציטים ראשוניים נורמליים נותרו עמידים יחסית, אפילו בתנאי גלוקוז נמוך.
הפניית שימוש האנרגיה והאטת תנועת תאי הסרטן
כדי להבין כיצד S-Gboxin משנה את מטבוליזם תאי הגידול, מדדו החוקרים שימוש בחמצן וייצור חומציות. באופן מפתיע, במקום לפעול בתור מדכא אנרגיה קלאסי, S-Gboxin הפך את המיטוכונדריות למנועים דולפים: דפוסי צריכת החמצן נראו דומים לאלו הנצפים כשהמיטוכונדריות "מובררות" (uncoupled), כך שהדלק נשרף ללא יצירת אנרגיה ביעילות. התאים הגיבו בהגברת הגליקוליזה — הדרך המהירה אך הפחות יעילה לייצור אנרגיה מגלוקוז — מה שהוביל לשחרור חומצת חלב גבוה יותר ולצריכת גלוקוז מהירה יותר. בו־זמנית, התנהגויות תלויות-אנרגיה כגון נדידה תאית פחתו, תואם למשבר אנרגטי פנימי שמשאיר את תאי הגידול פחות מסוגלים לנוע ובכך לצמצם את הפוטנציאל להתפשטות.
אותות לחץ עוזרים מעט, אך חיישן האנרגיה משנה רבות
לתאי סרטן יש תוכניות חירום מובנות להתמודדות עם לחץ. אחת התכניות האלו, תגובת הלחץ המשולבת, מתמקדת בחלבון בשם ATF4, שעוזר לתאים להסתגל למחסור במזון ובחמצן. S-Gboxin הדליק בבירור תגובה זו, אך חסימת ATF4 בעזרת מעכב מולקולרי קטן או באמצעות דיכוי גנטי לא הפכה את התרופה להרבה יותר קטלנית, מה שמצביע על כך שדרך לחץ זו אינה מגינה באופן משמעותי על תאי גליובלסטומה מפני S-Gboxin. שמירה אחרת, לעומת זאת, התגלתה כקריטית: AMPK, חיישן אנרגיה מרכזי שעוזר לתאים להשיב איזון כאשר רמות ATP יורדות. כאשר הוסר AMPK באופן גנטי או נחסם פרמקולוגית, תאי גליובלסטומה הפכו לרגישים הרבה יותר ל-S-Gboxin, במיוחד בתנאי גלוקוז נמוך. במצבים אלה, אפילו מינונים צנועים של התרופה גרמו למוות תאי ניכר, בעוד שאסטרוציטים נורמליים הושפעו במידה מועטה מהשילוב.
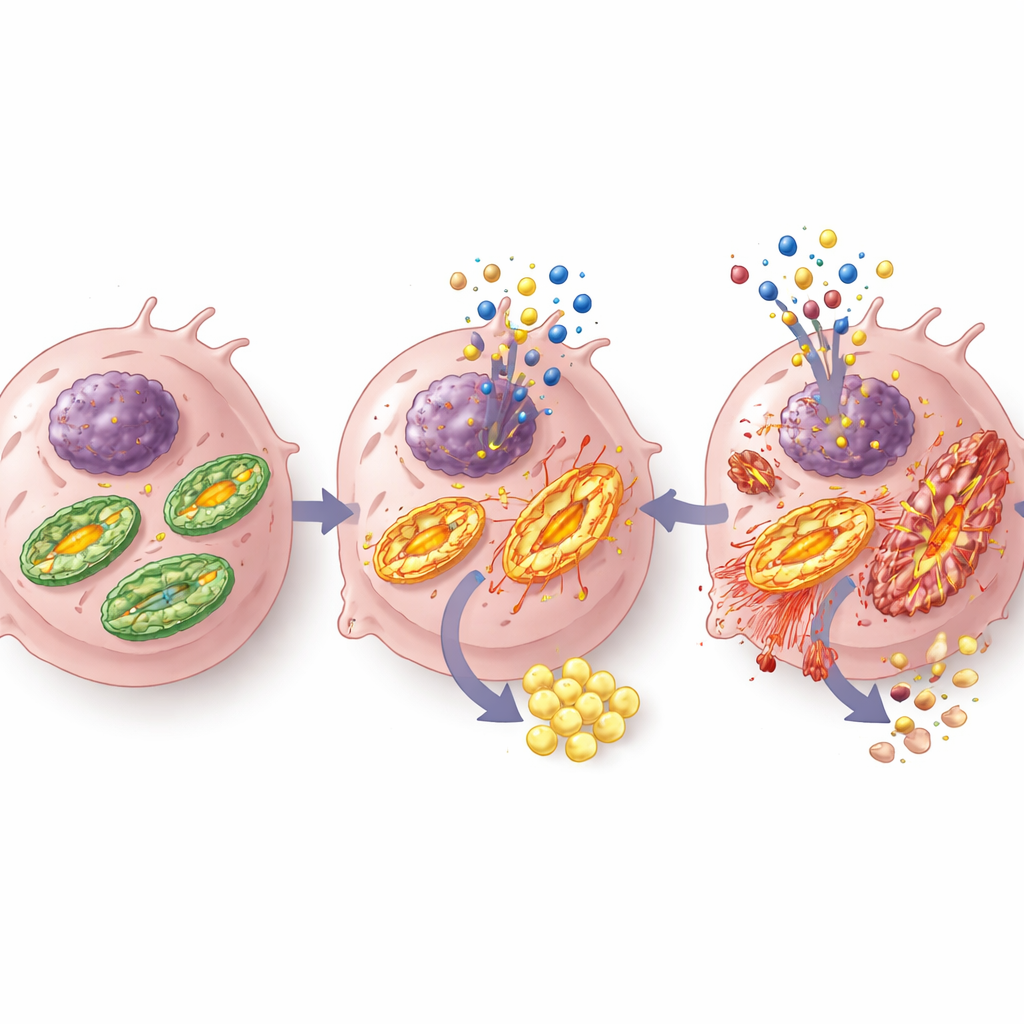
להפוך את רעב הגידול ליתרון טיפולי
בסך הכל, הממצאים מציעים כי S-Gboxin הופך את התלות של גליובלסטומה בייצור אנרגיה גמיש לחיסרון. על ידי הפרעת תפקוד מיטוכונדריאלי וכפייה על שימוש בזבזני בגלוקוז, התרופה יעילה במיוחד בתנאי העוני התזונתי וחוסר החמצן שמגדירים את סביבתו הפנימית של הגידול. חסימת מסלול חישת האנרגיה AMPK מפשטת את כלי ההישרדות של תאי הגידול, מה שמטה עוד את היתרות לעבר מוות תאי מבלי לגרום לנזק משמעותי לתאי מוח נורמליים בניסויים אלה. למרות שעוד נדרשת עבודה רבה — במיוחד כדי למקסם אספקה לגידולים במוח האנושי — מחקר זה מצביע על אסטרטגיה שבה תרופות המכוונות מטבוליזם, משולבות עם מעכבים של מסלולים לחישת אנרגיה, עשויות יום אחד לעזור "לרעב" את הגליובלסטומה מבפנים.
ציטוט: Weinem, JB., Urban, H., Sauer, B. et al. Targeting glioblastoma mitochondrial metabolism with S-Gboxin induces cytotoxicity under conditions of the tumor microenvironment. Cell Death Discov. 12, 181 (2026). https://doi.org/10.1038/s41420-026-03072-4
מילות מפתח: גליובלסטומה, מטבוליזם של סרטן, מיטוכונדריה, S-Gboxin, עיכוב AMPK