Clear Sky Science · pl
Celowanie w mitochondrialny metabolizm glejaka za pomocą S-Gboxin wywołuje cytotoksyczność w warunkach mikrośrodowiska guza
Dlaczego głodzenie guzów mózgu może być ich słabością
Glejak to jeden z najbardziej śmiertelnych nowotworów mózgu, częściowo dlatego, że jego komórki wykazują wyjątkową zdolność do przetrwania w trudnych warunkach, gdzie brakuje tlenu i składników odżywczych. W tym badaniu analizowano lek o nazwie S-Gboxin, zaprojektowany tak, by uderzać w „elektrownie” komórek glejaka, i zadano proste, ale istotne pytanie: czy ten preparat działa również w surowych, pozbawionych składników warunkach panujących wewnątrz rzeczywistych guzów — i czy jego skuteczność można wzmocnić, łącząc go z innymi terapiami?
Lek atakujący komórkowe elektrownie
Każda komórka polega na drobnych strukturach zwanych mitochondriami, które przekształcają pokarm i tlen w użyteczną energię. S-Gboxin to udoskonalona wersja wcześniejszego związku, Gboxin, który stwierdzono, że hamuje kluczowy krok wytwarzania energii w komórkach glejaka silniej niż w komórkach normalnych. W hodowlach linii komórkowych ludzkiego glejaka i komórek pochodzących od pacjentów badacze wykazali, że niskie stężenia w zakresie mikromolarnym spowalniają wzrost i wywołują śmierć komórek. Zespołom astrocytów unieśmiertelnionych (komórki wsparcia mózgu zmodyfikowane genetycznie, by dzieliły się nieograniczenie) również reagowały na lek, ale normalne, niezmienione ludzkie astrocyty były przy porównywalnych dawkach znacznie mniej dotknięte, co sugeruje, że S-Gboxin preferencynie szkodzi komórkom przypominającym nowotwór.
Surowe warunki guza potęgują działanie leku
Prawdziwe guzy glejaka często są słabo ukrwione, co prowadzi do niskiego poziomu glukozy i tlenu — warunków, które czasem osłabiają efekty terapii celowanych. Zespół odtworzył to wrogie środowisko, ograniczając glukozę i tlen w hodowli komórkowej. W tych stresowych warunkach S-Gboxin stał się w rzeczywistości bardziej toksyczny dla komórek glejaka: niższe dawki wystarczały, by doprowadzić je do śmierci, zwłaszcza gdy zarówno glukoza, jak i tlen były ograniczone. Gdy komórki zmuszono do silniejszego polegania na paliwach mitochondrialnych — podając im galaktozę zamiast łatwo spalanej glukozy — efekt zabijający leku zwiększył się dramatycznie. W przeciwieństwie do tego, normalne astrocyty pierwotne pozostały stosunkowo odporne, nawet przy niskim poziomie glukozy.
Przeprogramowanie wykorzystania energii i spowolnienie ruchliwości komórek nowotworowych
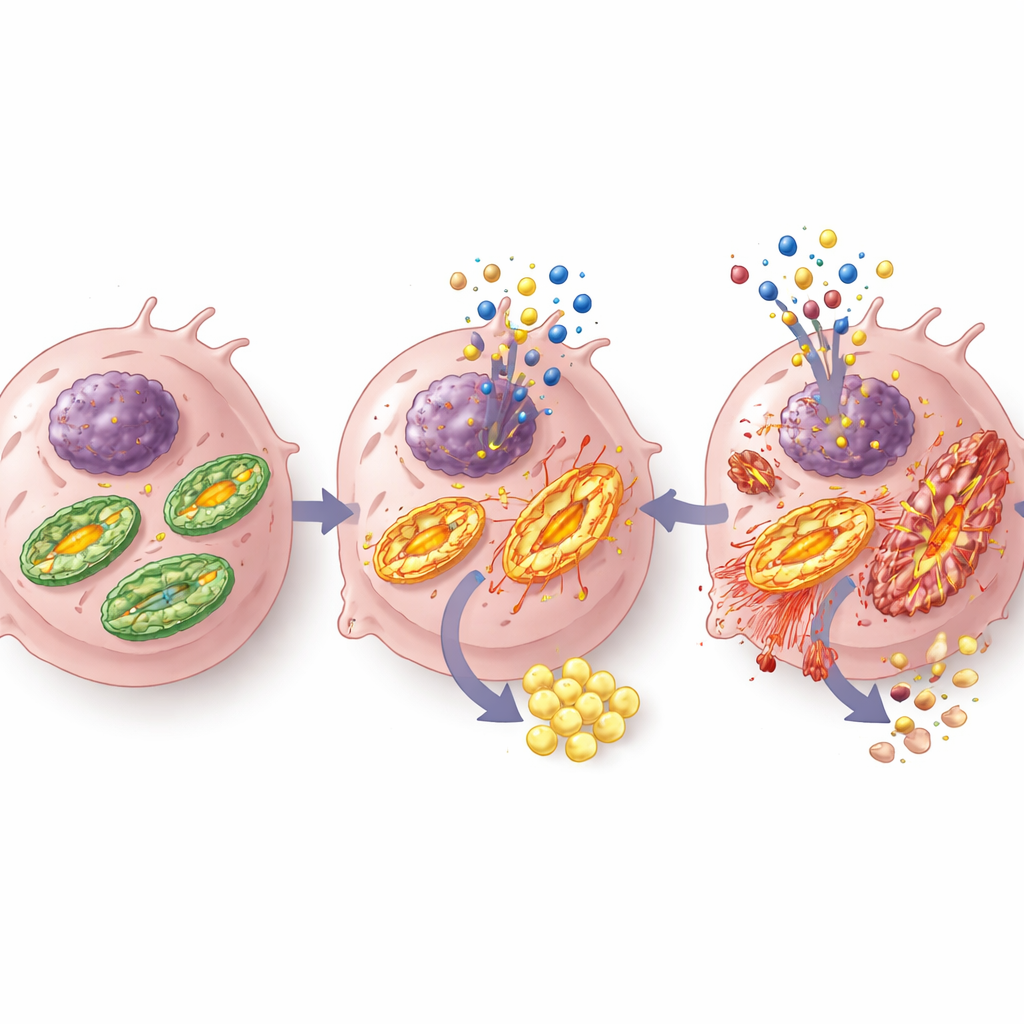
Aby zrozumieć, jak S-Gboxin zmienia metabolizm komórek nowotworowych, badacze mierzyli zużycie tlenu i produkcję kwasów. Ku zaskoczeniu, zamiast zachowywać się wyłącznie jak klasyczny inhibitor blokujący produkcję energii, S-Gboxin sprawiał, że mitochondria zachowywały się jak nieszczelne silniki: wzorce konsumpcji tlenu przypominały te obserwowane przy „rozprzęgnięciu” mitochondriów, tak że paliwo było spalane bez efektywnej produkcji energii. Komórki odpowiedziały zwiększeniem glikolizy — szybszej, mniej wydajnej drogi wytwarzania energii z glukozy — co prowadziło do większego uwalniania mleczanu i szybszego zużycia glukozy. Jednocześnie zachowania wymagające dużo energii, takie jak migracja komórek, były zmniejszone, co jest zgodne z wewnętrznym kryzysem energetycznym, który pozostawia komórki nowotworowe mniej zdolne do przemieszczania się i potencjalnego szerzenia.
Sygnały stresowe niewiele pomagają, ale czujnik energii ma duże znaczenie
Komórki nowotworowe dysponują wbudowanymi programami awaryjnymi radzenia sobie ze stresem. Jednym z takich programów jest zintegrowana odpowiedź na stres, w centrum której znajduje się białko ATF4, pomagające komórkom przystosować się do niedoborów składników odżywczych i tlenu. S-Gboxin wyraźnie włączał tę odpowiedź, ale blokowanie ATF4 małą cząsteczką lub przez wyciszenie genetyczne nie uczyniło leku wyraźnie bardziej śmiertelnym, co wskazuje, że ta ścieżka stresowa nie chroni silnie komórek glejaka przed S-Gboxin. Inne zabezpieczenie okazało się jednak kluczowe: AMPK, główny czujnik energetyczny, który pomaga komórkom przywrócić równowagę, gdy poziomy ATP spadają. Gdy AMPK zostało genetycznie usunięte lub farmakologicznie zablokowane, komórki glejaka stały się znacznie bardziej wrażliwe na S-Gboxin, szczególnie w warunkach niskiej glukozy. W takich okolicznościach nawet umiarkowane dawki leku wywoływały wyraźną śmierć komórek, podczas gdy normalne astrocyty w dużej mierze pozostawały nieuszkodzone przez to połączenie.
Przekształcenie głodu guza w przewagę terapeutyczną
Podsumowując, wyniki sugerują, że S-Gboxin zamienia zależność glejaka od elastycznych sposobów pozyskiwania energii w wadę. Poprzez zakłócenie funkcji mitochondriów i wymuszenie marnotrawnego nadmiernego wykorzystania glukozy, lek jest szczególnie skuteczny w bardzo ubogich w składniki i tlen warunkach definiujących wewnętrzne środowisko guza. Zablokowanie ścieżki czujnika energii AMPK pozbawia komórki nowotworowe kluczowego narzędzia przetrwania, jeszcze bardziej przechylając balans w stronę śmierci komórek bez istotnego zwiększenia szkód dla normalnych komórek mózgu w tych eksperymentach. Choć przed nami jeszcze wiele pracy — zwłaszcza by zoptymalizować dostarczanie do guzów w ludzkim mózgu — badanie to wskazuje strategię, w której starannie zaprojektowane leki celujące w metabolizm, w połączeniu z inhibitorami ścieżek czujników energii, mogłyby pewnego dnia pomóc „zagłodzić” glejaka od wewnątrz.
Cytowanie: Weinem, JB., Urban, H., Sauer, B. et al. Targeting glioblastoma mitochondrial metabolism with S-Gboxin induces cytotoxicity under conditions of the tumor microenvironment. Cell Death Discov. 12, 181 (2026). https://doi.org/10.1038/s41420-026-03072-4
Słowa kluczowe: glejak, metabolizm nowotworowy, mitochondria, S-Gboxin, hamowanie AMPK