Clear Sky Science · de
Gezielte Störung des mitochondrialen Stoffwechsels von Glioblastomen mit S-Gboxin löst unter Tumormikroumgebungsbedingungen Zytotoxizität aus
Warum das Ausdursten von Hirntumoren ihre Schwachstelle sein könnte
Glioblastom gehört zu den tödlichsten Hirntumoren, teilweise weil seine Zellen außergewöhnlich gut darin sind, unter harten Bedingungen mit wenig Sauerstoff und Nährstoffen zu überleben. In dieser Studie wird ein Wirkstoff namens S-Gboxin untersucht, der darauf abzielt, die „Kraftwerke“ in Glioblastomzellen zu treffen. Die zentrale Frage lautet: Wirkt dieses Mittel auch unter den rauen, ausgehungerten Bedingungen, wie sie in realen Tumoren herrschen — und lässt sich seine Wirkung durch Kombination mit anderen Behandlungen verstärken?
Ein Wirkstoff, der die zellulären Kraftwerke angreift
Jede Zelle ist auf winzige Strukturen angewiesen, die Mitochondrien, die Nahrung und Sauerstoff in nutzbare Energie verwandeln. S-Gboxin ist eine verfeinerte Version einer früheren Verbindung, Gboxin, die einen wichtigen Energieschritt in Glioblastomzellen stärker blockierte als in normalen Zellen. In Kulturen menschlicher Glioblastomzelllinien und patientenabgeleiteter Tumorzellen zeigen die Forschenden, dass niedrige Mikromolaren-Dosen von S-Gboxin das Wachstum verlangsamen und Zelltod auslösen. Immortalisierte Stützzellen des Gehirns (astrozytenartige Zellen, die genetisch verändert wurden, um sich unendlich zu teilen) reagieren ebenfalls auf das Medikament, während normale, nicht transformierte menschliche Astrozyten bei vergleichbaren Dosen deutlich weniger betroffen sind, was darauf hindeutet, dass S-Gboxin Tumor-ähnliche Zellen bevorzugt schädigt.
Rauhe Tumorbedingungen verstärken die Wirkung des Wirkstoffs
Reale Glioblastome sind oft schlecht durchblutet, was zu niedrigem Glukosespiegel und Sauerstoffmangel führt — Bedingungen, die gezielte Therapien abschwächen können. Das Team rekonstruierte diese feindliche Umgebung durch Begrenzung von Glukose und Sauerstoff in Zellkulturen. Unter diesen Stressbedingungen wurde S-Gboxin für Glioblastomzellen tatsächlich toxischer: Schon niedrigere Dosen reichten aus, um Zelltod zu induzieren, vor allem wenn sowohl Glukose als auch Sauerstoff knapp waren. Wenn die Zellen gezwungen wurden, stärker auf mitochondriale Brennstoffe zu setzen — indem man ihnen Galaktose statt leicht verbrennbarer Glukose gab — nahm die abtötende Wirkung des Wirkstoffs deutlich zu. Im Gegensatz dazu blieben normale primäre Astrozyten vergleichsweise resistent, selbst unter niedrigem Glukosespiegel.
Umschaltung des Energiestoffwechsels und verlangsamte Tumorzellbewegung
Um zu verstehen, wie S-Gboxin den Stoffwechsel der Tumorzellen verändert, maßen die Forschenden Sauerstoffverbrauch und Säureproduktion. Überraschenderweise verhielt sich S-Gboxin nicht rein wie ein klassischer Energiesperrer, sondern ließ die Mitochondrien wie undichte Motoren erscheinen: Die Muster des Sauerstoffverbrauchs erinnerten an eine „Entkopplung“, bei der Brennstoff verbrannt wird, ohne effizient Energie zu erzeugen. Die Zellen reagierten mit einer Hochregulierung der Glykolyse — der schnelleren, aber weniger effizienten Art, Energie aus Glukose zu gewinnen — was zu höherer Laktatfreisetzung und schnellerem Glukoseverbrauch führte. Gleichzeitig wurden energieintensive Verhaltensweisen wie Zellmigration reduziert, was zu einem inneren Energiemangel passt, der Tumorzellen weniger beweglich und damit womöglich weniger verbreitungsfähig macht.
Stresssignale helfen wenig, Energiesensoren sind entscheidend
Krebszellen verfügen über eingebaute Notfallprogramme zur Bewältigung von Stress. Eines dieser Programme, die integrierte Stressantwort, dreht sich um ein Protein namens ATF4, das Zellen hilft, sich an Nährstoff- und Sauerstoffmangel anzupassen. S-Gboxin schaltete diese Antwort eindeutig ein, doch das Blockieren von ATF4 mit einem kleinmolekularen Inhibitor oder durch genetisches Herunterregeln machte das Medikament nicht spürbar tödlicher, was darauf hinweist, dass dieser Stressweg Glioblastomzellen nicht stark vor S-Gboxin schützt. Eine andere Schutzvorrichtung erwies sich jedoch als entscheidend: AMPK, ein zentraler Energiesensor, der Zellen hilft, das Gleichgewicht wiederherzustellen, wenn ATP-Werte fallen. Wenn AMPK genetisch entfernt oder pharmakologisch blockiert wurde, wurden Glioblastomzellen deutlich empfindlicher gegenüber S-Gboxin, besonders unter niedrigem Glukosespiegel. Unter diesen Umständen lösten selbst moderate Wirkstoffdosen ausgeprägten Zelltod aus, während normale Astrozyten von der Kombination weitgehend unberührt blieben.
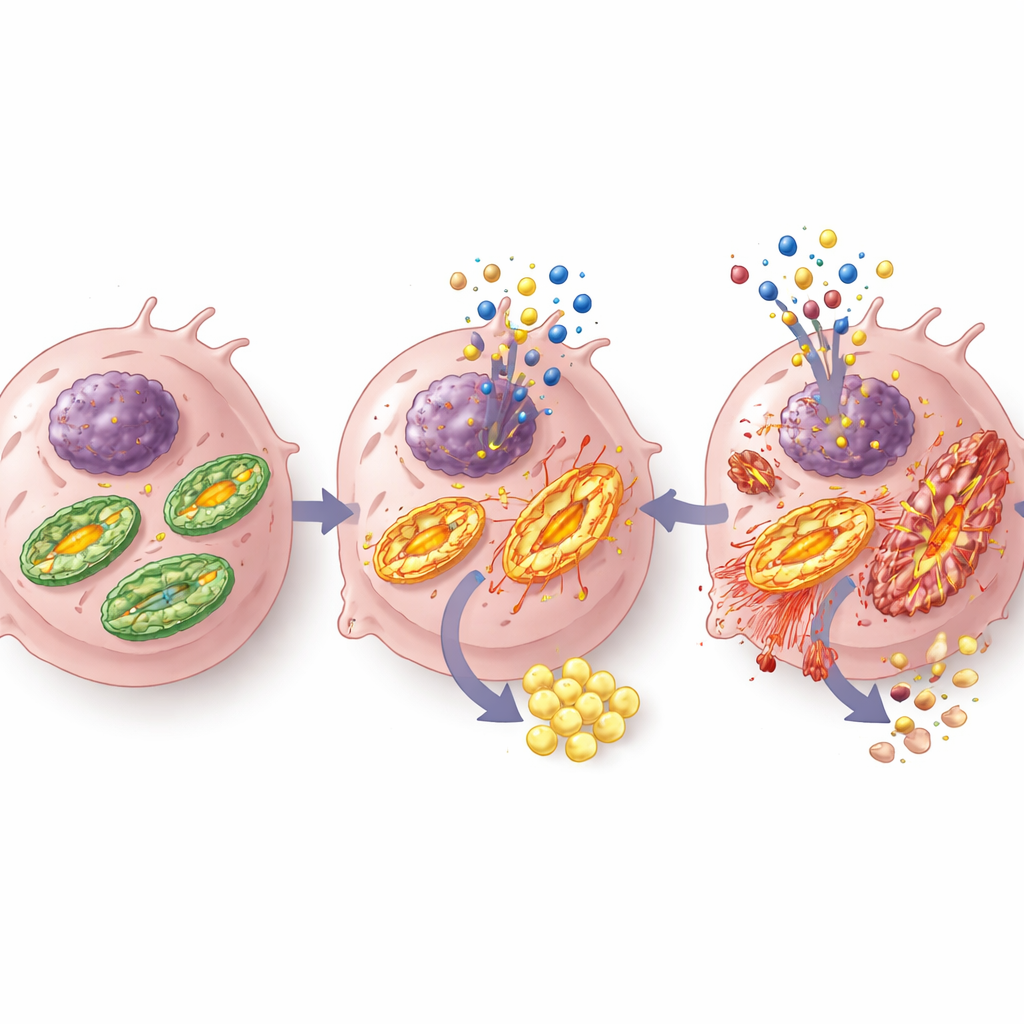
Den Hunger des Tumors in einen Behandlungsvorteil verwandeln
Insgesamt deuten die Ergebnisse darauf hin, dass S-Gboxin die Abhängigkeit des Glioblastoms von flexibler Energiegewinnung in eine verwundbare Stelle verwandelt. Durch die Störung der mitochondrialen Funktion und das Erzwingen eines verschwenderischen Mehrverbrauchs an Glukose ist das Medikament besonders wirksam unter den sehr nährstoffarmen, sauerstoffarmen Bedingungen, die das Tumorinnere kennzeichnen. Die Blockade des AMPK-Energiesensorwegs entzieht den Tumorzellen ein wichtiges Überlebenswerkzeug und kippt das Gleichgewicht weiter in Richtung Zelltod, ohne normale Gehirnzellen in diesen Experimenten erheblich zu schädigen. Zwar bleibt noch viel Arbeit — insbesondere um die Verabreichung an Tumoren im menschlichen Gehirn zu optimieren — doch die Studie weist auf eine Strategie hin, bei der sorgfältig entwickelte, den Stoffwechsel anvisierende Wirkstoffe in Kombination mit Inhibitoren von Energiesensoren eines Tages helfen könnten, Glioblastom von innen heraus auszuhungern.
Zitation: Weinem, JB., Urban, H., Sauer, B. et al. Targeting glioblastoma mitochondrial metabolism with S-Gboxin induces cytotoxicity under conditions of the tumor microenvironment. Cell Death Discov. 12, 181 (2026). https://doi.org/10.1038/s41420-026-03072-4
Schlüsselwörter: Glioblastom, Krebsstoffwechsel, Mitochondrien, S-Gboxin, AMPK-Inhibition