Clear Sky Science · pt
Variantes moleculares, evolução clonal e relevância clínica em neoplasias linfoblásticas de células T pediátricas e adultas
Por que esses cânceres sanguíneos importam para as famílias
As leucemias e linfomas de células T são cânceres agressivos que atingem principalmente crianças, adolescentes e adultos jovens. Apesar dos tratamentos modernos, muitos pacientes que recaem ainda enfrentam baixas chances de sobrevida. Este estudo faz uma pergunta aparentemente simples, com grandes consequências práticas: a leucemia de células T encontrada no sangue e na medula óssea e o linfoma linfoblástico estreitamente relacionado encontrado nos gânglios linfáticos são realmente a mesma doença, ou se comportam de forma diferente ao nível genético — e esse conhecimento pode ajudar os médicos a prever melhor quem terá recidiva?
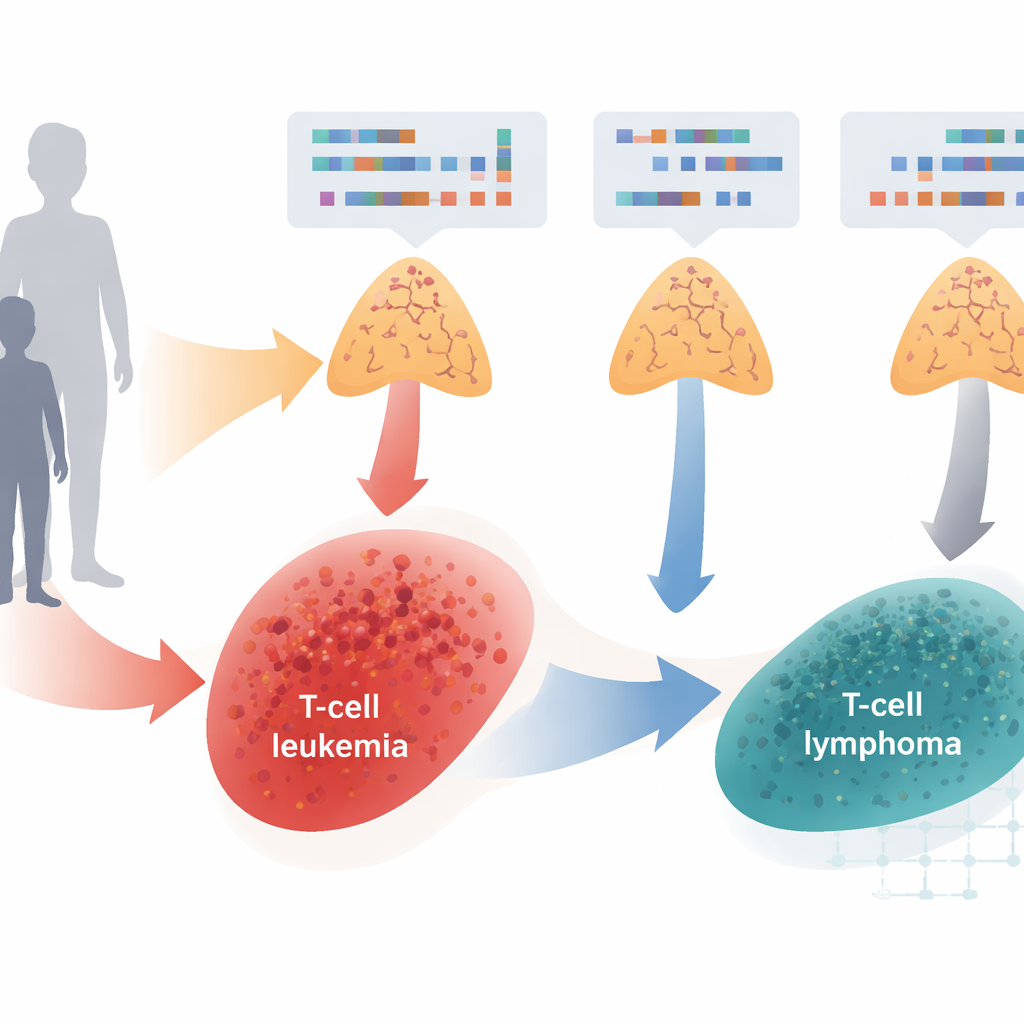
Dois cânceres relacionados sob o microscópio
Os pesquisadores examinaram amostras tumorais de 211 crianças e adultos com leucemia linfoblástica aguda de células T (T-ALL) ou linfoma linfoblástico de células T (T-LBL). Ambos os cânceres surgem de células T muito precoces no timo, mas geralmente são classificados pelo local onde as células cancerosas aparecem: principalmente na medula óssea e no sangue para a leucemia, e principalmente em gânglios linfáticos ou outros tecidos para o linfoma. Usando sequenciamento de DNA moderno e varreduras em todo o genoma, a equipe catalogou diferentes tipos de danos genéticos — pequenas alterações no DNA e ganhos ou perdas maiores de pedaços cromossômicos — e comparou os padrões entre faixas etárias e entre as duas doenças.
Raízes compartilhadas com diferenças relacionadas à idade
No geral, T-ALL e T-LBL apresentaram um conjunto muito semelhante de genes “motor” — genes que, quando danificados, ajudam a iniciar ou sustentar o câncer. Um gene em particular, NOTCH1, estava alterado na maioria dos pacientes em todos os grupos e tendia a ser mais comum em pacientes mais jovens. Outro gene, PHF6, tornou-se mais frequente com o aumento da idade. Enquanto o número total de mutações por paciente foi semelhante entre os grupos, alterações cromossômicas maiores se acumularam com a idade em T-ALL, mas não em T-LBL. Certos ganhos e perdas cromossômicos foram associados à recidiva em crianças com linfoma, sugerindo que mesmo cânceres intimamente relacionados podem envelhecer e evoluir de maneiras diferentes.
Primeiros golpes que moldam a árvore genealógica do câncer
Ao aprofundar, a equipe reconstruiu como cada tumor cresceu ao longo do tempo, construindo “árvores genealógicas” dos clones de células cancerosas. Eles descobriram que alterações em grande escala no cromossomo 9, especialmente deleções ou perda de uma cópia parental, frequentemente estavam entre os primeiros golpes genéticos tanto na leucemia quanto no linfoma. Esses eventos iniciais frequentemente afetavam um trecho do cromossomo 9 que inclui genes importantes do controle do ciclo celular, removendo essencialmente freios-chave ao crescimento celular. Em muitas crianças, células com esse dano no cromossomo 9 adquiriram depois mutações em NOTCH1, formando novos ramos do câncer que poderiam se expandir ou desaparecer durante o tratamento.
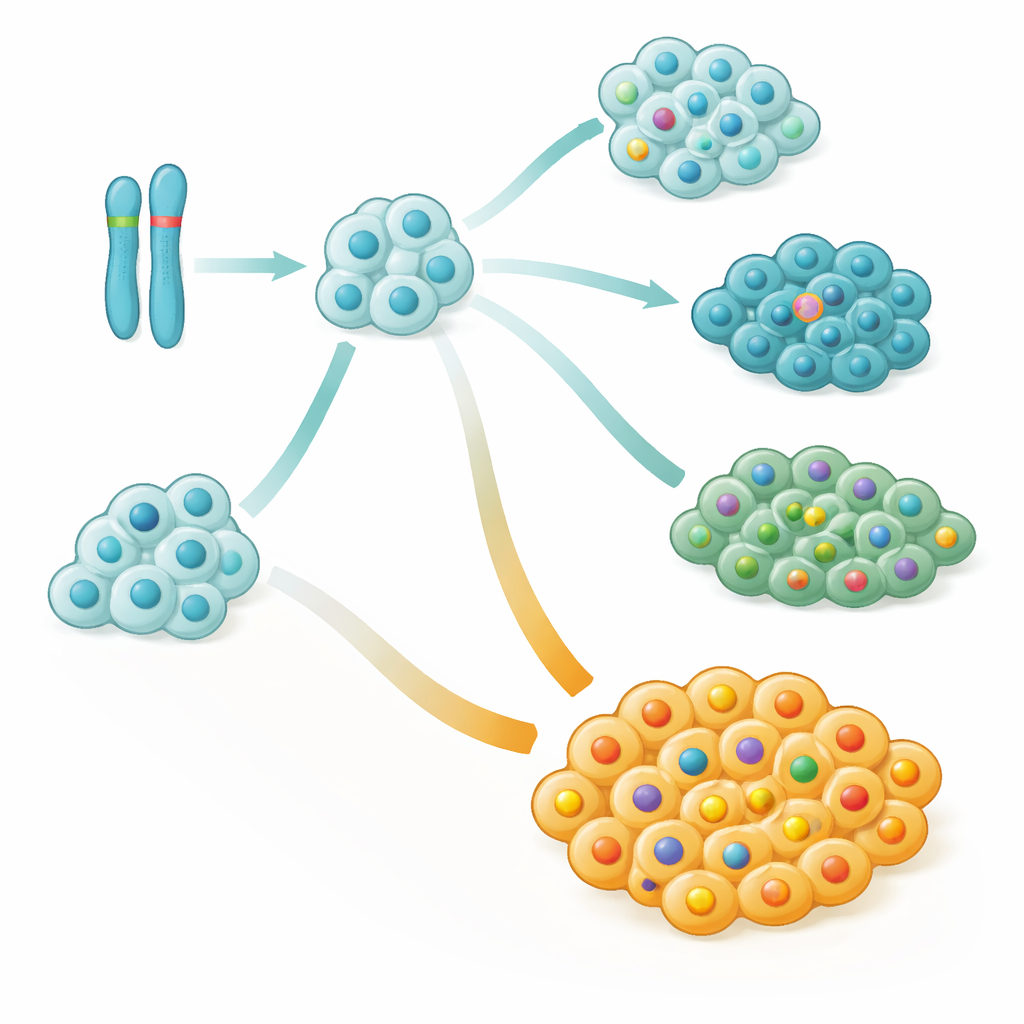
Ramos bons e ruins dentro do mesmo tumor
Uma visão surpreendente foi que alterações em NOTCH1, historicamente vistas apenas como promotoras do câncer, estavam na verdade associadas a melhores desfechos quando apareciam cedo e predominavam no tumor. Os pacientes tendiam a evoluir pior quando uma grande fração de suas células cancerosas não apresentava mutações em NOTCH1, mesmo que algumas células as tivessem. Em termos estatísticos, cada pequeno aumento na proporção de células cancerosas com NOTCH1 normal se traduzia em um salto significativo no risco de recidiva. Estudos de caso detalhados mostraram que recaídas agressivas muitas vezes surgiam de pequenos ramos laterais da árvore familiar do câncer que nunca adquiriram alterações em NOTCH1, mas acumularam outras alterações danosas.
O que isso significa para pacientes e médicos
O estudo sugere que, nesses cânceres de células T, quando e em que ramo da árvore familiar tumoral uma mutação aparece importa tanto quanto qual gene está mutado. O dano cromossômico precoce no cromossomo 9 parece preparar o terreno, enquanto diferentes ramos — com ou sem alterações em NOTCH1 — competem e respondem de forma distinta à terapia. Para os pacientes, isso abre a possibilidade de estimativas de risco mais precisas: não apenas perguntar “NOTCH1 está mutado?”, mas “quanto do tumor é conduzido por células mutantes de NOTCH1 versus células com NOTCH1 normal?”. Os autores argumentam que essas informações clonais, já promissoras no linfoma, poderiam ser usadas para ajustar melhor os grupos de risco e a intensidade do tratamento na leucemia de células T também, ajudando a combinar as terapias ao verdadeiro risco de recidiva de cada paciente.
Citação: Sandmann, S., te Vrugt, M., Randau, G. et al. Molecular variants, clonal evolution and clinical relevance in pediatric and adult T-cell lymphoblastic neoplasia. Blood Cancer J. 16, 57 (2026). https://doi.org/10.1038/s41408-026-01488-w
Palavras-chave: leucemia de células T, linfoma de células T, evolução clonal, alterações do cromossomo 9, mutação NOTCH1