Clear Sky Science · es
Variantes moleculares, evolución clonal y relevancia clínica en neoplasias linfoblásticas T pediátricas y adultas
Por qué estos cánceres sanguíneos importan para las familias
Las leucemias y linfomas de células T son cánceres agresivos que afectan sobre todo a niños, adolescentes y adultos jóvenes. A pesar de los tratamientos modernos, muchos pacientes que recaen siguen enfrentando peores probabilidades de supervivencia. Este estudio plantea una pregunta aparentemente sencilla con grandes consecuencias prácticas: ¿son la leucemia T que se encuentra en la sangre y la médula ósea y el linfoma estrechamente relacionado que aparece en los ganglios linfáticos realmente la misma enfermedad, o se comportan de forma diferente a nivel genético—y puede ese conocimiento ayudar a los médicos a predecir mejor quién recaerá?
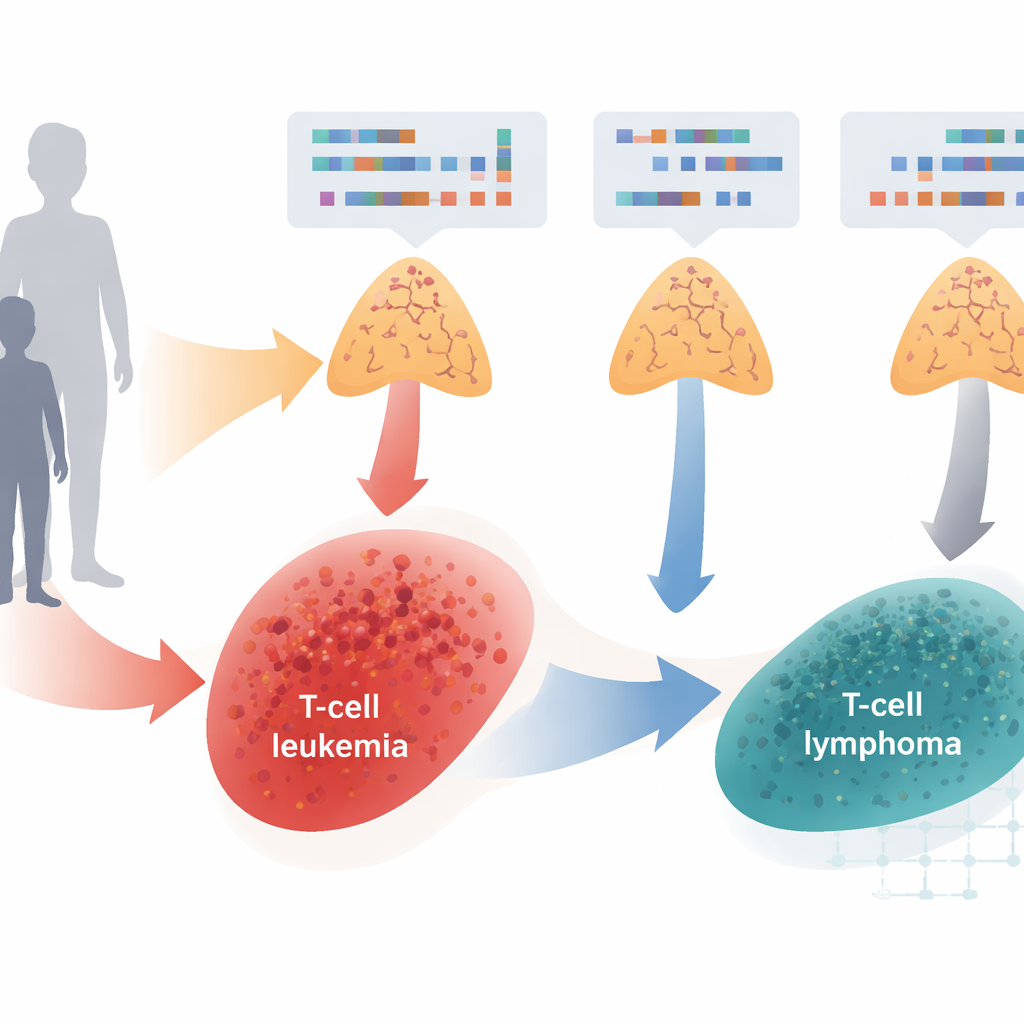
Dos cánceres relacionados bajo el microscopio
Los investigadores examinaron muestras tumorales de 211 niños y adultos con leucemia linfoblástica aguda de células T (T-ALL) o linfoma linfoblástico de células T (T-LBL). Ambos cánceres se originan en linfocitos T muy tempranos en el timo, pero suelen clasificarse según dónde aparecen las células cancerosas: principalmente en la médula ósea y la sangre para la leucemia, y principalmente en ganglios linfáticos u otros tejidos para el linfoma. Empleando secuenciación de ADN moderna y barridos genómicos a escala completa, el equipo catalogó distintos tipos de daño genético—cambios pequeños en el ADN y ganancias o pérdidas mayores de fragmentos cromosómicos—y comparó los patrones entre grupos de edad y entre las dos enfermedades.
Raíces compartidas con matices según la edad
En conjunto, T-ALL y T-LBL resultaron compartir un conjunto muy similar de genes “impulsores”—genes que, cuando se dañan, ayudan a iniciar o mantener el cáncer. Un gen en particular, NOTCH1, estaba alterado en la mayoría de los pacientes en todos los grupos y tendía a ser más común en pacientes más jóvenes. Otro gen, PHF6, se volvía más frecuente con la edad. Aunque el número total de mutaciones por paciente fue similar entre los grupos, los cambios cromosómicos de mayor escala se acumularon con la edad en T-ALL pero no en T-LBL. Ciertas ganancias y pérdidas cromosómicas se asociaron con recaída en niños con linfoma, lo que sugiere que incluso cánceres estrechamente relacionados pueden envejecer y evolucionar de maneras distintas.
Golpes tempranos que configuran el árbol genealógico del cáncer
Al profundizar más, el equipo reconstruyó cómo creció cada tumor a lo largo del tiempo, construyendo “árboles genealógicos” de clones de células cancerosas. Encontraron que los cambios a gran escala en el cromosoma 9, especialmente deleciones o la pérdida de una copia parental, estaban a menudo entre los primeros impactos genéticos en leucemia y linfoma. Estos eventos tempranos afectaban con frecuencia un tramo del cromosoma 9 que incluye genes importantes para el control del ciclo celular, eliminando esencialmente frenos clave del crecimiento celular. En muchos niños, las células que portaban este daño en el cromosoma 9 adquirieron después mutaciones en NOTCH1, formando nuevas ramas del cáncer que podían expandirse o desaparecer durante el tratamiento.
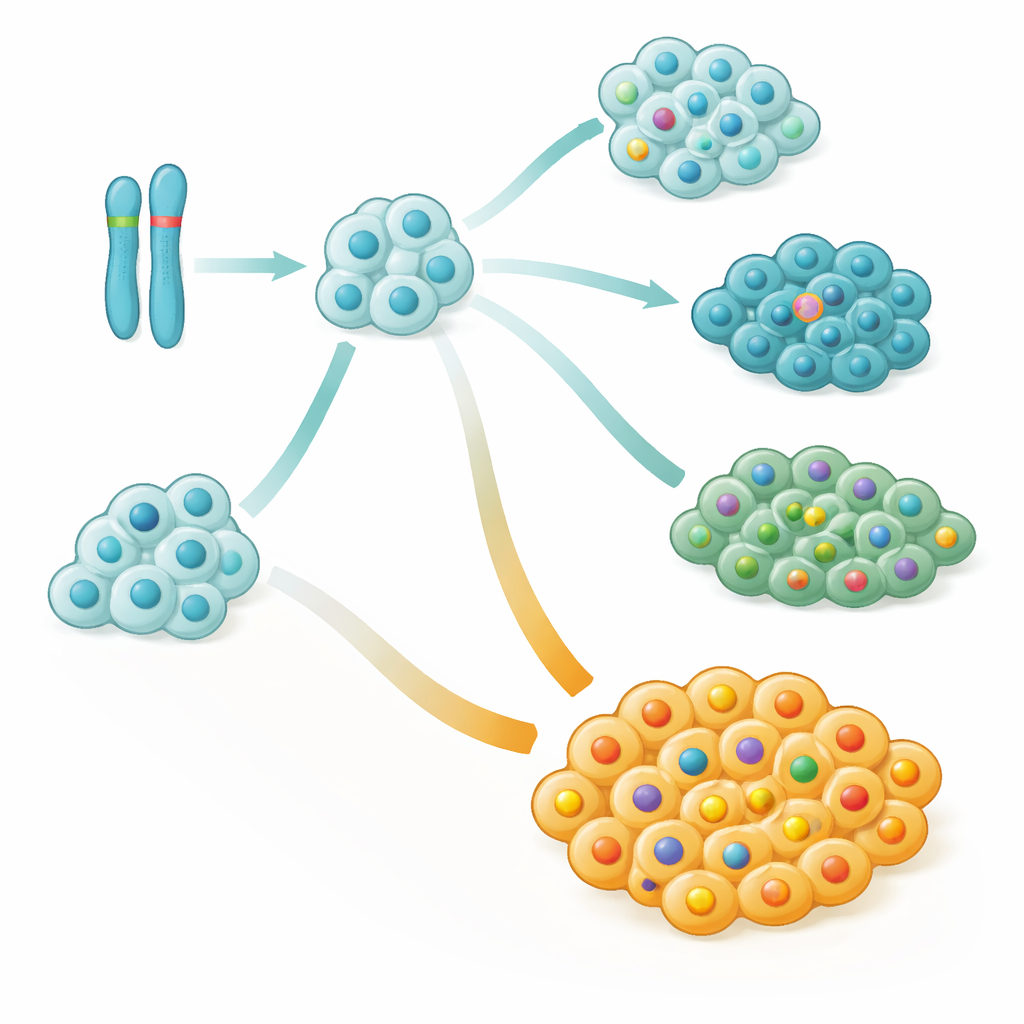
Ramas buenas y malas dentro del mismo tumor
Una idea sorprendente fue que los cambios en NOTCH1, tradicionalmente vistos simplemente como promotores del cáncer, estaban en realidad asociados a mejores resultados cuando aparecían temprano y dominaban el tumor. Los pacientes tendían a evolucionar peor cuando una gran fracción de sus células cancerosas carecía de mutaciones en NOTCH1, incluso si algunas células las tenían. En términos estadísticos, cada pequeño aumento en la proporción de células tumorales con NOTCH1 normal se tradujo en un salto significativo en el riesgo de recaída. Estudios de casos detallados mostraron que las recaídas agresivas a menudo surgieron de ramas menores del árbol familiar del cáncer que nunca adquirieron cambios en NOTCH1, pero sí acumularon otras alteraciones dañinas.
Qué significa esto para pacientes y médicos
El estudio sugiere que, en estos cánceres de células T, cuándo y dónde aparece una mutación dentro del árbol genealógico del tumor importa tanto como qué gen está mutado. El daño cromosómico temprano en el cromosoma 9 parece preparar el terreno, mientras que distintas ramas—con o sin cambios en NOTCH1—compiten y responden de modo diferente a la terapia. Para los pacientes, esto plantea la posibilidad de estimaciones de riesgo más precisas: no solo preguntar “¿está mutado NOTCH1?” sino “¿qué proporción del tumor está impulsada por células con NOTCH1 mutado frente a células con NOTCH1 normal?”. Los autores sostienen que esta información clonal, ya prometedora en linfoma, podría utilizarse para afinar grupos de riesgo e intensidad de tratamiento en la leucemia de células T, ayudando a ajustar mejor las terapias al riesgo real de recaída de cada paciente.
Cita: Sandmann, S., te Vrugt, M., Randau, G. et al. Molecular variants, clonal evolution and clinical relevance in pediatric and adult T-cell lymphoblastic neoplasia. Blood Cancer J. 16, 57 (2026). https://doi.org/10.1038/s41408-026-01488-w
Palabras clave: leucemia de células T, linfoma de células T, evolución clonal, alteraciones del cromosoma 9, mutación NOTCH1