Clear Sky Science · pl
Warianty molekularne, ewolucja klonalna i znaczenie kliniczne w dziecięcych i dorosłych nowotworach limfoblastycznych z komórek T
Dlaczego te nowotwory krwi mają znaczenie dla rodzin
Nowotwory limfoblastyczne i białaczki z komórek T to agresywne nowotwory, które najczęściej dotykają dzieci, nastolatków i młodych dorosłych. Mimo współczesnych terapii wielu pacjentów, u których dochodzi do nawrotu choroby, nadal ma złe rokowania. W badaniu postawiono pozornie proste pytanie o istotnych praktycznych konsekwencjach: czy białaczki z komórek T znajdujące się we krwi i szpiku oraz blisko spokrewnione chłoniaki występujące w węzłach chłonnych to rzeczywiście ta sama choroba, czy może różnią się zachowaniem na poziomie genetycznym — i czy ta wiedza może pomóc lekarzom lepiej przewidywać, u kogo wystąpi nawrót?
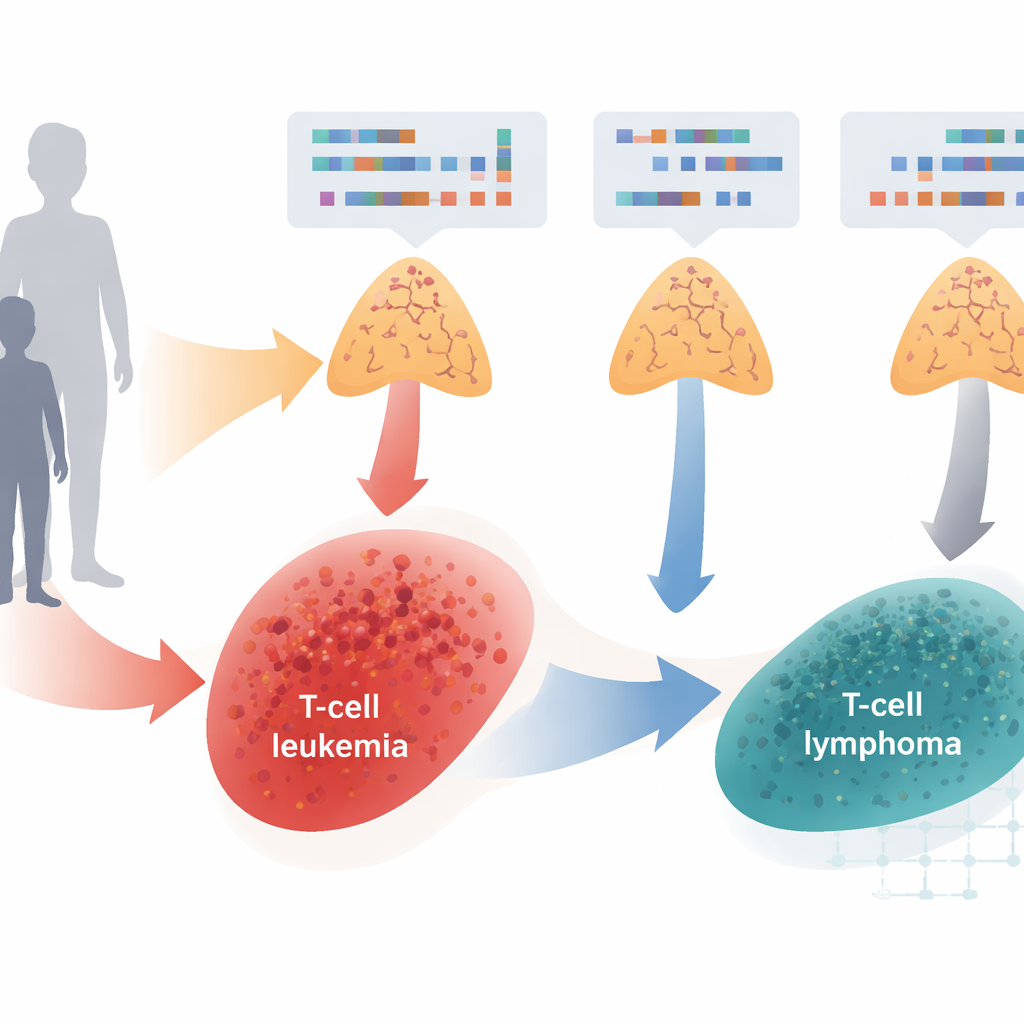
Dwa spokrewnione nowotwory pod mikroskopem
Naukowcy przeanalizowali próbki guza od 211 dzieci i dorosłych z rozpoznaniem ostrej białaczki limfoblastycznej z komórek T (T-ALL) lub limfoblastycznego chłoniaka z komórek T (T-LBL). Oba nowotwory wywodzą się z bardzo wczesnych komórek T w grasicy, ale zwykle klasyfikuje się je według tego, gdzie głównie występują: białaczki w szpiku kostnym i krwi, a chłoniaki w węzłach chłonnych lub innych tkankach. Dzięki nowoczesnemu sekwencjonowaniu DNA i badaniom obejmującym cały genom zespół skatalogował różne typy uszkodzeń genetycznych — małe zmiany w DNA oraz większe zyski lub straty fragmentów chromosomów — i porównał wzorce między grupami wiekowymi oraz między dwoma chorobami.
Wspólne korzenie z wiekowymi odcieniami
Ogólnie rzecz biorąc, T-ALL i T-LBL okazały się wykazywać bardzo podobny zestaw genów „driverowych” — genów, które po uszkodzeniu pomagają zapoczątkować lub utrzymać nowotwór. Szczególnie jeden gen, NOTCH1, był zmieniony u większości pacjentów we wszystkich grupach i zwykle występował częściej u młodszych pacjentów. Inny gen, PHF6, pojawiał się częściej wraz z wiekiem. Podczas gdy całkowita liczba mutacji na pacjenta była podobna w grupach, większe zmiany chromosomowe kumulowały się z wiekiem w T-ALL, ale nie w T-LBL. Pewne zyski i straty chromosomowe wiązały się z nawrotem u dzieci z chłoniakiem, co sugeruje, że nawet blisko spokrewnione nowotwory mogą się starzeć i ewoluować w różny sposób.
Wczesne uderzenia, które kształtują drzewo rodowe nowotworu
Dokładniejsza analiza pozwoliła zespołowi odtworzyć, jak każdy guz rozwijał się w czasie, budując „drzewa rodowe” klonów komórek nowotworowych. Stwierdzono, że zmiany dużej skali na chromosomie 9, zwłaszcza delecje lub utrata jednego rodzicielskiego allelu, często należały do pierwszych zdarzeń genetycznych zarówno w białaczce, jak i w chłoniaku. Wczesne wydarzenia często dotyczyły odcinka chromosomu 9 zawierającego ważne geny kontrolujące cykl komórkowy, co w praktyce usuwało kluczowe hamulce wzrostu komórek. U wielu dzieci komórki z uszkodzeniem chromosomu 9 później nabywały mutacje NOTCH1, tworząc nowe gałęzie nowotworu, które mogły się rozrastać lub wymierać podczas leczenia.
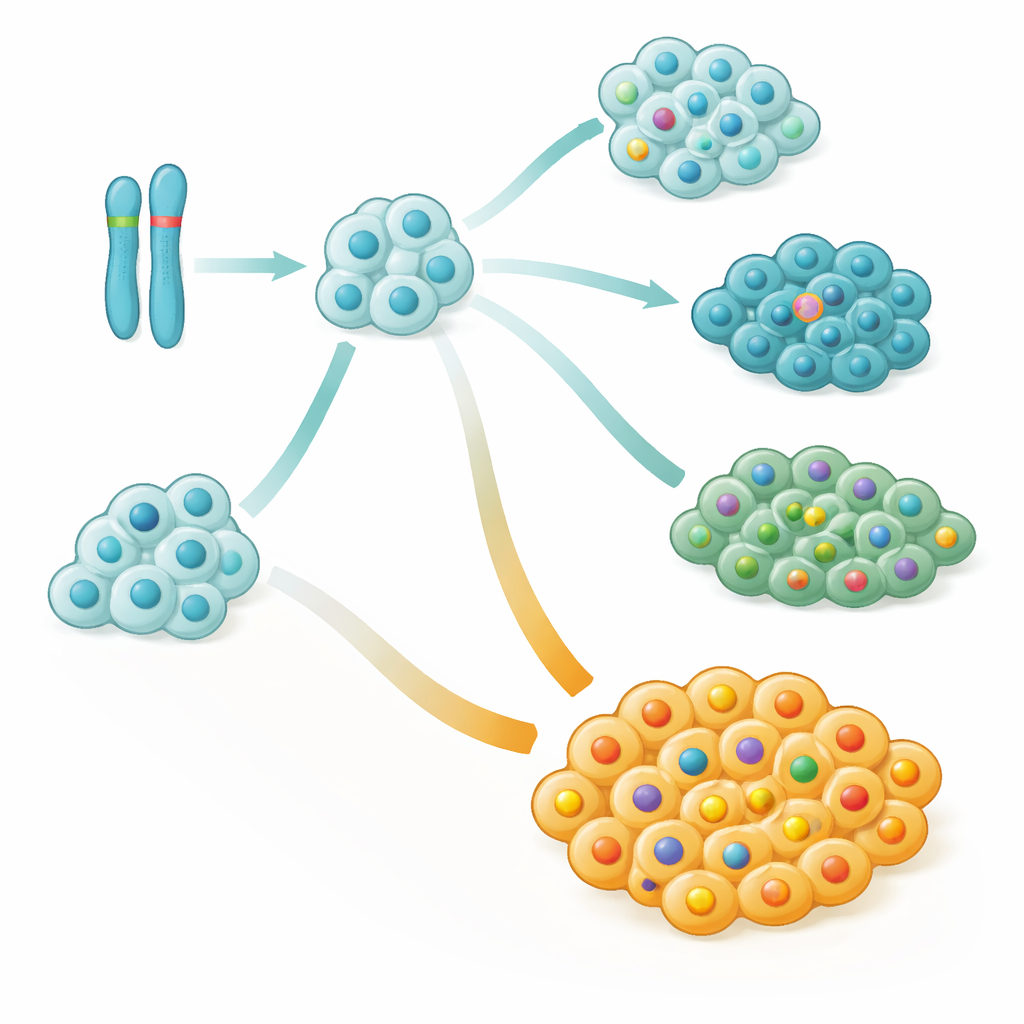
Dobre i złe gałęzie w obrębie tego samego guza
Jednym z zaskakujących wniosków było to, że zmiany w NOTCH1, długo postrzegane po prostu jako promujące nowotwór, były w rzeczywistości związane z lepszymi wynikami, gdy pojawiały się wcześnie i dominowały w guzie. Pacjenci mieli gorsze rokowanie, gdy duża część ich komórek nowotworowych nie miała mutacji NOTCH1, nawet jeśli niektóre komórki je posiadały. Statystycznie rzecz biorąc, każdy niewielki wzrost proporcji komórek nowotworowych z prawidłowym NOTCH1 wiązał się ze znaczącym wzrostem ryzyka nawrotu. Szczegółowe opisy przypadków wykazały, że agresywne nawroty często powstawały z drobnych odgałęzień drzewa rodzinnego nowotworu, które nigdy nie nabyły zmian w NOTCH1, lecz zgromadziły inne szkodliwe alteracje.
Co to oznacza dla pacjentów i lekarzy
Badanie sugeruje, że w tych nowotworach z komórek T ważne jest nie tylko które geny ulegają mutacji, lecz także kiedy i w jakiej części drzewa rodowego guza się pojawiają. Wczesne uszkodzenia chromosomu 9 wydają się przygotowywać grunt, podczas gdy różne gałęzie — z mutacją NOTCH1 lub bez niej — konkurują i różnie reagują na terapię. Dla pacjentów otwiera to możliwość dokładniejszych szacunków ryzyka: nie tylko pytania „czy NOTCH1 jest zmutowany?”, lecz „jak dużą część guza stanowią komórki napędzane przez komórki z mutacją NOTCH1 w porównaniu z komórkami o prawidłowym NOTCH1?”. Autorzy argumentują, że takie informacje klonalne, już obiecujące w chłoniakach, mogłyby służyć do precyzyjniejszego dzielenia na grupy ryzyka i dostosowywania intensywności leczenia także w białaczkach z komórek T, pomagając lepiej dopasować terapie do rzeczywistego ryzyka nawrotu u poszczególnych pacjentów.
Cytowanie: Sandmann, S., te Vrugt, M., Randau, G. et al. Molecular variants, clonal evolution and clinical relevance in pediatric and adult T-cell lymphoblastic neoplasia. Blood Cancer J. 16, 57 (2026). https://doi.org/10.1038/s41408-026-01488-w
Słowa kluczowe: bialaczka z komórek T, chłoniak z komórek T, ewolucja klonalna, zmiany w chromosomie 9, mutacja NOTCH1