Clear Sky Science · de
Molekulare Varianten, klonale Evolution und klinische Relevanz bei pädiatrischen und erwachsenen T‑Zell‑lymphoblastischen Neoplasien
Warum diese Bluttumoren für Familien wichtig sind
T‑Zell‑Leukämien und ‑Lymphome sind aggressive Krebserkrankungen, die überwiegend Kinder, Jugendliche und junge Erwachsene betreffen. Trotz moderner Therapien haben viele Patientinnen und Patienten, die einen Rückfall erleiden, weiterhin schlechte Überlebenschancen. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Handelt es sich bei der im Blut und Knochenmark nachweisbaren T‑Zell‑Leukämie und dem eng verwandten Lymphom in den Lymphknoten wirklich um dieselbe Krankheit — oder verhalten sie sich genetisch unterschiedlich, und kann dieses Wissen Ärzten helfen, Rückfälle besser vorherzusagen?
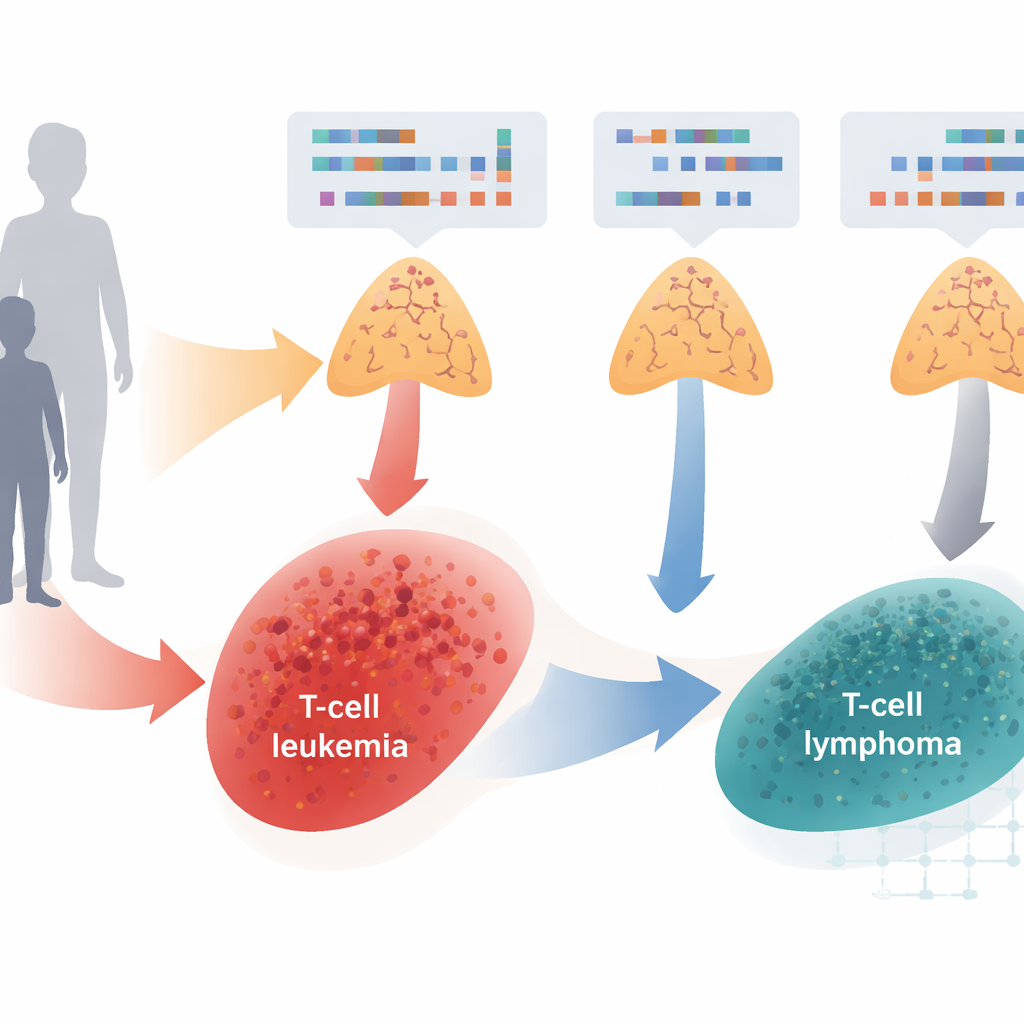
Zwei verwandte Krebserkrankungen unter dem Mikroskop
Die Forschenden untersuchten Tumorproben von 211 Kindern und Erwachsenen mit entweder T‑zelliger akuter lymphatischer Leukämie (T‑ALL) oder T‑zelligem lymphoblastischem Lymphom (T‑LBL). Beide Krebsarten entstehen aus sehr frühen T‑Zellen im Thymus, werden aber üblicherweise nach dem vorherrschenden Klinikbild klassifiziert: Bei der Leukämie finden sich die Krebszellen hauptsächlich im Knochenmark und Blut, beim Lymphom hauptsächlich in Lymphknoten oder anderen Geweben. Mithilfe moderner DNA‑Sequenzierung und genomweiter Analysen katalogisierte das Team verschiedene Arten genetischer Schäden — kleine DNA‑Veränderungen sowie größere Gewinne oder Verluste von Chromosomenabschnitten — und verglich die Muster zwischen Altersgruppen und den beiden Erkrankungen.
Gemeinsame Wurzeln mit altersbedingten Unterschieden
Insgesamt zeigten T‑ALL und T‑LBL ein sehr ähnliches Spektrum an sogenannten Treibergenen — Gene, die bei Schädigung die Entstehung oder Aufrechterhaltung des Krebses fördern. Ein Gen stach dabei besonders hervor: NOTCH1 war in der Mehrheit der Patientinnen und Patienten in allen Gruppen verändert und trat tendenziell häufiger bei Jüngeren auf. Ein anderes Gen, PHF6, wurde mit zunehmendem Alter häufiger. Während die Gesamtzahl der Mutationen pro Patient in den Gruppen ähnlich war, häuften sich größere chromosomale Veränderungen mit dem Alter bei T‑ALL, nicht jedoch bei T‑LBL. Bestimmte Chromosomengewinne und‑verluste standen bei Kindern mit Lymphom in Zusammenhang mit Rückfällen, was darauf hindeutet, dass sich eng verwandte Krebsformen altersabhängig unterschiedlich entwickeln und altern können.
Frühe Treffer, die den Stammbaum des Krebses formen
Bei detaillierterer Analyse rekonstruierten die Forschenden, wie jeder Tumor im Verlauf gewachsen ist, und bauten so „Stammbäume“ der Krebszellklone. Sie fanden, dass großflächige Veränderungen auf Chromosom 9, insbesondere Deletionen oder der Verlust einer elterlichen Kopie, häufig zu den allerersten genetischen Ereignissen bei sowohl Leukämien als auch Lymphomen gehörten. Diese frühen Ereignisse betrafen oft einen Abschnitt von Chromosom 9, der wichtige Gene zur Zellzyklussteuerung umfasst, und entfernten damit praktisch zentrale Bremsen des Zellwachstums. Bei vielen Kindern erwarben Zellen mit dieser Chromosom‑9‑Schädigung später NOTCH1‑Mutationen, wodurch neue Zweige des Tumors entstanden, die während der Behandlung entweder expandierten oder ausstarben.
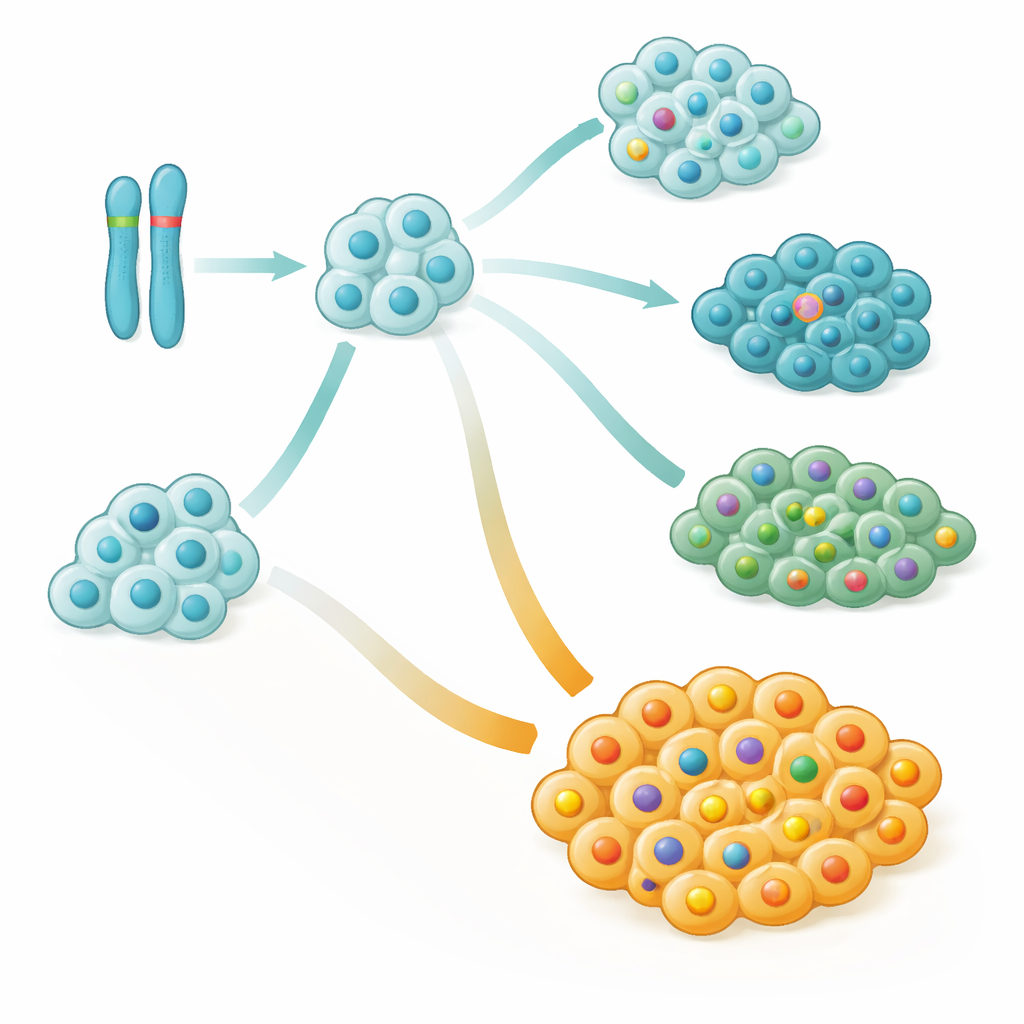
Gute und schlechte Zweige innerhalb desselben Tumors
Eine überraschende Erkenntnis war, dass NOTCH1‑Veränderungen, lange Zeit einfach als krebstreibend angesehen, tatsächlich mit besseren Ergebnissen verknüpft waren, wenn sie früh auftraten und den Tumor dominierten. Patientinnen und Patienten hatten tendenziell schlechtere Verläufe, wenn ein großer Anteil ihrer Krebszellen keine NOTCH1‑Mutationen trug, selbst wenn einige Zellen solche Mutationen aufwiesen. Statistisch gesehen führte jeder kleine Anstieg des Anteils an NOTCH1‑normalen Krebszellen zu einem spürbaren Anstieg des Rückfallrisikos. Detaillierte Fallstudien zeigten, dass aggressive Rückfälle oft aus kleinen Nebenästen des Krebsstammbaums hervorgingen, die nie NOTCH1‑Veränderungen erworben hatten, sondern stattdessen andere schädigende Alterationen ansammelten.
Was das für Patientinnen, Patienten und Ärztinnen, Ärzte bedeutet
Die Studie legt nahe, dass in diesen T‑Zell‑Krebsformen nicht nur wichtig ist, welches Gen mutiert ist, sondern auch wann und in welchem Zweig des Tumorstammbaums die Mutation auftaucht. Frühe Chromosom‑9‑Schäden scheinen den Rahmen zu setzen, während verschiedene Zweige — mit oder ohne NOTCH1‑Veränderungen — miteinander konkurrieren und unterschiedlich auf Therapien reagieren. Für Betroffene eröffnet dies die Möglichkeit präziserer Risikoabschätzungen: nicht nur die Frage „Ist NOTCH1 mutiert?“, sondern „Welcher Anteil des Tumors wird von NOTCH1‑mutierten gegenüber NOTCH1‑normalen Zellen angetrieben?“ Die Autorinnen und Autoren argumentieren, dass solche klonalen Informationen, die bereits beim Lymphom vielversprechend sind, auch genutzt werden könnten, um Risikogruppen und Behandlungsintensität bei T‑Zell‑Leukämien feiner zuzuschneiden und Therapien besser an das tatsächliche Rückfallrisiko der einzelnen Patientinnen und Patienten anzupassen.
Zitation: Sandmann, S., te Vrugt, M., Randau, G. et al. Molecular variants, clonal evolution and clinical relevance in pediatric and adult T-cell lymphoblastic neoplasia. Blood Cancer J. 16, 57 (2026). https://doi.org/10.1038/s41408-026-01488-w
Schlüsselwörter: T‑Zell‑Leukämie, T‑Zell‑Lymphom, klonale Evolution, Chromosom‑9‑Veränderungen, NOTCH1‑Mutation