Clear Sky Science · pt
Transcritos do cérebro humano e de organoides revelam vias-chave de tirosina quinase de receptor e assinaturas genéticas na doença de Alzheimer
Por que isso importa para entender a doença de Alzheimer
A doença de Alzheimer é geralmente descrita em termos de placas pegajosas e proteínas emaranhadas no cérebro. Mas por trás dessas mudanças visíveis há uma história mais silenciosa escrita em genes e sinais entre células. Este estudo investiga os bastidores do cérebro humano e de “mini-cérebros” cultivados em laboratório para descobrir quais chaves de sinalização nas células cerebrais estão mais perturbadas na doença de Alzheimer e se elas poderiam nos ajudar a detectar ou até tratar a doença mais cedo.
Procurando sinais ocultos em uma região cerebral vulnerável
Os pesquisadores focaram no giro temporal médio, uma região do cérebro importante para linguagem e memória que é afetada precocemente na doença de Alzheimer. Eles analisaram a atividade gênica de centenas de milhares de genes em tecido cerebral doado por pessoas com Alzheimer e por pessoas sem a doença. Ao comparar dois grandes conjuntos de dados públicos dos Estados Unidos e da Europa, concentraram-se em 145 genes que estavam consistentemente alterados em cérebros com Alzheimer. Muitos desses genes se agrupavam em torno de uma família de moléculas de superfície chamadas receptores, que funcionam como antenas que permitem que as células cerebrais percebam e respondam ao ambiente.
“Antenas” receptoras e uma lista curta de genes suspeitos
Aprofundando, a equipe usou vários bancos de dados biológicos online para identificar a quais vias esses 145 genes pertenciam. Emergiu um sinal forte das tirosina quinases receptoras, um grupo de receptores que ajuda a controlar a sobrevivência, o crescimento e a comunicação celular. Deste grupo, reduziram a lista para 18 genes ligados a essas vias de receptor e então construíram um mapa de interação que também incluiu genes bem conhecidos da doença de Alzheimer associados à amiloide e à tau. Essa análise de rede destacou seis genes que ocupavam cruzamentos-chave: AXL e ITGB1 (ambos envolvidos em como as células percebem seu entorno), GFAP (um marcador de astrócitos), CAV1 e RHOA (que ajudam a moldar a estrutura e a sinalização celular) e NRG1 (importante para o desenvolvimento cerebral). Em cérebros com Alzheimer, cinco desses genes estavam acima do normal, enquanto NRG1 estava reduzido.
Testando as descobertas em mini-cérebros e neurônios
Para ir além das análises computacionais, os pesquisadores recorreram a organoides cerebrais derivados de células-tronco humanas — “mini-cérebros” tridimensionais que contêm neurônios e células de suporte — e a neurônios primários de rato cultivados em placas. Ao expor esses organoides à beta-amiloide, a proteína tóxica ligada às placas, os níveis de vários dos genes-chave, incluindo AXL e ITGB1, aumentaram. Testes de proteína mostraram que AXL aumentou dentro dos organoides, e ITGB1 aumentou especificamente na membrana celular, onde pode influenciar como as células se aderem e sinalizam entre si. Ao mesmo tempo, uma via de sinalização interna importante chamada via PI3K–AKT tornou-se mais ativa, sugerindo que a amiloide pode estar acionando um ramo específico da sinalização por receptores em vez de apenas causar estresse geral.
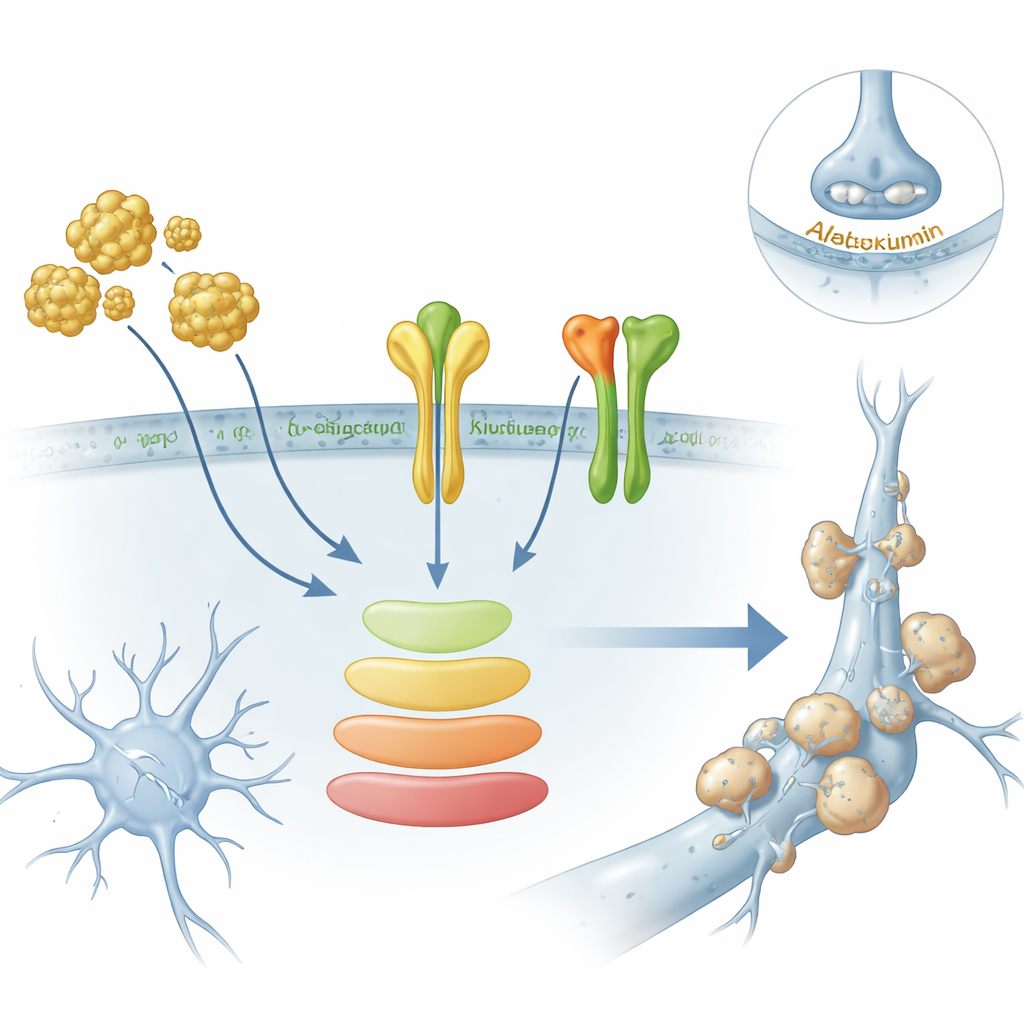
De padrões gênicos a possíveis biomarcadores
A equipe então investigou se a atividade combinada dos seis genes destacados poderia ajudar a distinguir cérebros com Alzheimer daqueles cognitivamente normais. Usando modelos estatísticos, descobriram que uma pontuação construída a partir desses seis genes separou os dois grupos com alta precisão em ambas as coortes cerebrais. Pontuações mais altas também se correlacionaram com classificações clínicas de demência mais severas. Isso sugere que padrões de atividade gênica relacionados a receptores, especialmente envolvendo AXL e ITGB1, podem servir como impressões moleculares das alterações associadas ao Alzheimer no giro temporal médio e talvez em outras regiões vulneráveis, como o hipocampo.
O que isso pode significar para diagnóstico e tratamento futuros
No geral, o estudo propõe que certas vias de receptores, centradas no receptor AXL e na integrina ITGB1, tornam-se hiperativas em condições semelhantes às da doença de Alzheimer e alimentam um ciclo de sinalização que pode agravar a doença. Embora ainda faltem muitos trabalhos — especialmente experimentos que liguem ou desliguem diretamente esses genes em sistemas vivos — as descobertas apontam para uma nova camada da biologia do Alzheimer além de placas e emaranhados. A longo prazo, medir essas alterações gênicas e proteicas, ou reduzir com segurança vias de receptores hiperativas, pode complementar as abordagens existentes para diagnosticar e tratar a doença de Alzheimer.
Citação: Shin, S., Zhu, X., Amartumur, S. et al. Human brain and organoid transcriptomes reveal key receptor tyrosine kinase pathways and genetic signatures in Alzheimer's disease. Exp Mol Med 58, 1230–1241 (2026). https://doi.org/10.1038/s12276-026-01684-5
Palavras-chave: Doença de Alzheimer, sinalização cerebral, vias de receptor, organoides cerebrais, biomarcadores