Clear Sky Science · de
Menschliches Gehirn- und Organoid-Transkriptome zeigen zentrale Rezeptor-Tyrosinkinase-Wege und genetische Signaturen bei Alzheimer
Warum das für das Verständnis von Alzheimer wichtig ist
Alzheimer wird meist anhand von klebrigen Plaques und verfilzten Proteinen im Gehirn beschrieben. Hinter diesen sichtbaren Veränderungen verbirgt sich jedoch eine leisere Geschichte, geschrieben in Genen und zellulären Signalen. Diese Studie schaut in das Innenleben des menschlichen Gehirns und in im Labor gezüchtete „Mini-Gehirne“, um herauszufinden, welche Schaltkreise der Signalübertragung in Gehirnzellen bei Alzheimer am stärksten gestört sind und ob sie uns helfen könnten, die Krankheit früher zu erkennen oder zu behandeln.
Suche nach verborgenen Signalen in einer besonders anfälligen Hirnregion
Die Forschenden konzentrierten sich auf den mittleren temporalen Gyrus, eine für Sprache und Gedächtnis wichtige Hirnregion, die bei Alzheimer früh betroffen ist. Sie analysierten die Genaktivität von Hunderttausenden von Genen in Hirngewebe, das von Menschen mit und ohne Alzheimer gespendet wurde. Durch den Vergleich zweier großer öffentlicher Datensätze aus den USA und Europa identifizierten sie 145 Gene, die in Alzheimer-Gehirnen konsistent verändert waren. Viele dieser Gene gruppierten sich um eine Familie von Oberflächenmolekülen, den Rezeptoren, die wie Antennen arbeiten und den Zellen erlauben, ihre Umgebung zu erfassen und darauf zu reagieren.
Rezeptor-„Antennen“ und eine kurze Liste verdächtiger Gene
Bei tiefergehender Analyse nutzte das Team mehrere Online-Biologiedatenbanken, um zu bestimmen, welchen Signalwegen diese 145 Gene zugeordnet sind. Ein deutliches Signal kam aus den Rezeptor-Tyrosinkinasen, einer Gruppe von Rezeptoren, die das Überleben, Wachstum und die Kommunikation von Zellen steuern. Aus dieser Gruppe reduzierte sich die Liste auf 18 Gene, die mit diesen Rezeptorwegen verbunden sind; anschließend erstellten die Forschenden eine Interaktionskarte, die auch bekannte Alzheimer-Gene im Zusammenhang mit Amyloid und Tau einbezog. Diese Netzwerk-Analyse hob sechs Gene als zentrale Knotenpunkte hervor: AXL und ITGB1 (beide an der Umweltwahrnehmung von Zellen beteiligt), GFAP (ein Astrozyten-Marker), CAV1 und RHOA (die Struktur und Signalübertragung der Zelle beeinflussen) sowie NRG1 (wichtig für die Gehirnentwicklung). In Alzheimer-Gehirnen waren fünf dieser Gene hochreguliert, während NRG1 herunterreguliert war.
Überprüfung der Befunde in Mini-Gehirnen und Neuronen
Um über computergestützte Analysen hinauszugehen, arbeiteten die Forschenden mit aus menschlichen Stammzellen gewonnenen Gehirn-Organoiden – dreidimensionalen „Mini-Gehirnen“, die Neuronen und Stützzellen enthalten – sowie mit primären Rattenneuronenkulturen. Exponierte man diese Organoide dem amyloid-beta, dem toxischen Protein, das mit Plaques verbunden ist, so stiegen die Spiegel mehrerer Schlüsselgene, darunter AXL und ITGB1. Proteintests zeigten, dass AXL innerhalb der Organoide zunahm, während ITGB1 speziell an der Zellmembran anstieg, wo es beeinflussen kann, wie Zellen haften und miteinander kommunizieren. Gleichzeitig wurde ein wichtiger interner Signalweg, die PI3K–AKT-Signalkaskade, aktiver, was darauf hindeutet, dass Amyloid eine bestimmte Verzweigung der Rezeptorsignalisierung antreiben könnte, statt nur allgemeinen Stress zu verursachen.
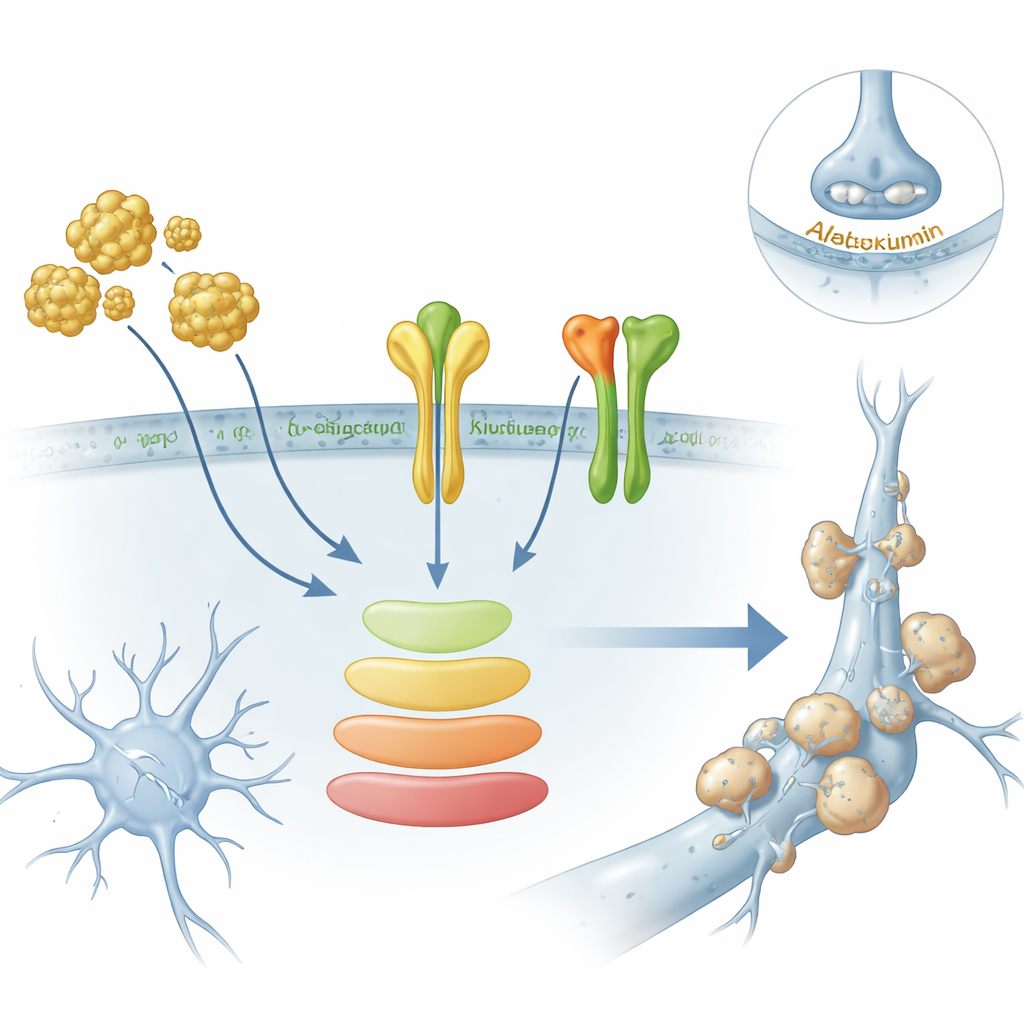
Von Genmustern zu möglichen Biomarkern
Das Team prüfte dann, ob die kombinierte Aktivität der sechs hervorgehobenen Gene helfen könnte, Alzheimer-Gehirne von kognitiv normalen Gehirnen zu unterscheiden. Mithilfe statistischer Modelle fanden sie, dass ein aus diesen sechs Genen entwickelter Score die beiden Gruppen in beiden Hirn-Kohorten mit hoher Genauigkeit trennte. Höhere Scores korrelierten außerdem mit schwereren klinischen Demenzbewertungen. Das deutet darauf hin, dass Muster rezeptorbezogener Genaktivität, insbesondere unter Beteiligung von AXL und ITGB1, als molekulare Fingerabdrücke Alzheimer-typischer Veränderungen im mittleren temporalen Gyrus und möglicherweise in anderen besonders anfälligen Regionen wie dem Hippocampus dienen könnten.
Was das für Diagnose und Behandlung in der Zukunft bedeuten könnte
Insgesamt schlägt die Studie vor, dass bestimmte Rezeptorwege, zentriert um den AXL-Rezeptor und das Integrin ITGB1, in Alzheimer-ähnlichen Zuständen überaktiv werden und in eine Signalschleife einmünden könnten, die die Krankheit verschlechtert. Obwohl noch viel Arbeit erforderlich ist – insbesondere Experimente, die diese Gene in lebenden Systemen gezielt ein- oder ausschalten – zeigen die Ergebnisse eine neue Ebene der Alzheimer-Biologie jenseits von Plaques und Verfilzungen. Langfristig könnten das Messen dieser Gen- und Proteinveränderungen oder das sichere Herunterregulieren überaktiver Rezeptorwege bestehende Ansätze zur Diagnose und Behandlung der Alzheimer-Krankheit ergänzen.
Zitation: Shin, S., Zhu, X., Amartumur, S. et al. Human brain and organoid transcriptomes reveal key receptor tyrosine kinase pathways and genetic signatures in Alzheimer's disease. Exp Mol Med 58, 1230–1241 (2026). https://doi.org/10.1038/s12276-026-01684-5
Schlüsselwörter: Alzheimer-Krankheit, Gehirnsignale, Rezeptorwege, Gehirn-Organoide, Biomarker