Clear Sky Science · nl
Transcriptoomgegevens van menselijk brein en organoïden onthullen sleutelsignalering via receptor-tyrosinekinasen en genetische handtekeningen bij de ziekte van Alzheimer
Waarom dit belangrijk is voor het begrijpen van Alzheimer
De ziekte van Alzheimer wordt meestal beschreven aan de hand van kleverige plaques en verwarde eiwitten in de hersenen. Maar achter die zichtbare veranderingen gaat een stillere verhaallijn schuil, geschreven in genen en in cel-tot-cel communicatie. Deze studie kijkt onder de motorkap van het menselijk brein en van in het laboratorium gekweekte “mini-breinen” om te achterhalen welke signaalknoppen van hersencellen het meest verstoord zijn bij Alzheimer, en of die ons kunnen helpen de ziekte eerder te detecteren of mogelijk te behandelen.
Op zoek naar verborgen signalen in een kwetsbare hersenregio
De onderzoekers richtten zich op de middle temporal gyrus, een hersengebied dat belangrijk is voor taal en geheugen en dat vroeg wordt aangedaan bij Alzheimer. Ze analyseerden genactiviteit van honderden duizenden genen in hersenweefsel geschonken door mensen met en zonder Alzheimer. Door twee grote openbare datasets uit de Verenigde Staten en Europa te vergelijken, isoleerden ze 145 genen die consequent veranderd waren in Alzheimer-hersenen. Veel van deze genen groepeerden rond een familie van oppervlaktemoleculen die receptoren worden genoemd, die als antennes functioneren zodat hersencellen hun omgeving kunnen waarnemen en erop kunnen reageren.
Receptor-“antennes” en een korte lijst verdachte genen
Dieper gravend gebruikten de onderzoekers meerdere online biologische databases om te bepalen tot welke routes deze 145 genen behoorden. Een sterk signaal kwam van receptor-tyrosinekinasen, een groep receptoren die helpt bij de regulatie van celdood, groei en communicatie. Uit deze groep versmalden ze de lijst tot 18 genen die aan deze receptorroutes zijn gekoppeld, en bouwden vervolgens een interactiekaart die ook bekende Alzheimer-genen rond amyloïd en tau omvatte. Deze netwerkanalyse lichtte zes genen uit die op belangrijke kruispunten lagen: AXL en ITGB1 (beide betrokken bij hoe cellen hun omgeving waarnemen), GFAP (een astrocytenmarker), CAV1 en RHOA (die structuur en signalering van cellen helpen vormen) en NRG1 (belangrijk voor hersenontwikkeling). In Alzheimer-hersenen waren vijf van deze genen omhooggereguleerd, terwijl NRG1 omlaaggereguleerd was.
De bevindingen testen in mini-breinen en neuronen
Om verder te gaan dan computeraanalyse schakelden de onderzoekers over naar humane stamcel-afgeleide hersenorganoïden — driedimensionale “mini-breinen” die neuronen en ondersteunende cellen bevatten — en naar primaire ratteneurnen gekweekt in schalen. Toen ze deze organoïden blootstelden aan amyloïd-beta, het toxische eiwit dat aan plaques wordt gekoppeld, steeg het niveau van meerdere van de sleutelgenen, waaronder AXL en ITGB1. Eiwitmetingen lieten zien dat AXL in de organoïden toenam, en ITGB1 specifiek aan het celmembraan toenam, waar het kan beïnvloeden hoe cellen hechten en signaleren naar elkaar. Tegelijkertijd werd een belangrijke interne signaallijn, de PI3K–AKT-route, actiever, wat suggereert dat amyloïd mogelijk een specifieke tak van receptor-gestuurde signalering aanjaagt in plaats van alleen algemene stress te veroorzaken.
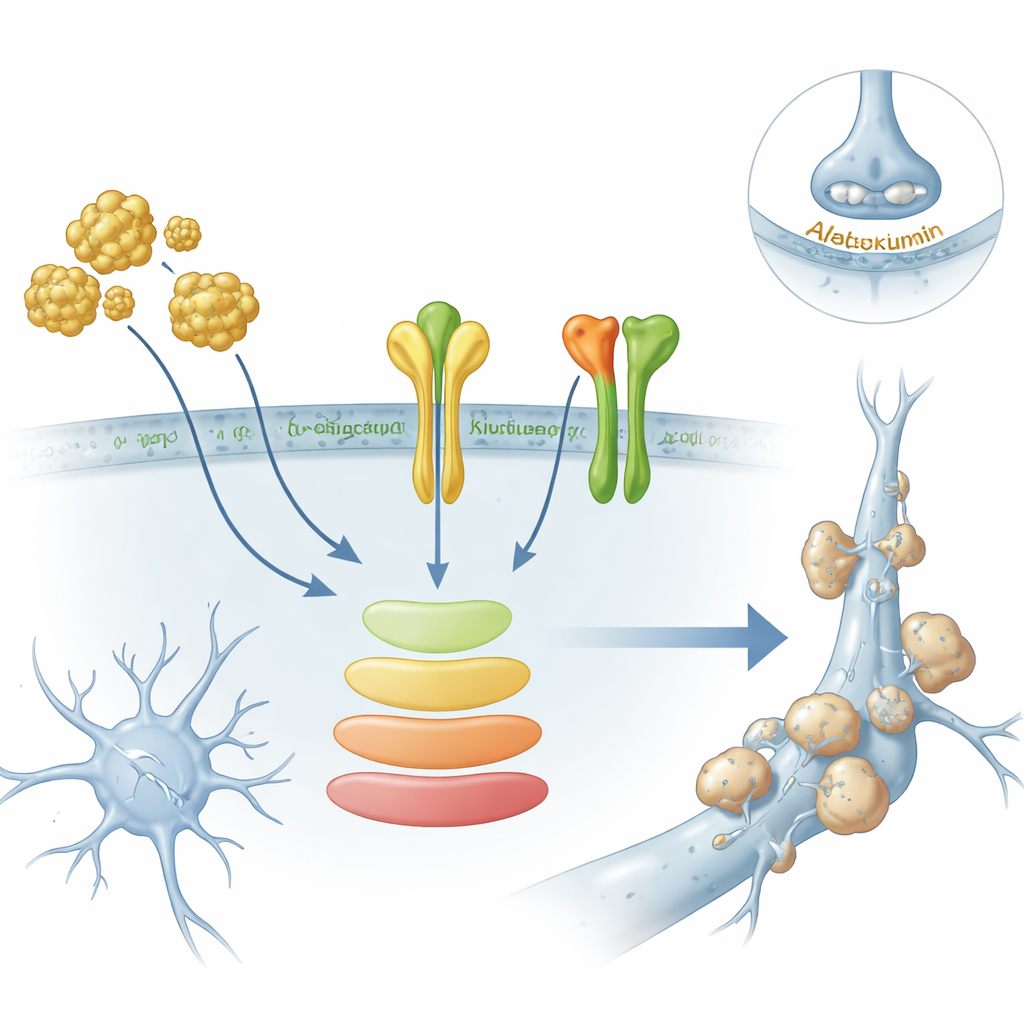
Van genpatronen naar mogelijke biomarkers
Vervolgens onderzochten de onderzoekers of de gezamenlijke activiteit van de zes uitgelichte genen Alzheimer-hersenen kon onderscheiden van cognitief normale hersenen. Met statistische modellen vonden ze dat een score samengesteld uit deze zes genen de twee groepen met hoge nauwkeurigheid scheidde in beide breindatasets. Hogere scores correleerden ook met ernstigere klinische dementiescores. Dit suggereert dat patronen van receptor-gerelateerde genactiviteit, met name rond AXL en ITGB1, als moleculaire vingerafdrukken kunnen dienen van Alzheimer-gerelateerde veranderingen in de middle temporal gyrus en mogelijk ook in andere kwetsbare regio’s zoals de hippocampus.
Wat dit kan betekenen voor toekomstige diagnostiek en behandeling
Over het geheel genomen stelt de studie voor dat bepaalde receptorroutes, gecentreerd rond de AXL-receptor en de integrine ITGB1, overactief worden in Alzheimer-achtige omstandigheden en bijdragen aan een signaleringslus die de ziekte kan verergeren. Hoewel er nog veel werk te doen is — met name experimenten die deze genen direct aan- of uitzetten in levende systemen — wijzen de bevindingen op een nieuwe laag van Alzheimer-biologie voorbij plaques en tangles. Op de lange termijn kan het meten van deze genen- en eiwitveranderingen, of het veilig terugschakelen van overactieve receptorroutes, bestaande benaderingen voor de diagnose en behandeling van de ziekte van Alzheimer aanvullen.
Bronvermelding: Shin, S., Zhu, X., Amartumur, S. et al. Human brain and organoid transcriptomes reveal key receptor tyrosine kinase pathways and genetic signatures in Alzheimer's disease. Exp Mol Med 58, 1230–1241 (2026). https://doi.org/10.1038/s12276-026-01684-5
Trefwoorden: Ziekte van Alzheimer, hersensignalen, receptorroutes, hersenen-organoïden, biomarkers