Clear Sky Science · pl
Mózgi ludzkie i transkryptomy organoidów ujawniają kluczowe szlaki kinaz receptorowych tyrozyny i sygnatury genetyczne w chorobie Alzheimera
Dlaczego to ma znaczenie dla zrozumienia Alzheimera
Choroba Alzheimera jest zwykle opisywana przez pryzmat lepko przylegających płyt i splątanych białek w mózgu. Jednak za tymi widocznymi zmianami kryje się cichsza opowieść zapisana w genach i sygnałach międzykomórkowych. Niniejsze badanie zagląda pod maskę ludzkiego mózgu i hodowanych w laboratorium „mini-mózgów”, aby ustalić, które przełączniki sygnalizacyjne w komórkach mózgowych są najbardziej zaburzone w Alzheimerze i czy mogą pomóc we wcześniejszym wykrywaniu lub leczeniu choroby.
Poszukiwanie ukrytych sygnałów w wrażliwym obszarze mózgu
Naukowcy skupili się na zakręcie skroniowym środkowym, obszarze mózgu ważnym dla mowy i pamięci, który ulega wczesnemu uszkodzeniu w chorobie Alzheimera. Przeanalizowali aktywność genów w setkach tysięcy odczytów z tkanki mózgowej pochodzącej od osób z Alzheimerem i bez choroby. Porównując dwa duże publiczne zbiory danych ze Stanów Zjednoczonych i Europy, wyodrębnili 145 genów, które były konsekwentnie zmienione w mózgach chorych na Alzheimera. Wiele z tych genów skupiało się wokół rodziny cząsteczek powierzchniowych zwanych receptorami, które działają jak anteny pozwalające komórkom mózgowym wyczuwać i reagować na otoczenie.
Receptorowe „anteny” i krótka lista podejrzanych genów
Bliższe analizy z użyciem kilku internetowych baz biologicznych pozwoliły przypisać 145 genów do konkretnych szlaków. Wyraźny sygnał pochodził od receptorów kinaz tyrozynowych, grupy receptorów kontrolujących przeżywalność, wzrost i komunikację komórek. Z tej grupy wyselekcjonowano 18 genów powiązanych z tymi szlakami, a następnie stworzono mapę interakcji, która objęła także dobrze znane geny Alzheimera związane z amyloidem i tau. Analiza sieci uwypukliła sześć genów znajdujących się w kluczowych punktach skrzyżowań: AXL i ITGB1 (oba zaangażowane w sposób, w jaki komórki odczuwają otoczenie), GFAP (marker astrocytów), CAV1 i RHOA (wpływające na kształt i sygnalizację komórek) oraz NRG1 (ważny dla rozwoju mózgu). W mózgach osób z Alzheimerem pięć z tych genów było nadekspresjonowanych, natomiast NRG1 wykazywał obniżoną ekspresję.
Weryfikacja wyników w mini-mózgach i neuronach
Aby wyjść poza analizy komputerowe, badacze wykorzystali pochodzące od ludzkich komórek macierzystych organoidy mózgowe — trójwymiarowe „mini-mózgi”, zawierające neurony i komórki wspierające — oraz pierwotne neurony szczura hodowane w hodowlach. Ekspozycja organoidów na amyloid‑beta, toksyczne białko związane z płytkami, spowodowała wzrost poziomów kilku kluczowych genów, w tym AXL i ITGB1. Badania białek wykazały, że AXL zwiększył się wewnątrz organoidów, a ITGB1 wzrósł szczególnie w błonie komórkowej, gdzie może wpływać na przyczepność i sygnalizację międzykomórkową. Jednocześnie silniej aktywował się główny szlak wewnętrznej sygnalizacji zwany PI3K–AKT, co sugeruje, że amyloid może napędzać konkretną gałąź sygnalizacji receptorowej, a nie wyłącznie wywoływać ogólny stres komórkowy.
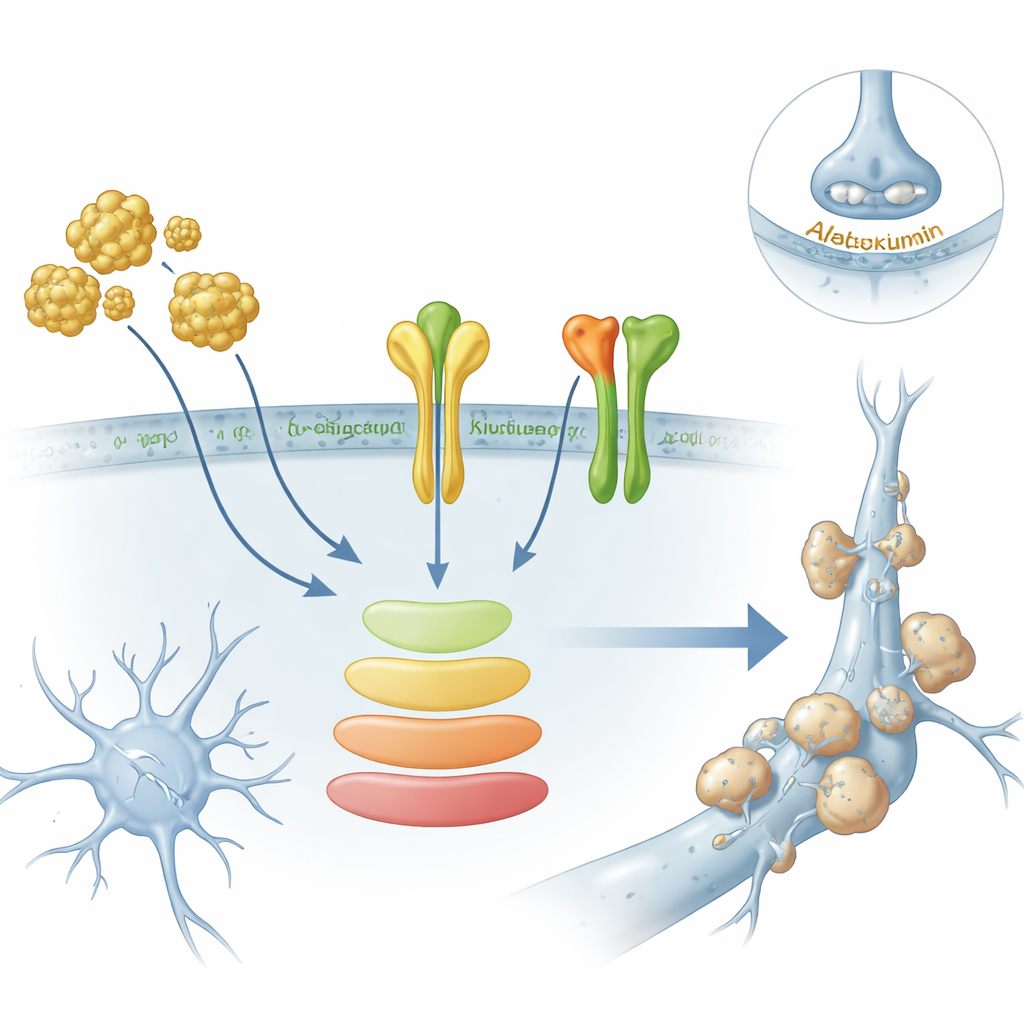
Od wzorców genowych do potencjalnych biomarkerów
Następnie zespół sprawdził, czy łączna aktywność sześciu wyróżnionych genów może rozróżniać mózgi z Alzheimerem od mózgów o prawidłowej funkcji poznawczej. Przy użyciu modeli statystycznych okazało się, że wynik oparty na tych sześciu genach z dużą dokładnością oddzielał obie grupy w obu kohortach mózgowych. Wyższe wartości tego wskaźnika korelowały również z cięższymi ocenami demencji klinicznej. To sugeruje, że wzorce aktywności genów związanych z receptorami, szczególnie dotyczące AXL i ITGB1, mogą stanowić molekularny odcisk zmian związanych z Alzheimerem w zakręcie skroniowym środkowym, a być może także w innych wrażliwych obszarach, takich jak hipokamp.
Co to może znaczyć dla przyszłej diagnostyki i leczenia
Podsumowując, badanie proponuje, że określone szlaki receptorowe, skoncentrowane wokół receptora AXL i integryny ITGB1, ulegają nadaktywacji w warunkach przypominających Alzheimera i włączają pętlę sygnałową, która może pogarszać chorobę. Choć potrzeba jeszcze wielu badań — zwłaszcza eksperymentów, które bezpośrednio włączają lub wyłączają te geny w żywych systemach — wyniki wskazują na nową warstwę biologii Alzheimera wykraczającą poza płytki i splątki. W dłuższej perspektywie mierzenie tych zmian genowych i białkowych albo bezpieczne stłumienie nadaktywnych szlaków receptorowych mogłoby uzupełniać istniejące podejścia do diagnozy i leczenia choroby Alzheimera.
Cytowanie: Shin, S., Zhu, X., Amartumur, S. et al. Human brain and organoid transcriptomes reveal key receptor tyrosine kinase pathways and genetic signatures in Alzheimer's disease. Exp Mol Med 58, 1230–1241 (2026). https://doi.org/10.1038/s12276-026-01684-5
Słowa kluczowe: choroba Alzheimera, sygnalizacja mózgowa, szlaki receptorowe, organoidy mózgowe, biomarkery