Clear Sky Science · pl
Niedobór MCT4 hamuje występowanie nowotworów i przerzuty poprzez obniżenie ekspresji IGF1 i wzmocnienie odporności przeciwnowotworowej
Dlaczego to badanie nad rakiem ma znaczenie
Komórki nowotworowe przebudowują sposób wykorzystania energii, a ta metaboliczna przemiana nie tylko napędza guzy, lecz także pomaga im ukrywać się przed układem odpornościowym. W pracy skoncentrowano się na jednym białku transportowym, MCT4, które wypompowuje produkt odpadowy — mleczan — z szybko dzielących się komórek. Tworząc myszy całkowicie pozbawione MCT4, badacze stawiają proste, lecz istotne pytanie: jeśli wyłączymy ten metaboliczny zawór, czy guzy rosną wolniej i stają się łatwiejszym celem dla układu odpornościowego?
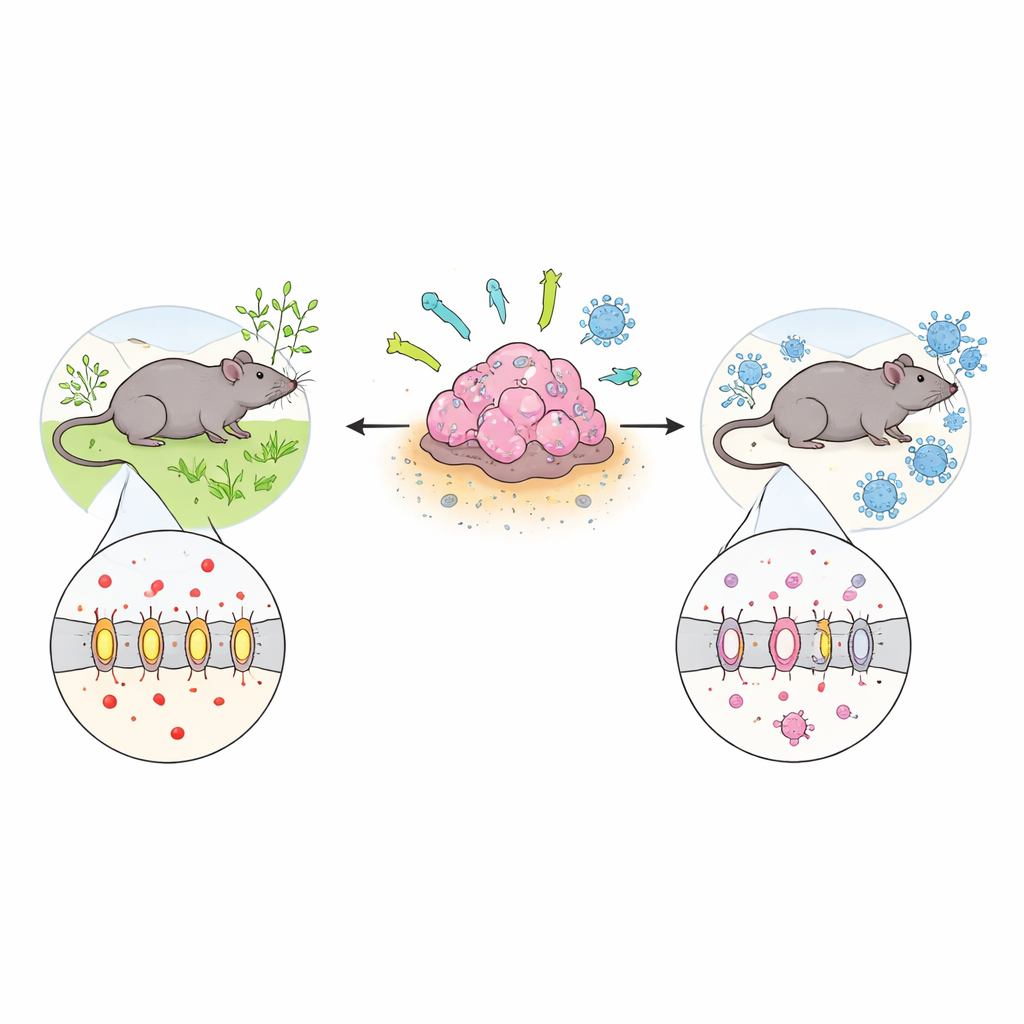
Skrót energetyczny wykorzystywany przez guzy
Większość zdrowych komórek w obecności tlenu wytwarza energię wydajnie. W przeciwieństwie do nich komórki o wysokiej aktywności — w tym wiele komórek nowotworowych — wolą szybszą, lecz „bardziej chaotyczną” ścieżkę zwaną glikolizą, która produkuje duże ilości mleczanu. Aby uniknąć zakwaszenia wnętrza komórki, komórki nowotworowe polegają na transporterach, takich jak MCT4, które wypompowują mleczan do otaczających tkanek. W tkankach prawidłowych MCT4 występuje głównie w komórkach wykonujących duży wysiłek, np. w mięśniach szkieletowych, jednak analiza dużych baz danych nowotworowych wykazała, że wiele typów nowotworów — w tym piersi, płuca, mózgu oraz głowy i szyi — wykazuje silną ekspresję MCT4. Pacjenci, których guzy mają więcej MCT4, zwykle przeżywają krócej, co sugeruje, że ten transporter nie jest jedynie „pasażerem”, lecz aktywnie napędza agresywny przebieg choroby.
Tworzenie myszy bez „zaworu” mleczanowego
Aby bezpośrednio zbadać rolę MCT4, zespół użył narzędzi edycji genów do wygenerowania myszy BALB/c, w których gen MCT4 został całkowicie usunięty. Zwierzęta te były ogólnie zdrowe, choć nieco mniejsze i miały nieznacznie podwyższony poziom cukru we krwi, co sugeruje, że MCT4 wpływa także na metabolizm całego organizmu. Po przeszczepieniu komórek raka piersi (4T1) lub raka płuca (M109) do tych myszy, guzy rosły około 40 procent wolniej niż u myszy normalnych i tworzyły mniej przerzutów do płuc. Próbki guzów od myszy kontrolnych zwiększały poziom białka MCT4 podczas wzrostu, natomiast guzy u myszy z delecją utrzymywały niski poziom MCT4. W wielu modelach chemicznego wywoływania raka — dla piersi, płuc i jamy ustnej — myszy pozbawione MCT4 konsekwentnie rozwijały mniej, mniejsze i mniej inwazyjne ogniska nowotworowe.
Sygnały wzrostu i mikrośrodowisko guza
Pogłębiając analizę, badacze zmierzyli poziomy insulinopodobnego czynnika wzrostu 1 (IGF1), hormonu sprzyjającego wzrostowi i przeżyciu komórek. U zdrowych myszy bez MCT4 stężenie IGF1 we krwi było o około 45 procent niższe niż u zwierząt normalnych, a zarówno IGF1, jak i mleczan były wyraźnie zredukowane w płynie otaczającym guzy. Gdy badacze dostarczyli dodatkowy IGF1 lub mleczan myszom z delecją, wzrost guzów częściowo się odnowił, co wskazuje, że MCT4 wspiera nowotwór nie tylko poprzez usuwanie mleczanu, lecz także przez wzmacnianie sygnałów wzrostowych zależnych od IGF1. Jednak efekt „uratowania” był niepełny, co sugeruje udział innych ścieżek.
Przywrócenie ataku odpornościowego
Badanie zwróciło się następnie ku układowi odpornościowemu, który nieustannie patroluje tkanki w poszukiwaniu nieprawidłowych komórek. W warunkach wyjściowych liczba komórek odpornościowych we krwi była podobna u myszy normalnych i pozbawionych MCT4. Jednak po pojawieniu się guzów różnice stały się wyraźne. Myszy bez MCT4 miały więcej komórek T pomocniczych, cytotoksycznych komórek T, komórek NK i makrofagów zarówno we krwi, jak i w guzach. Ich makrofagi przeszły z korzystnego dla guza, „gojącego” stanu (często określanego jako M2) w kierunku bardziej zapalnego, przeciwnowotworowego stanu (M1). Zespół powiązał aktywność MCT4 z wyższymi poziomami cząsteczki sygnałowej CCL28, która przyciąga immunosupresyjne komórki pochodzenia szpikowego. Myszy z delecją wykazywały niższe stężenie CCL28 we krwi i płynie guza oraz mniejszą liczbę tych komórek tłumiących, co sprzyjało przechyleniu równowagi w stronę skutecznej odpowiedzi immunologicznej.
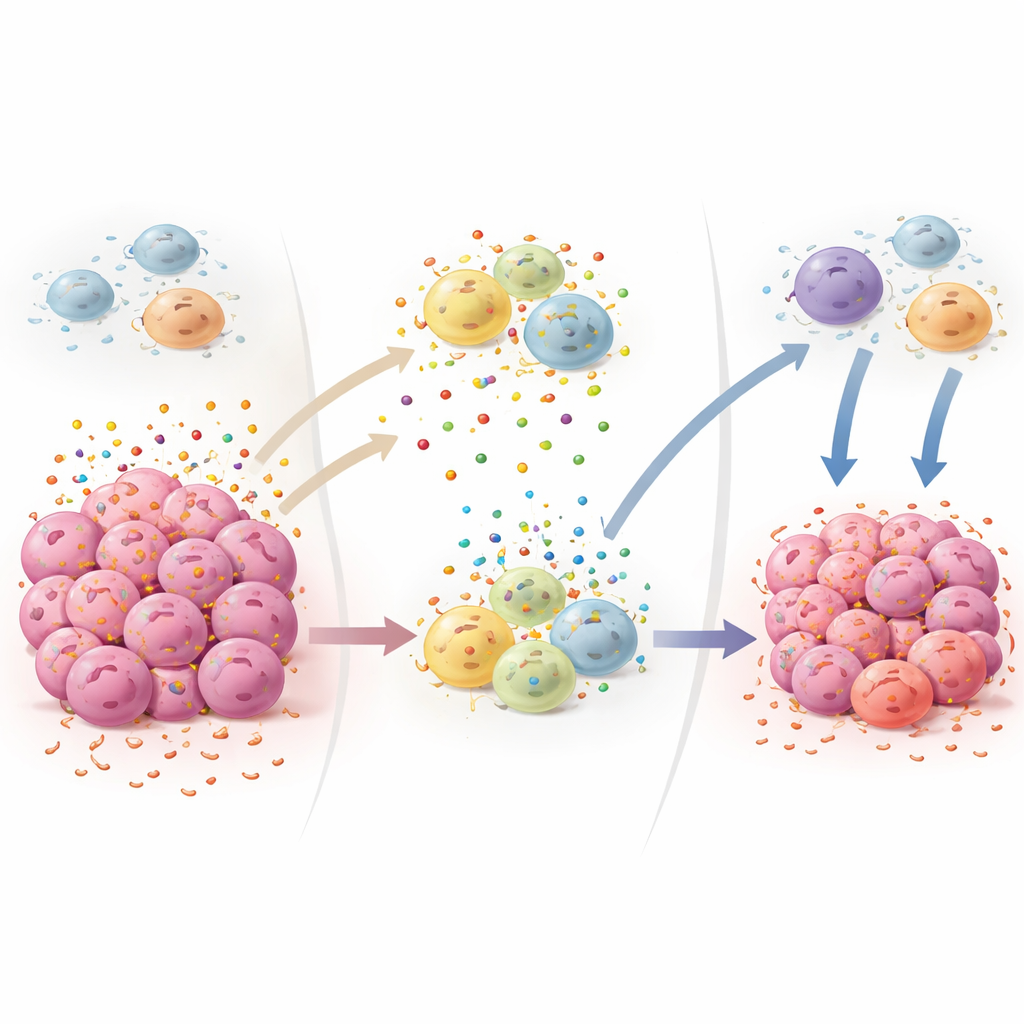
Szerszy obraz dla przyszłych terapii przeciwnowotworowych
Podsumowując, wyniki stawiają MCT4 jako centralny przełącznik łączący trzy cechy charakterystyczne nowotworów: zmieniony metabolizm, nadmierne sygnalizowanie wzrostu i miejscowe tłumienie odporności. Usunięcie tego transportera u myszy obniża poziom IGF1 sprzyjającego wzrostowi, redukuje nagromadzenie mleczanu, uniemożliwia rekrutację komórek immunosupresyjnych i pozwala ochronnym komórkom T oraz komórkom NK skuteczniej penetrować guzy. Ponieważ myszy bez MCT4 prowadzą normalne życie przy jedynie łagodnych zmianach metabolicznych, badanie sugeruje, że starannie zaprojektowane leki blokujące MCT4 mogłyby jednocześnie spowalniać wzrost guzów i wzmacniać naturalne mechanizmy obronne organizmu, potencjalnie uzupełniając istniejące immunoterapie.
Cytowanie: Wang, S., Guo, H., Feng, L. et al. MCT4 deficiency suppresses tumor incidence and metastasis by downregulating IGF1 expression and enhancing anti-tumor immunity. Commun Biol 9, 539 (2026). https://doi.org/10.1038/s42003-026-10002-8
Słowa kluczowe: metabolizm nowotworów, odporność przeciwnowotworowa, transporter mleczanowy, sygnalizacja IGF1, inhibicja MCT4