Clear Sky Science · nl
MCT4‑tekort vermindert tumorincidentie en metastase door IGF1‑expressie te verlagen en anti‑tumorimmuniteit te versterken
Waarom deze kankerstudie ertoe doet
Kankercellen herschikken hun energiegebruik, en die metabole ommekeer voedt niet alleen tumoren maar kan ze ook helpen zich aan het immuunsysteem te onttrekken. Deze studie richt zich op één transporteiwit, MCT4, dat het afvalproduct lactaat uit snelgroeiende cellen pompt. Door muizen te creëren die volledig MCT4 missen, stellen de onderzoekers een eenvoudige maar krachtige vraag: als we deze metabole klep uitzetten, groeien tumoren dan langzamer en worden ze makkelijker door het immuunsysteem aangevallen?
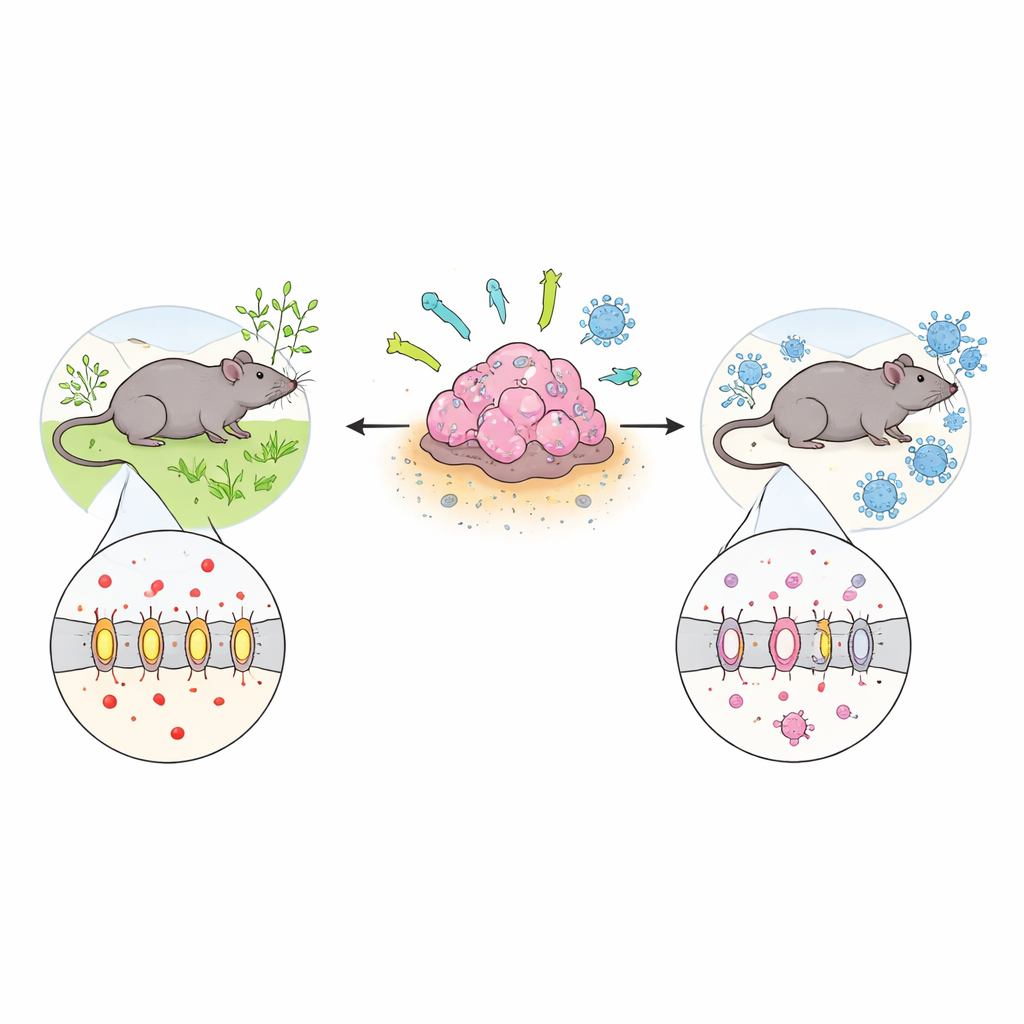
De energieweg die tumoren uitbuiten
De meeste gezonde cellen maken energie efficiënt in aanwezigheid van zuurstof. Daarentegen geven zeer actieve cellen – waaronder veel kankercellen – de voorkeur aan een snellere maar „rommeligere” route genaamd glycolyse, die grote hoeveelheden lactaat produceert. Om interne verzuring te voorkomen vertrouwen tumorcellen op transporters zoals MCT4 om lactaat naar het omliggende weefsel te pompen. In normale weefsels komt MCT4 vooral voor in hardwerkende cellen zoals skeletspier, maar analyse van grote kankerdatabanken toonde aan dat veel tumortypen, waaronder borst-, long-, hersen‑ en hoofd‑en‑halskankers, MCT4 op hoge niveaus inschakelen. Patiënten wiens tumoren meer MCT4 hebben, blijken slechtere overlevingskansen te hebben, wat suggereert dat deze transporter geen passagier is maar een actieve bestuurder van agressieve ziekte.
Muizen zonder de lactaatklep maken
Om de rol van MCT4 direct te onderzoeken, gebruikte het team genbewerkingstools om BALB/c‑muizen te genereren waarin het MCT4‑gen volledig is verwijderd. Deze dieren waren over het algemeen gezond, maar iets kleiner en hadden licht verhoogde bloedglucose, wat erop wijst dat MCT4 ook de stofwisseling van het hele organisme beïnvloedt. Wanneer borstkankercellen (4T1) of longkankercellen (M109) in deze muizen werden getransplanteerd, groeiden tumoren ongeveer 40 procent langzamer dan bij normale muizen en vormden ze minder longmetastasen. Tumorvlees van normale muizen verhoogde MCT4‑eiwit tijdens groei, terwijl tumoren in knockout‑muizen MCT4 laag hielden. In meerdere chemische kankeriniteringsmodellen – voor borst-, long‑ en mondkanker – ontwikkelden MCT4‑deficiënte muizen consequent minder, kleinere en minder invasieve laesies.
Groei‑signalen en de tumoromgeving
Dieper graven, maten de onderzoekers niveaus van insulinelike groeifactor 1 (IGF1), een hormoon dat celgroei en overleving bevordert. In gezonde MCT4‑knockoutmuizen was IGF1 in het bloed ongeveer 45 procent lager dan in normale dieren, en zowel IGF1 als lactaat waren sterk verminderd in de vloeistof rondom tumoren. Toen de onderzoekers extra IGF1 of lactaat toedienden aan de knockoutmuizen, herstelde de tumorgroei gedeeltelijk, wat aangeeft dat MCT4 kanker ondersteunt niet alleen door lactaat te verwerken maar ook door IGF1‑gedreven groeisignalen te versterken. De rescue was echter onvolledig, wat suggereert dat ook andere routes betrokken zijn.
Het immuunaanval heractiveren
De studie wendde zich vervolgens tot het immuunsysteem, dat weefsels voortdurend patrouilleert op afwijkende cellen. Onder basisomstandigheden leken de aantallen immuuncellen in het bloed vergelijkbaar bij normale en MCT4‑deficiënte muizen. Maar zodra tumoren aanwezig waren, werden de verschillen duidelijk. Muizen zonder MCT4 hadden meer helper‑T‑cellen, cytotoxische T‑cellen, natural killer‑cellen en macrofagen zowel in het bloed als binnen tumoren. Hun macrofagen verschoven van een tumorvriendelijke, wondhelende toestand (vaak M2 genoemd) naar een meer inflammatoire, tumorbestrijdende toestand (M1). Het team koppelde MCT4‑activiteit aan hogere niveaus van het signaalmolecuul CCL28, dat immuunsuppressieve myeloïde‑afgeleide onderdrukkende cellen aantrekt. Knockoutmuizen vertoonden lagere CCL28 in bloed en tumorvloeistof en minder van deze onderdrukkende cellen, wat hielp het evenwicht te verschuiven naar een effectieve immuunrespons.
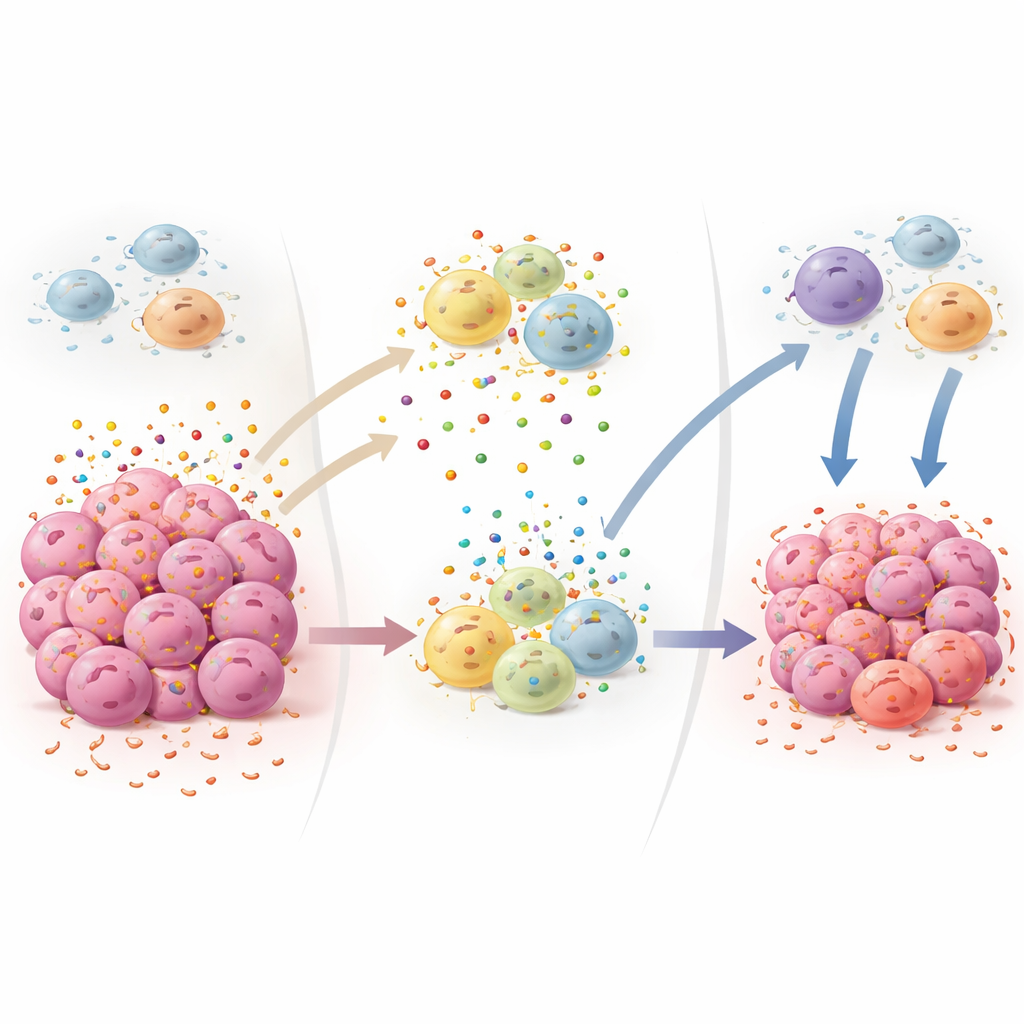
Het grote plaatje voor toekomstige kankertherapieën
Alles bij elkaar plaatsen de bevindingen MCT4 als een centraal schakelpunt dat drie kenmerken van kanker verbindt: veranderde stofwisseling, ongecontroleerde groeisignalen en lokale immuunsuppressie. Het verwijderen van deze transporter bij muizen verlaagt groeibevorderend IGF1, vermindert lactaatopbouw, blokkeert de aanvoer van onderdrukkende immuuncellen en maakt het mogelijk dat beschermende T‑cellen en natural killer‑cellen tumoren effectiever binnendringen. Omdat muizen zonder MCT4 een normaal leven leiden met slechts milde metabolische veranderingen, suggereert het werk dat zorgvuldig ontworpen MCT4‑blokkerende geneesmiddelen een manier zouden kunnen bieden om tumorgroei te vertragen en tegelijkertijd de eigen antitumorafweer van het lichaam te versterken, mogelijk ter aanvulling op bestaande immunotherapieën.
Bronvermelding: Wang, S., Guo, H., Feng, L. et al. MCT4 deficiency suppresses tumor incidence and metastasis by downregulating IGF1 expression and enhancing anti-tumor immunity. Commun Biol 9, 539 (2026). https://doi.org/10.1038/s42003-026-10002-8
Trefwoorden: kankermetabolisme, tumorimmuniteit, lactaattransporteur, IGF1‑signalering, MCT4‑remming