Clear Sky Science · de
MCT4-Mangel verringert Tumorentstehung und Metastasenbildung durch Herunterregulierung von IGF1-Expression und Verstärkung der Anti-Tumor-Immunität
Warum diese Krebsstudie wichtig ist
Krebszellen verändern, wie sie Energie nutzen; diese metabolische Umbildung treibt Tumoren nicht nur an, sondern kann ihnen auch helfen, sich vor dem Immunsystem zu verbergen. Diese Studie konzentriert sich auf ein einzelnes Transportprotein, MCT4, das das Abfallprodukt Laktat aus schnell wachsenden Zellen pumpt. Indem die Forschenden Mäuse erzeugten, die vollständig ohne MCT4 auskommen, stellen sie eine einfache, aber kraftvolle Frage: Wenn wir dieses metabolische Ventil abschalten, wachsen Tumoren dann langsamer und werden sie für das Immunsystem angreifbarer?
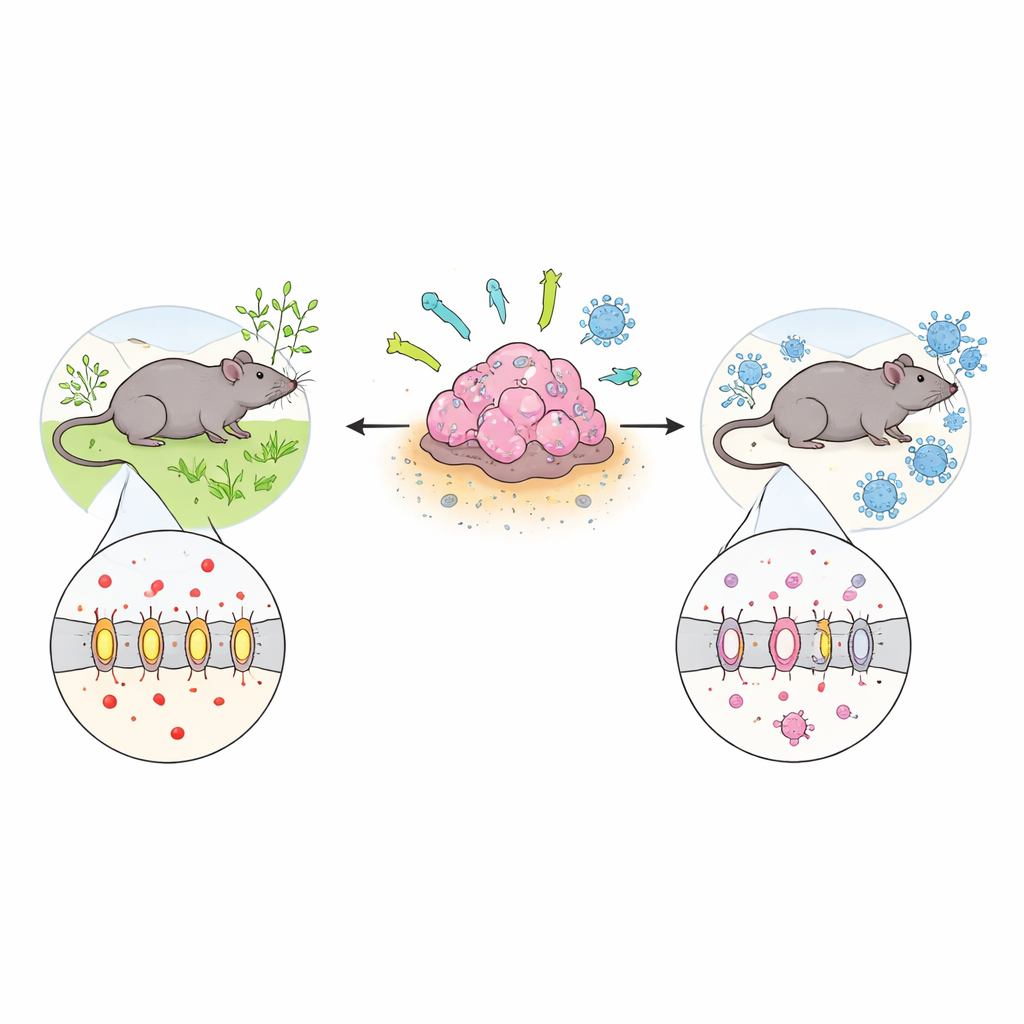
Die Energie-Abkürzung, die Tumoren ausnutzen
Die meisten gesunden Zellen erzeugen Energie in Gegenwart von Sauerstoff effizient. Im Gegensatz dazu bevorzugen hochaktive Zellen – darunter viele Krebszellen – einen schnelleren, aber „schmutzigeren“ Weg namens Glykolyse, der große Mengen Laktat produziert. Um eine innere Ansäuerung zu vermeiden, verlassen sich Tumorzellen auf Transporter wie MCT4, um Laktat ins umliegende Gewebe zu pumpen. In normalen Geweben findet sich MCT4 vor allem in leistungsfähigen Zellen wie Skelettmuskel; die Analyse großer Krebsdatenbanken zeigte jedoch, dass viele Tumortypen, darunter Brust-, Lungen-, Hirn- und Kopf-Hals-Karzinome, MCT4 in hoher Menge anschalten. Patientinnen und Patienten, deren Tumoren mehr MCT4 aufweisen, haben tendenziell eine schlechtere Überlebensprognose, was darauf hindeutet, dass dieser Transporter nicht nur ein Beiwerk, sondern ein aktiver Treiber aggressiver Erkrankung ist.
Mäuse ohne Laktatventil erzeugen
Um die Rolle von MCT4 direkt zu untersuchen, nutzte das Team Gen-Editing-Werkzeuge, um BALB/c-Mäuse zu erzeugen, bei denen das MCT4-Gen vollständig entfernt ist. Diese Tiere waren insgesamt gesund, jedoch etwas kleiner und mit mäßig erhöhtem Blutzucker, was andeutet, dass MCT4 auch den Gesamtstoffwechsel beeinflusst. Wurden Brustkrebszellen (4T1) oder Lungenkrebszellen (M109) in diese Mäuse transplantiert, wuchsen die Tumoren etwa 40 Prozent langsamer als in normalen Mäusen und bildeten weniger Lungenmetastasen. Tumorproben aus normalen Mäusen erhöhten während des Wachstums die MCT4-Proteinmenge, während Tumoren in Knockout-Mäusen MCT4 niedrig hielten. Über mehrere chemische Krebsinduktionsmodelle hinweg – für Brust-, Lungen- und Mundhöhlenkrebs – entwickelten MCT4-defiziente Mäuse konsistent weniger, kleinere und weniger invasive Läsionen.
Wachstums-signale und die Tumorumgebung
Tiefer gehend maßen die Forschenden Werte des insulinähnlichen Wachstumsfaktors 1 (IGF1), eines Hormons, das Zellwachstum und -überleben fördert. Bei gesunden MCT4-Knockout-Mäusen war IGF1 im Blut etwa 45 Prozent niedriger als bei normalen Tieren, und sowohl IGF1 als auch Laktat waren in der Flüssigkeit rund um Tumoren deutlich reduziert. Als die Forschenden den Knockout-Mäusen zusätzliches IGF1 oder Laktat zuführten, kehrte das Tumorwachstum teilweise zurück, was darauf hinweist, dass MCT4 Krebs nicht nur durch Laktathandhabung unterstützt, sondern auch durch die Verstärkung von IGF1-getriebenen Wachstumssignalen. Die teilweise Rückkehr deutet jedoch darauf hin, dass weitere Pfade beteiligt sind.
Die Immunattacke wieder wecken
Die Studie wandte sich dann dem Immunsystem zu, das kontinuierlich Gewebe auf abnorme Zellen überwacht. Unter Basisbedingungen waren die Immunzellzahlen im Blut bei normalen und MCT4-defizienten Mäusen ähnlich. Sobald Tumoren jedoch vorhanden waren, wurden die Unterschiede deutlich. Mäuse ohne MCT4 hatten mehr Helfer-T-Zellen, Killer-T-Zellen, natürliche Killerzellen und Makrophagen sowohl im Blut als auch in den Tumoren. Ihre Makrophagen verschoben sich von einem tumorfördernden, wundheilungsähnlichen Zustand (oft M2 genannt) hin zu einem stärker entzündlichen, tumorbekämpfenden Zustand (M1). Das Team verknüpfte MCT4-Aktivität mit höheren Spiegeln des Signalmoleküls CCL28, das immunsuppressive myeloische Suppressor-Zellen anzieht. Knockout-Mäuse zeigten niedrigere CCL28-Werte im Blut und in der Tumorflüssigkeit und weniger dieser suppressiven Zellen, was dazu beitrug, das Gleichgewicht zugunsten einer effektiven Immunantwort zu verschieben.
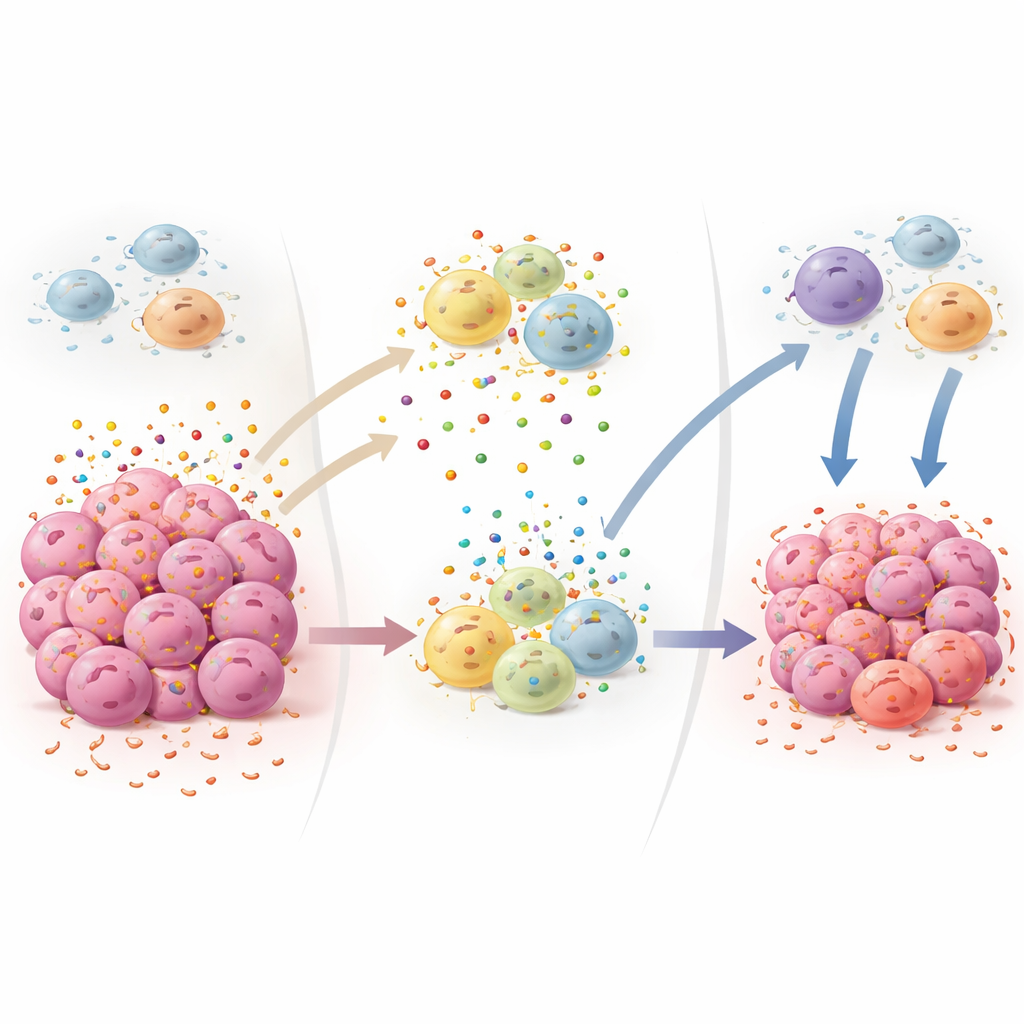
Das große Bild für künftige Krebstherapien
Insgesamt positionieren die Befunde MCT4 als zentralen Schalter, der drei Kennzeichen von Krebs verbindet: veränderter Stoffwechsel, enthemmte Wachstumssignale und lokale Immunsuppression. Das Entfernen dieses Transporters bei Mäusen senkt das wachstumsfördernde IGF1, reduziert Laktatanhäufung, unterbindet die Rekrutierung suppressiver Immunzellen und erlaubt schützenden T‑Zellen sowie natürlichen Killerzellen, Tumoren effektiver zu infiltrieren. Da Mäuse ohne MCT4 mit nur milden metabolischen Veränderungen normal leben, legt die Arbeit nahe, dass sorgfältig entwickelte MCT4-blockierende Medikamente einen Weg bieten könnten, Tumorwachstum zu verlangsamen und zugleich die körpereigene Anti-Tumor-Abwehr zu stärken – möglicherweise als Ergänzung zu bestehenden Immuntherapien.
Zitation: Wang, S., Guo, H., Feng, L. et al. MCT4 deficiency suppresses tumor incidence and metastasis by downregulating IGF1 expression and enhancing anti-tumor immunity. Commun Biol 9, 539 (2026). https://doi.org/10.1038/s42003-026-10002-8
Schlüsselwörter: Krebsstoffwechsel, Tumorimmunität, Laktattransporter, IGF1-Signalgebung, MCT4-Inhibition