Clear Sky Science · he
חסרון MCT4 מדכא תחלואה גרורתית וגידול גידולים על ידי דיכוי ביטוי IGF1 וחיזוק החיסון נגד הגידול
מדוע המחקר הזה על סרטן חשוב
תאי סרטן משנים את האופן שבו הם מנצלים אנרגיה, ומהפך מטבולי זה לא רק מזין את הגידולים אלא גם יכול לסייע להם להתחמק ממערכת החיסון. המחקר מתמקד בחלבון נשא יחיד, MCT4, המייצא את תוצר הפסולת לקטט מתאים שמתחלקים במהירות. על‑ידי יצירת עכברים החסרים לחלוטין את MCT4, החוקרים שואלים שאלה פשוטה אך משמעותית: אם נסגור את שבר ההסדרה המטבולי הזה, האם הגידולים יגדלו לאט יותר ויהיו קלים יותר להתקפה על‑ידי מערכת החיסון?
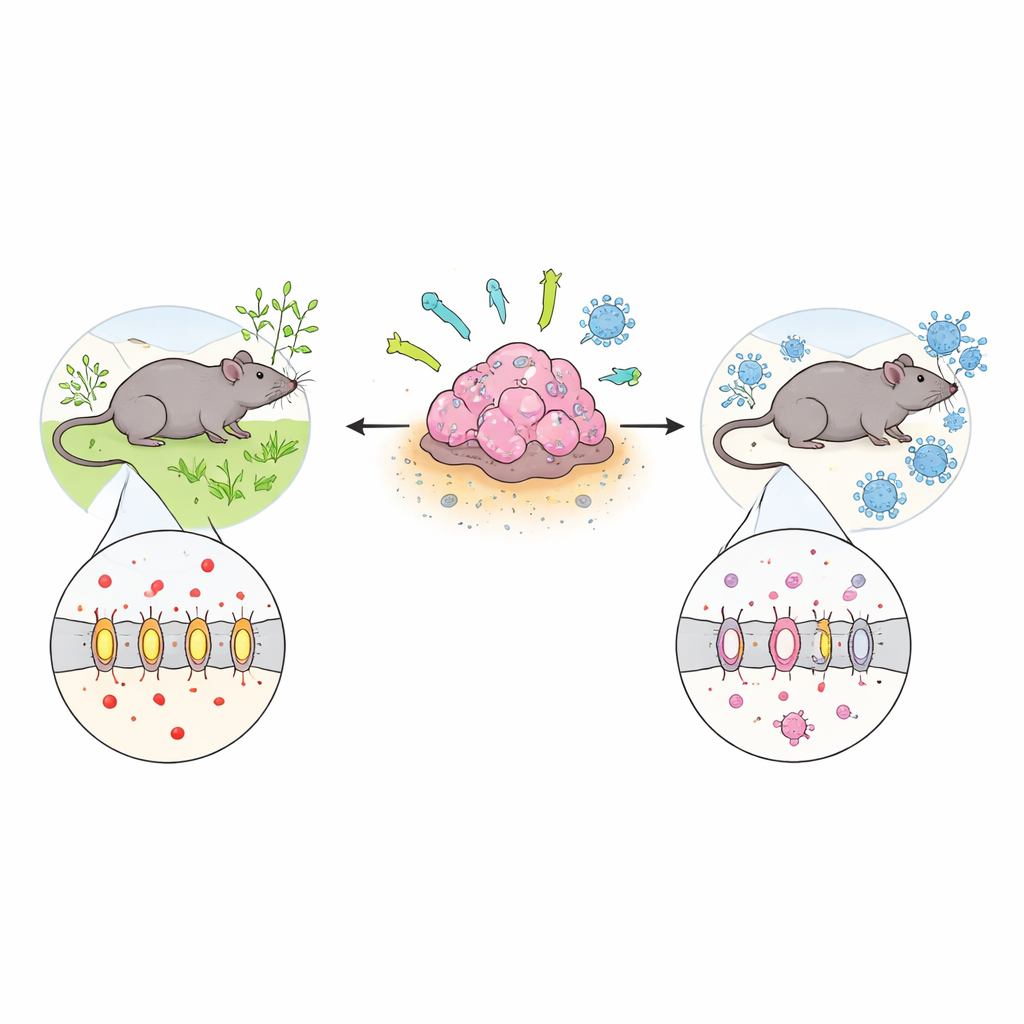
הקיצור האנרגטי שגידולים מנצלים
רוב התאים הבריאים מייצרים אנרגיה ביעילות בנוכחות חמצן. לעומת זאת, תאים בעלי פעילות גבוהה — ובכללם תאים סרטניים רבים — מעדיפים מסלול מהיר יותר אך "מסורבל" יותר הנקרא גליקוליזה, שמייצר כמויות גדולות של לקטט. כדי למנוע הצטברות חומציות פנימית, תאי גידול נשענים על נשאים כמו MCT4 כדי לפנות את הלקטט לרקמה הסובבת. ברקמות תקינות MCT4 נמצא בעיקר בתאים העובדים קשה כגון שריר שלד, אך ניתוח מאגרי נתונים גדולים על סרטן הראה שסוגי גידול רבים — כולל שד, ריאות, מוח וראש‑צוואר — מבטאים MCT4 ברמות גבוהות. מטופלים שלגידוליהם יש יותר MCT4 נוטים להישרדות גרועה יותר, מה שמרמז שהנשא אינו רק נוסע, אלא גורם פעיל בהתנהגות תוקפנית של המחלה.
בניית עכברים בלי שסתום הלקטט
כדי לבחון ישירות את תפקידה של MCT4, הקבוצה השתמשה בכלי עריכת גנים ליצירת עכברי BALB/c שבהם גן MCT4 נמחק לחלוטין. בעלי החיים הללו היו בריאים באופן כללי, אך מעט קטנים יותר והיו להם רמות סוכר בדם מעט גבוהות יותר, מרמז ש‑MCT4 משפיע גם על מטבוליזם של הגוף כולו. כאשר תאי סרטן שד (4T1) או ריאות (M109) הושתלו בעכברים הללו, הגידולים גדלו בכ‑כ־40% יותר לאט מאשר בעכברים רגילים והشكل פחות גרורות בריאות. דגימות גידול מעכברים רגילים העלו את רמת חלבון MCT4 במהלך הגדילה, בעוד הגידולים בעכברי הנוקאאוט שמרו על רמת MCT4 נמוכה. במספר מודלים כימיים להשריית סרטן — לשד, לריאה ולפה — עכברי חסרי MCT4 פיתחו בעקביות פחות אירועים של גידולים, קטנים יותר ופחות חודרניים.
אותות גדילה והשכונה של הגידול
בחינה מעמיקה יותר מדדה החוקרים רמות של גורם דמוי אינסולין 1 (IGF1), הורמון המעודד גדילה ותמותה של תאים. בעכברי MCT4‑נוקאאוט הבריאים, IGF1 בדם היה נמוך בכ‑כ־45% לעומת בעלי החיים הרגילים, וגם IGF1 ולקטט הופחתו באופן בולט בנוזל שסביב הגידולים. כאשר החוקרים סיפקו IGF1 או לקטט נוספים לעכברי הנוקאאוט, גדילת הגידול החזירה חלקית את עצמה, מה שמצביע על כך ש‑MCT4 תומך בסרטן לא רק על ידי פינוי לקטט אלא גם על ידי חיזוק אותות הגדילה המונעים מ‑IGF1. עם זאת, ההחזרה לא היתה מלאה, מה שמרמז שמעורבות גם מסלולים נוספים.
הפעלת התקפת מערכת החיסון מחדש
המחקר פנה אז למערכת החיסון, אשר עובדת כל הזמן בסריקות ברקמות לאיתור תאים בלתי תקינים. בתנאים בסיסיים, מספר תאי מערכת החיסון בדם נראה דומה בעכברים רגילים ובעכברים חסרי MCT4. אך ברגע שהגידולים הופיעו, ההבדלים הפכו בולטים. בעכברים החסרים MCT4 נצפו יותר תאי T מסייעים, תאי T קטלניים, תאי הרג טבעי ותא־מאקרופאגים הן בדם והן בתוך הגידולים. המאקרופאגים שלהם הזזו ממצב ידידותי לגידול ומרפא פצעים (מוכר כמצב M2) לכיוון מצב דלקתי יותר ונלחם בגידול (M1). הקבוצה קישרה את פעילות MCT4 לרמות גבוהות של מולקולת האיתות CCL28, שמושכת תאי מדכאים ממקור מיואידי. בעכברי הנוקאאוט נרשמה רמה נמוכה יותר של CCL28 בדם ובנוזל הגידול ופחות מתאי המדכאים הללו, מה שעוזר לנטות את המאזן לעבר תגובה חיסונית יעילה.
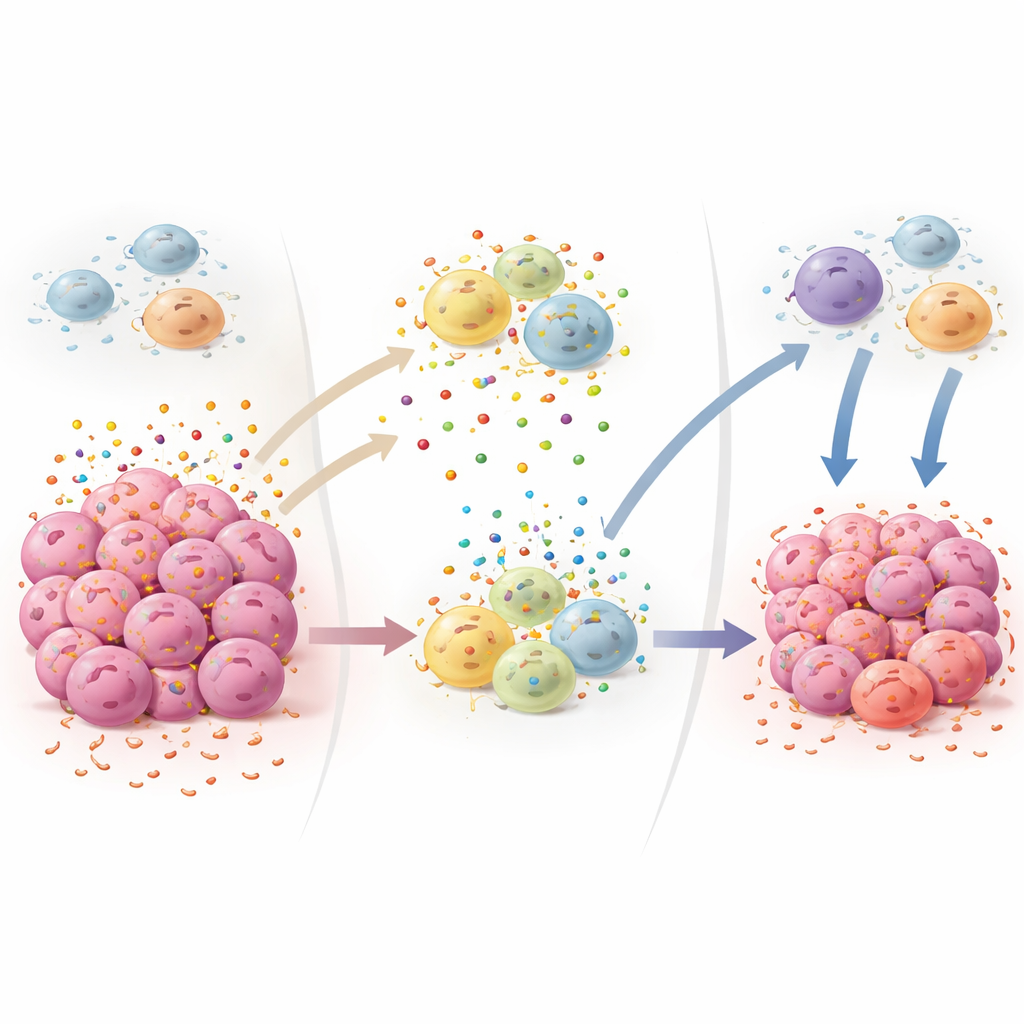
התמונה הגדולה עבור טיפולי סרטן עתידיים
באופן מצטבר, הממצאים מציבים את MCT4 כמפתח מרכזי המחבר בין שלושה סימני דרך של סרטן: מטבוליזם משתנה, איתותי גדילה בלתי נשלטים ודיכוי חיסוני מקומי. הסרת הנשאי בעכברים מורידה את IGF1 המעודד גדילה, מצמצמת הצטברות לקטט, חותכת גיוס של תאי חיסון מדכאים, ומאפשרת לתאי T ומקרי הרג טבעיים לחדור לגידולים ביעילות רבה יותר. מכיוון שעכברים ללא MCT4 חיים חיים תקינים עם שינויים מטבוליים מתונים בלבד, העבודה מצביעה על כך שתרופות חוסמות‑MCT4 שעוצבו בקפידה יכולות להציע דרך להאט את גדילת הגידול ולהגביר במקביל את ההגנה החיסונית של הגוף נגד הגידול, ובכך לשלב פוטנציאלית עם אימונותרפיות קיימות.
ציטוט: Wang, S., Guo, H., Feng, L. et al. MCT4 deficiency suppresses tumor incidence and metastasis by downregulating IGF1 expression and enhancing anti-tumor immunity. Commun Biol 9, 539 (2026). https://doi.org/10.1038/s42003-026-10002-8
מילות מפתח: מטבוליזם של סרטן, חיסון נגד גידול, מוביל לקטט, איתות IGF1, עיכוב MCT4