Clear Sky Science · pl
Obrazowanie cytometrii masowej ujawnia funkcjonalną i przestrzenną przebudowę komórek okołozmianowych w martwicy kości szczęki
Dlaczego gojenie szczęki czasem zawodzi
U niektórych osób przyjmujących silne leki chroniące kości pojawia się zagadkowy problem: fragmenty kości szczęki obumierają, a leżące nad nimi dziąsło nigdy całkowicie się nie goi. Stan ten, zwany martwicą kości szczęki związaną z lekami, może powodować ból, infekcje i długo utrzymujące się, niezamykające się rany. Lekarze wiedzą, które leki są związane z tym schorzeniem, ale nie rozumieją, dlaczego dotyka ono tylko części pacjentów ani dlaczego rany odmawiają zamknięcia. Badanie to zagląda do żywej krawędzi tych zmian, mapując miliony komórek i ich położenie, by zrozumieć, jak normalne procesy naprawcze ulegają zaburzeniu.
Bliższe spojrzenie na uszkodzoną tkankę szczęki
Naukowcy skupili się na strefie „okołozmianowej” — obręczy wciąż żywej tkanki otaczającej martwą kość w zajętych szczękach. Porównali próbki od pacjentów z martwicą kości szczęki ze zdrową tkanką jamy ustnej pobraną podczas rutynowych zabiegów stomatologicznych. Wykorzystując technologię zwaną obrazową cytometrią masową, wybarwili każdą cienką sekcję tkanki szerokim panelem przeciwciał, a następnie odczytali kilkadziesiąt białek w każdej pojedynczej komórce, zachowując przy tym jej dokładne położenie. Pozwoliło to podzielić tkankę na trzy główne obszary — nabłonek powierzchniowy, tkankę łączną podporową (stroma) oraz naczynia krwionośne i limfatyczne — oraz jednocześnie zidentyfikować komórki odpornościowe, komórki strukturalne i ich stany aktywności. 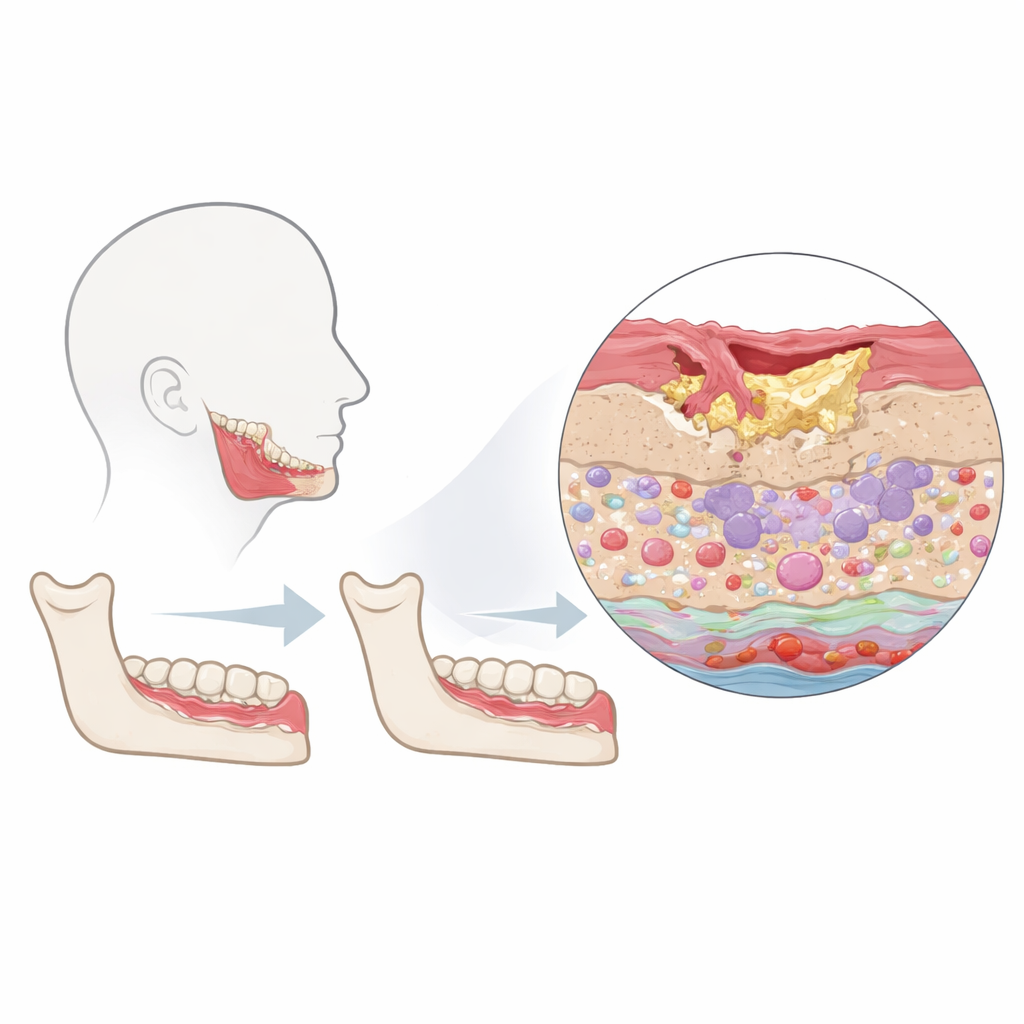
Komórki odpornościowe gromadzą się, ale tracą orientację
W chorych szczękach komórki układu odpornościowego wielu typów zalewały wszystkie regiony tkanki — powierzchnię, stromę i naczynia — znacznie bardziej niż u zdrowych kontrolnych próbek. Ich organizacja zmieniła się jednak w wymowny sposób. W normalnych warunkach wiele komórek odpornościowych jest rozproszonych i wykazuje jedynie subtelne preferencje względem siebie oraz sąsiadujących tkanek, tworząc zrównoważoną sieć nadzoru. W martwicy kilka typów komórek powiązanych z tłumieniem odporności i przewlekłym zapaleniem — komórki T regulatorowe, tzw. „wyczerpane” komórki T oraz makrofagi przypominające M2 — przeszło od wzajemnego unikania do formowania ciasnych lokalnych skupisk, szczególnie wokół naczyń. Inne pary komórek odpornościowych, które normalnie współpracowały blisko z nabłonkiem, stały się bardziej odsunięte. Ta reorganizacja sugeruje, że zamiast koordynować skuteczne sprzątanie, układ odpornościowy staje się mozaikowy i lokalnie tłumiący, co może pozwalać na utrzymywanie się infekcji i uszkodzeń.
Zestresowane tkanki próbują, ale nie potrafią się naprawić
Nabłonek jamy ustnej nad martwiczą kością wykazywał mniej typowych komórek nabłonkowych i słabsze ekspresje markerów strukturalnych, które zwykle utrzymują tę barierę. Jednocześnie wiele pozostałych komórek wyścielających produkowało wysokie poziomy białek związanych z podziałami komórkowymi i naprawą oraz markery stresu, zapalenia i programowanej śmierci komórkowej. Ten miks wskazuje na gorączkową, lecz chaotyczną próbę odrostu powierzchni. W tkance podporowej poniżej fibroblasty stały się liczniejsze i aktywowane, a zwykle bogata w kolagen macierz została zastąpiona gęsto upakowanymi komórkami. Naczynia krwionośne i limfatyczne wydawały się powiększone, a komórki ich wyściółki wykazywały oznaki proliferacji, zapalenia i niedoboru tlenu. Razem te zmiany malują obraz mikrośrodowiska utkniętego między wzrostem a uszkodzeniem: wiele komórek dzieli się, a jednocześnie równie wiele jest zestresowanych lub umiera. 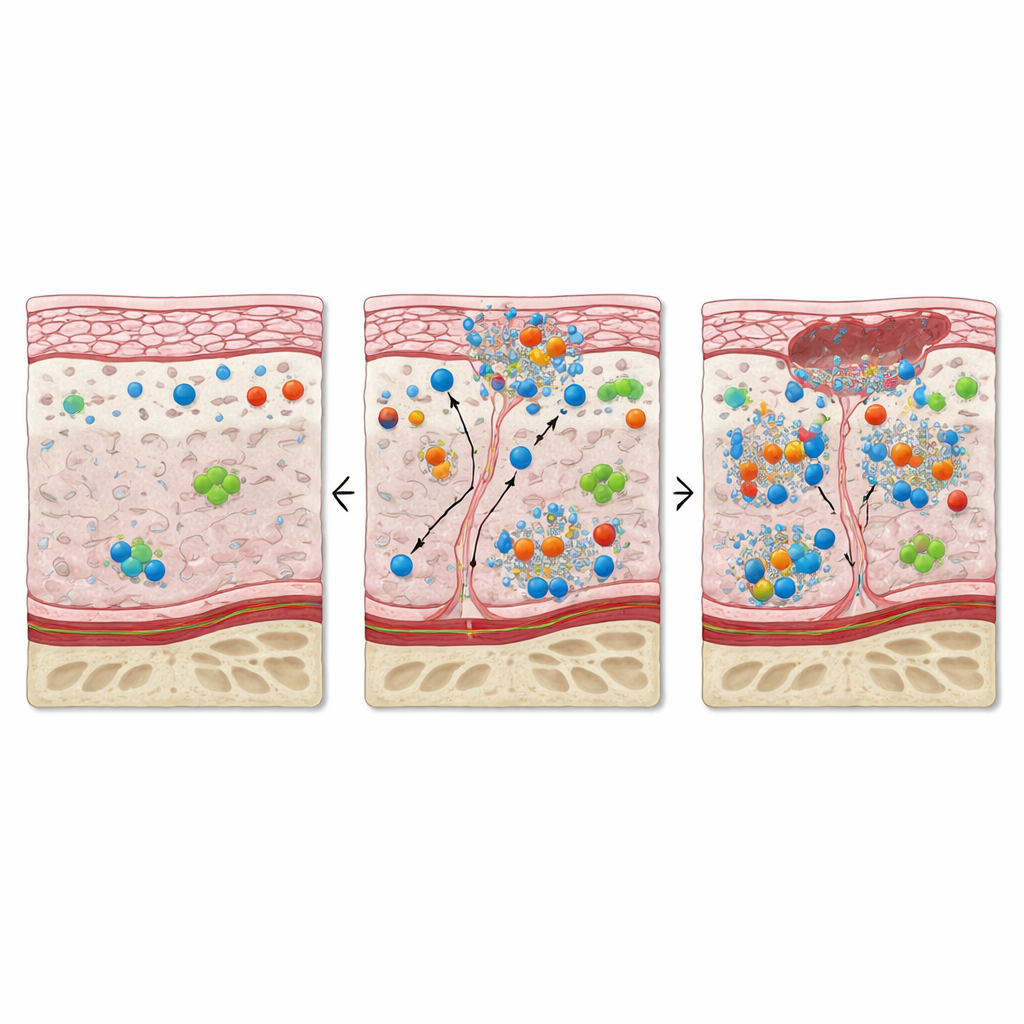
Splątana sieć sygnałów i przestrzeni
Łącząc ich przestrzenne mapy z bardziej tradycyjnymi metodami barwienia, zespół potwierdził, że kluczowe populacje odpornościowe i cząsteczki sygnałowe były wzbogacone i przemieszone w tkance chorobowej. Białka takie jak PD‑1, które zwykle pomagają hamować odpowiedzi odpornościowe, były silnie eksprymowane nie tylko na komórkach odpornościowych, ale też na komórkach nabłonkowych, co sugeruje szerokie „hamulce” zapalenia mogące być nadmiernie stosowane. Markery związane ze szlakami przetrwania i migracją były podwyższone w wielu typach komórek, zgodnie z obrazem komórek usiłujących przystosować się do surowego, przewlekle zapalonego środowiska. Jednak gdy te dane skompresowano do wzorców globalnych, próbki zdrowe i chore nadal znacznie się pokrywały, podkreślając, że kluczowe różnice leżą tak samo w rozmieszczeniu przestrzennym i nierównowadze funkcjonalnej, jak i w samym składzie typów komórek.
Co to znaczy dla pacjentów
Zamiast prostego zawodu kości lub jednego „złego” typu komórek, praca ta ukazuje martwicę kości szczęki jako problem systemowy: komórki odpornościowe, naczynia krwionośne, tkanka łączna i nabłonek powierzchniowy są wszystkie przebudowane i zablokowane w stanie stresu i słabej koordynacji. Tkanki wokół zmiany są wypełnione komórkami próbującymi naprawić uszkodzenie, ale jednocześnie są wyczerpane, zagęszczone i źle rozmieszczone. Dostarczając szczegółowego atlasu tego, kto jest gdzie i co robi, badanie to oferuje mapę drogową dla przyszłych terapii — takich, które mogłyby na przykład rozluźnić tłumiące skupiska odpornościowe, złagodzić szkodliwe zapalenie i przywrócić uporządkowaną regenerację, by szczęka mogła się zregenerować.
Cytowanie: Cai, J., Xue, Y., Tornaas, S. et al. Imaging mass cytometry unveils functional and spatial remodeling of peri-lesional cells in jaw osteonecrosis. Commun Biol 9, 442 (2026). https://doi.org/10.1038/s42003-026-09696-7
Słowa kluczowe: martwica kości szczęki, leki chroniące kości, gojenie ran w jamie ustnej, mikrośrodowisko odpornościowe, przestrzenne mapowanie tkanek