Clear Sky Science · nl
Beeldvormende massacytometrie onthult functionele en ruimtelijke herinrichting van peri‑laesionele cellen bij kaakosteonécrose
Waarom kaakgenezing soms faalt
Sommige mensen die krachtige middelen gebruiken om hun botten te beschermen, krijgen een raadselachtig probleem: delen van hun kaakbot sterven af en het daarboven liggende tandvlees geneest nooit volledig. Deze aandoening, medicatiegerelateerde osteonecrose van de kaak genoemd, kan pijn, infectie en open zweren veroorzaken die maandenlang aanhouden. Artsen weten welke geneesmiddelen betrokken zijn, maar niet waarom slechts een deel van de patiënten wordt getroffen of waarom de wonden niet sluiten. Deze studie werpt een blik in de levende rand van deze kaaklaesies, waarbij miljoenen cellen en hun locaties in kaart worden gebracht om te begrijpen hoe normale reparatieprocessen ontsporen.
Een nadere blik op beschadigd kaakweefsel
De onderzoekers concentreerden zich op de “peri‑laesionele” zone — de rand van nog levende weefsels rond het dode bot in aangedane kaken. Ze vergeleken monsters van patiënten met kaakosteonécrose met gezond mondweefsel dat tijdens routinematige tandheelkundige ingrepen werd genomen. Met een techniek genaamd imaging mass cytometry kleurden ze elke dunne weefselplaat met een groot paneel antilichamen en konden vervolgens tientallen eiwitten in elke individuele cel meten terwijl de exacte positie behouden bleef. Dit stelde hen in staat het weefsel in drie hoofdregio's te verdelen — oppervlaktebekleding (epitheel), ondersteunend bindweefsel (stroma) en bloed- en lymfevaten — en gelijktijdig immuuncellen, structurele cellen en hun activiteitstoestanden te identificeren. 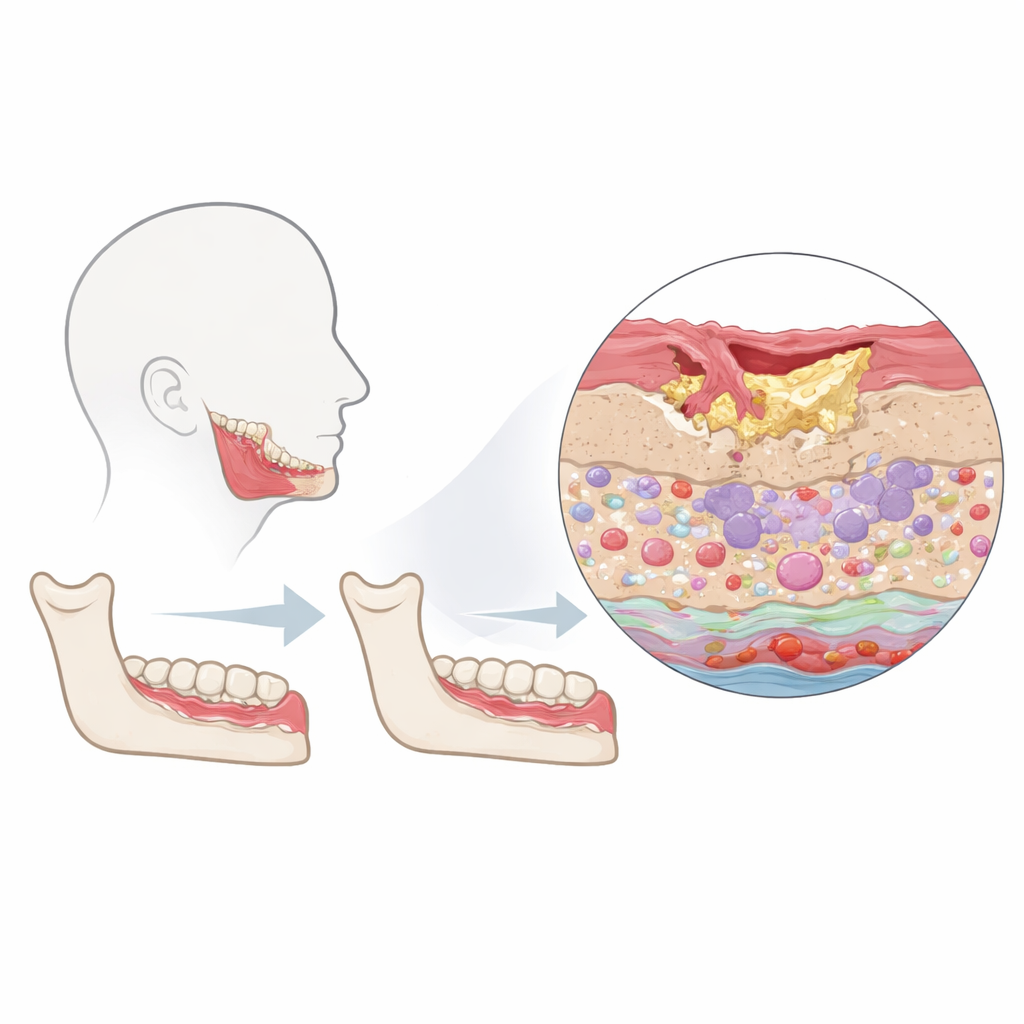
Immuuncellen verzamelen zich maar verliezen hun sturing
In zieke kaken stroomden immuuncellen van vele typen alle regio's van het weefsel binnen — oppervlakte, stroma en vaten — veel meer dan bij gezonde controles. Hun organisatie veranderde echter op betekenisvolle manieren. Onder normale omstandigheden zijn veel immuuncellen verspreid en tonen slechts milde voorkeuren voor elkaar en voor nabijgelegen weefsels, waardoor een evenwichtig surveillancesysteem ontstaat. Bij osteonecrose verschoof een aantal celtypen die geassocieerd zijn met immuunsuppressie en chronische ontsteking — regulerende T‑cellen, zogenoemde “uitgeputte” T‑cellen en M2‑achtige macrofagen — van elkaar vermijden naar het vormen van compacte lokale clusters, vooral rond vaten. Andere immuunkoppelingen die normaal nauw met het epitheel samenwerkten, raakten verder van elkaar verwijderd. Deze herschikking suggereert dat het immuunsysteem, in plaats van een efficiënte opruiming te coördineren, gefragmenteerd en lokaal onderdrukkend wordt, wat mogelijk infectie en schade in stand houdt.
Gestreste weefsels proberen te repareren, maar falen
De bekleding van de mond over het osteonecrotische bot vertoonde minder typische epitheelcellen en zwakkere expressie van de structurele merkers die deze barrière normaal bijeenhouden. Tegelijkertijd produceerden veel resterende bekledingscellen hoge niveaus van eiwitten die geassocieerd zijn met celdeling en herstel, evenals merkers van stress, ontsteking en geprogrammeerde celdood. Deze combinatie wijst op een wanhopige maar ongeordende poging om het oppervlak te herstellen. In het ondersteunende weefsel daaronder werden fibroblasten talrijker en geactiveerd, en de normaal collageenrijke matrix werd vervangen door dicht opeengepakte cellen. Bloed- en lymfevaten leken vergroot en hun bekledende cellen vertoonden tekenen van proliferatie, ontsteking en zuurstoftekort. Samen schetsen deze veranderingen een micro‑omgeving gevangen tussen groei en beschadiging: veel cellen delen zich, maar evenveel zijn gestrest of sterven. 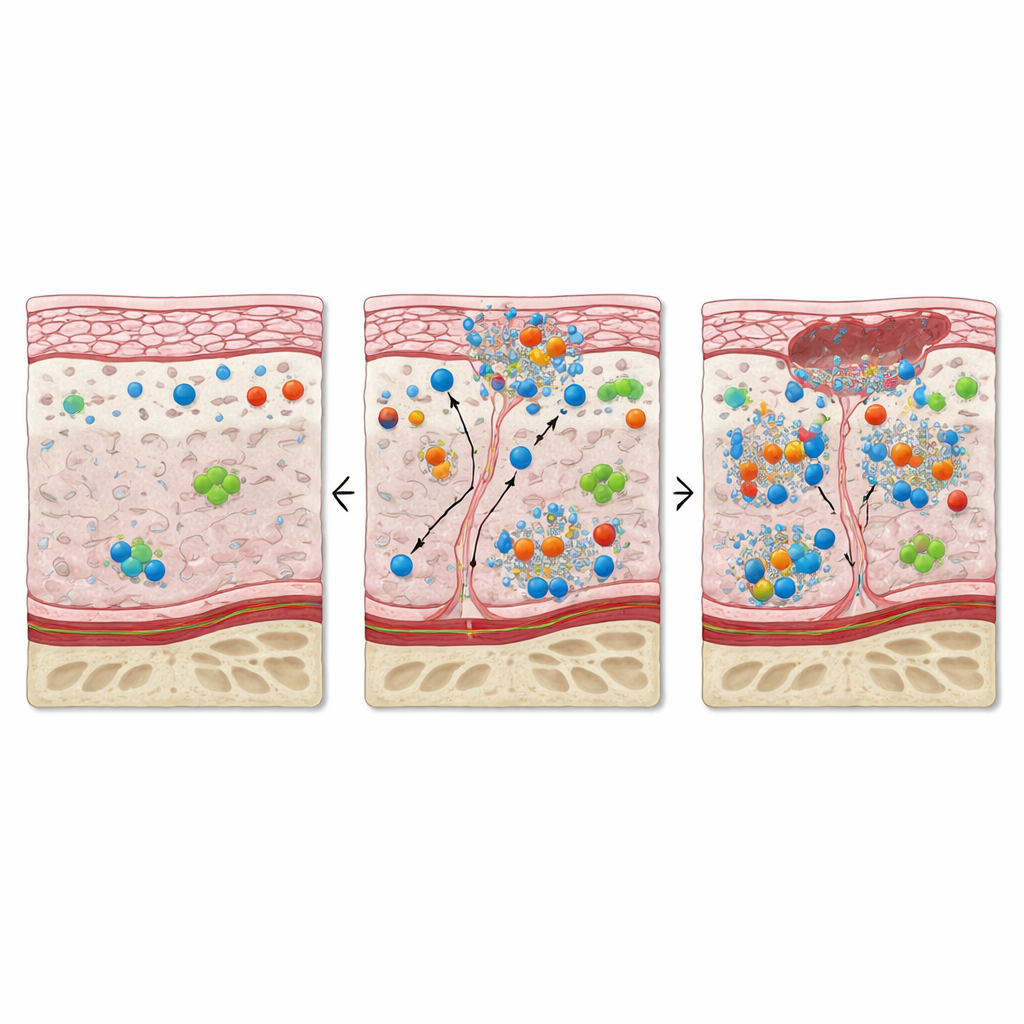
Een verward web van signalen en ruimten
Door hun ruimtelijke kaarten te combineren met meer traditionele kleuringsmethoden, bevestigde het team dat sleutelimmuuncellen en signaalmoleculen verrijkt en herpositioneerd waren in ziek weefsel. Eiwitten zoals PD‑1, die normaal helpen immuunreacties te remmen, werden sterk tot expressie gebracht niet alleen op immuuncellen maar ook op epitheelcellen, wat wijst op wijdverbreide “remmen” op ontsteking die mogelijk te sterk zijn toegepast. Merkers gekoppeld aan overlevingspaden en migratie waren verhoogd in veel celtypen, wat overeenkomt met cellen die worstelen zich aan te passen aan een harde, chronisch ontstoken omgeving. Toch overlappen gezonde en zieke monsters, wanneer deze gegevens in globale patronen worden samengevat, nog steeds aanzienlijk, wat benadrukt dat de cruciale verschillen net zozeer liggen in ruimtelijke ordening en functionele disbalans als in welke celtypen aanwezig zijn.
Wat dit betekent voor patiënten
In plaats van een eenvoudige uitval van bot of één “slechte” celsoort, toont dit werk kaakosteonécrose als een systeemprobleem: immuuncellen, bloedvaten, bindweefsel en oppervlaktebekleding worden allemaal hergevormd en vastgezet in een gestreste, slecht gecoördineerde toestand. De weefsels rond de laesie zitten vol cellen die proberen schade te herstellen, maar die tegelijk uitgeput, overbezet en verkeerd gepositioneerd zijn. Door een gedetailleerde atlas te bieden van wie waar is en wat ze doen, biedt deze studie een routekaart voor toekomstige therapieën — bijvoorbeeld benaderingen die suppressieve immuunclusters losmaken, schadelijke ontsteking kalmeren en ordelijk regenereren herstellen zodat de kaak kan genezen.
Bronvermelding: Cai, J., Xue, Y., Tornaas, S. et al. Imaging mass cytometry unveils functional and spatial remodeling of peri-lesional cells in jaw osteonecrosis. Commun Biol 9, 442 (2026). https://doi.org/10.1038/s42003-026-09696-7
Trefwoorden: kaakosteonécrose, botbeschermende geneesmiddelen, orale wondgenezing, immuunmicro‑omgeving, ruimtelijke weefselmapping