Clear Sky Science · es
La citometría de masas por imagen revela la remodelación funcional y espacial de las células peri‑lesionales en la osteonecrosis mandibular
Por qué a veces falla la cicatrización de la mandíbula
Algunas personas que toman medicamentos potentes para proteger sus huesos desarrollan un problema desconcertante: partes del hueso mandibular mueren y la encía que las cubre nunca termina de cicatrizar. Esta afección, llamada osteonecrosis de la mandíbula relacionada con medicación, puede provocar dolor, infección y úlceras abiertas que persisten durante meses. Los médicos saben qué fármacos están implicados, pero no por qué solo una fracción de pacientes se ve afectada ni por qué las heridas no cierran. Este estudio examina el borde vivo de estas lesiones mandibulares, cartografiando millones de células y sus ubicaciones para entender cómo los procesos normales de reparación se descarrilan.
Una mirada de cerca al tejido mandibular dañado
Los investigadores se centraron en la zona “peri‑lesional”: el borde de tejido aún vivo que rodea el hueso muerto en mandíbulas afectadas. Compararon muestras de pacientes con osteonecrosis mandibular con tejido oral sano tomado durante cirugía dental rutinaria. Usando una tecnología llamada citometría de masas por imagen, tiñeron cada corte fino de tejido con un amplio panel de anticuerpos y luego midieron docenas de proteínas en cada célula manteniendo su posición exacta. Esto les permitió separar el tejido en tres regiones principales—revestimiento superficial (epitelio), tejido conectivo de sostén (estroma) y vasos sanguíneos y linfáticos—e identificar células inmunitarias, células estructurales y sus estados de actividad de forma simultánea. 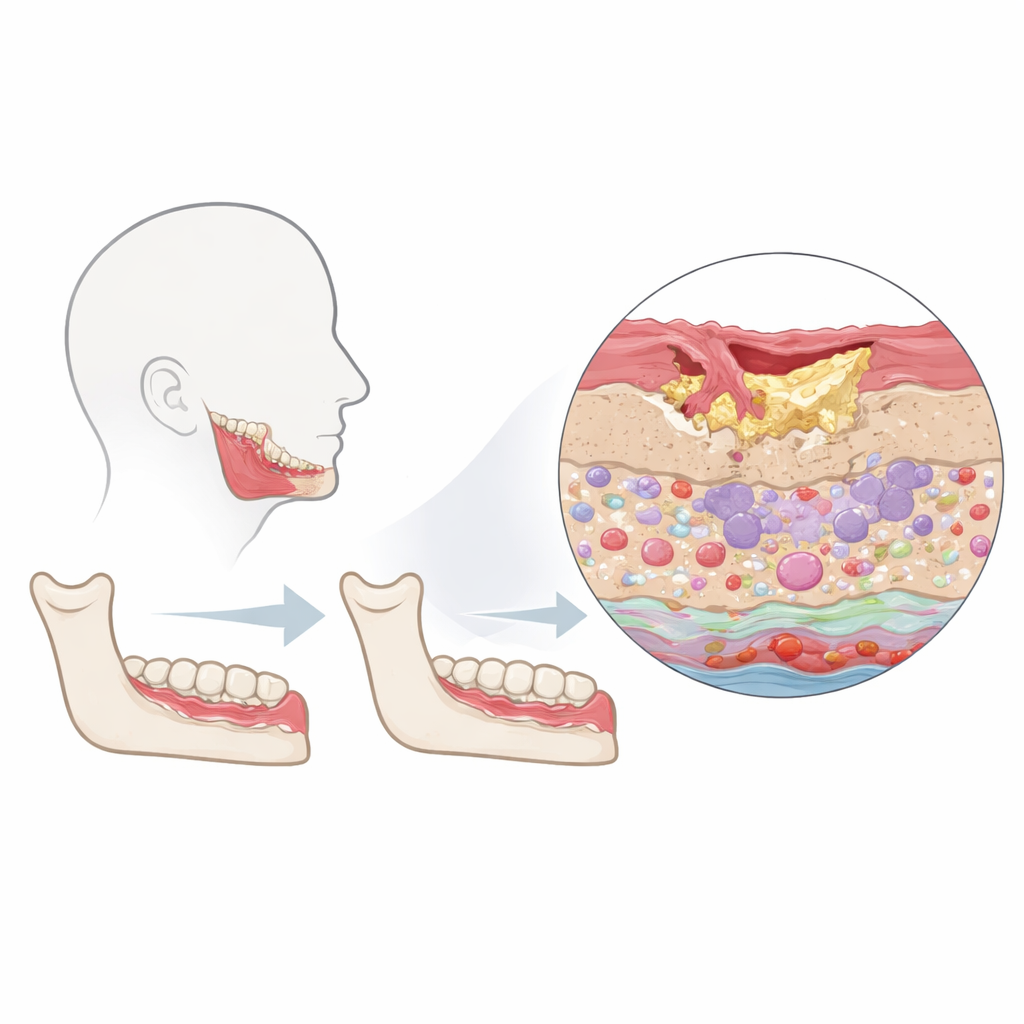
Las células inmunitarias se congregan pero pierden su orientación
En las mandíbulas enfermas, células inmunitarias de muchos tipos invadieron todas las regiones del tejido—superficie, estroma y vasos—con mucha mayor abundancia que en los controles sanos. Sin embargo, su organización cambió de maneras reveladoras. En condiciones normales, muchas células inmunitarias están dispersas y muestran solo preferencias suaves entre sí y con los tejidos cercanos, formando una red equilibrada de vigilancia. En la osteonecrosis, varios tipos celulares vinculados a la supresión inmune y la inflamación crónica—células T reguladoras, las llamadas células T “exhaustas” y macrófagos tipo M2—pasaron de evitarse entre sí a formar cúmulos locales compactos, especialmente alrededor de los vasos. Otras asociaciones inmunitarias que normalmente trabajaban cerca del epitelio se volvieron más distantes. Esta reorganización sugiere que, en lugar de coordinar una limpieza eficaz, el sistema inmunitario se vuelve parcheado y localmente supresor, lo que podría permitir que la infección y el daño persistan.
Tejidos estresados que intentan, y fracasan, reparar
El revestimiento de la boca sobre el hueso osteonecrótico mostró menos células epiteliales típicas y una expresión más débil de los marcadores estructurales que normalmente mantienen esta barrera unida. Al mismo tiempo, muchas de las células del revestimiento que quedaban producían altos niveles de proteínas asociadas con la división celular y la reparación, así como marcadores de estrés, inflamación y muerte celular programada. Esta mezcla apunta a un intento frenético pero desorganizado de regenerar la superficie. En el tejido de sostén subyacente, las células fibroblásticas aumentaron en número y se activaron, y la matriz normalmente rica en colágeno fue reemplazada por células densamente empaquetadas. Los vasos sanguíneos y linfáticos aparecieron agrandados y sus células endoteliales mostraron signos de proliferación, inflamación y falta de oxígeno. En conjunto, estos cambios dibujan el paisaje de un microambiente atrapado entre el crecimiento y la lesión: muchas células están proliferando, pero un número similar está estresado o muriendo. 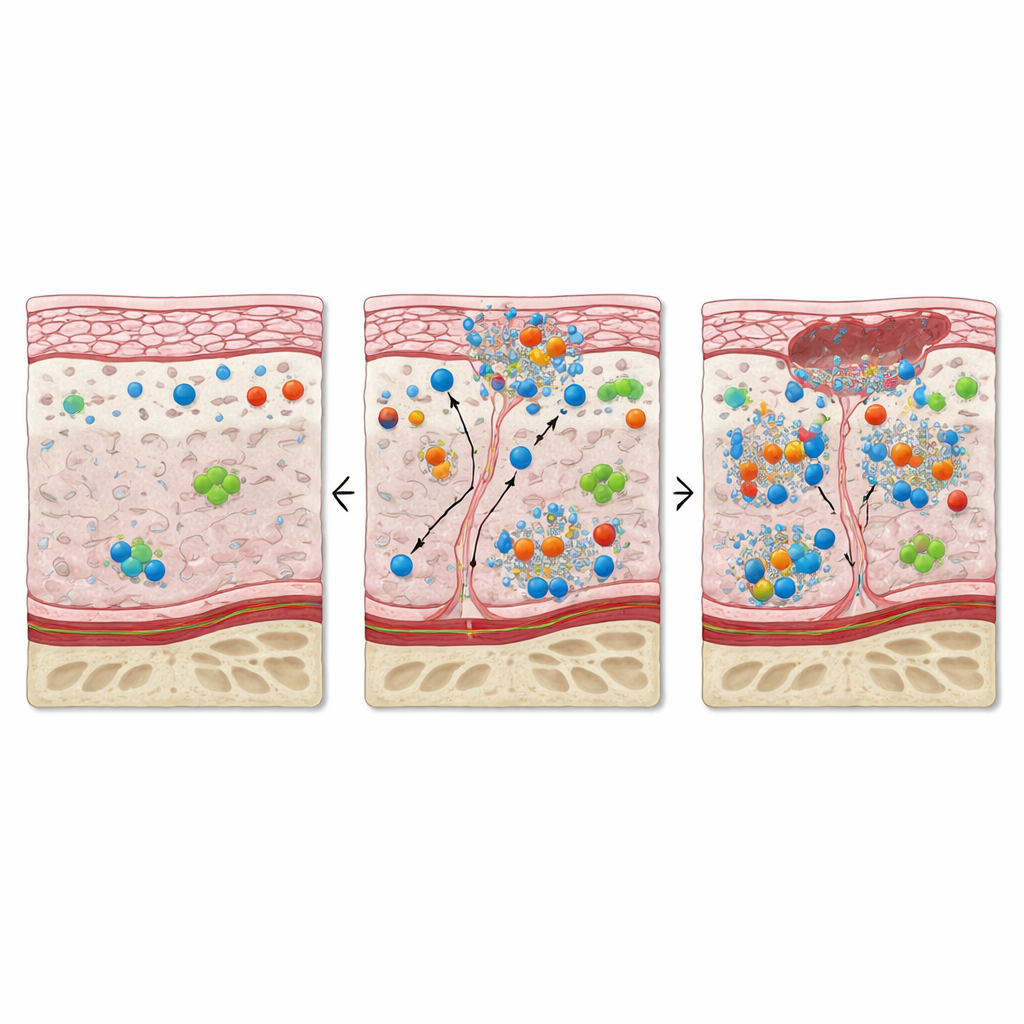
Una red enmarañada de señales y espacios
Al combinar sus mapas espaciales con métodos de tinción más tradicionales, el equipo confirmó que poblaciones inmunitarias clave y moléculas de señalización estaban enriquecidas y reposicionadas en el tejido enfermo. Proteínas como PD‑1, que normalmente ayudan a mantener las respuestas inmunitarias bajo control, se expresaron fuertemente no solo en células inmunitarias sino también en células epiteliales, sugiriendo frenos generalizados sobre la inflamación que podrían estar sobreactivados. Marcadores vinculados a vías de supervivencia y migración se elevaron en muchos tipos celulares, coherente con células que luchan por adaptarse a un entorno hostil y crónicamente inflamado. Sin embargo, cuando estos datos se condensaron en patrones globales, las muestras sanas y enfermas todavía se solaparon sustancialmente, lo que subraya que las diferencias cruciales residen tanto en la disposición espacial y el desequilibrio funcional como en los tipos celulares presentes.
Lo que esto significa para los pacientes
En lugar de un simple fallo del hueso o un único tipo celular “malo”, este trabajo muestra la osteonecrosis mandibular como un problema sistémico: células inmunitarias, vasos sanguíneos, tejido conectivo y revestimiento superficial están todos remodelados y bloqueados en un estado estresado y mal coordinado. Los tejidos alrededor de la lesión están repletos de células que intentan reparar el daño, pero al mismo tiempo están exhaustas, apiñadas y mal posicionadas. Al proporcionar un atlas detallado de quién está dónde y qué está haciendo, este estudio ofrece una hoja de ruta para terapias futuras—por ejemplo, intervenciones que puedan aflojar los cúmulos inmunosupresores, calmar la inflamación dañina y restaurar una regeneración ordenada para que la mandíbula pueda sanar.
Cita: Cai, J., Xue, Y., Tornaas, S. et al. Imaging mass cytometry unveils functional and spatial remodeling of peri-lesional cells in jaw osteonecrosis. Commun Biol 9, 442 (2026). https://doi.org/10.1038/s42003-026-09696-7
Palabras clave: osteonecrosis mandibular, fármacos con efecto protector óseo, cicatrización de heridas orales, microambiente inmunitario, mapado espacial de tejidos