Clear Sky Science · de
Bildgebende Massenspektrometrie enthüllt funktionelle und räumliche Umbildung peri‑läsionaler Zellen bei Kieferosteonekrose
Warum die Heilung im Kiefer manchmal versagt
Bei einigen Menschen, die starke Medikamente zum Schutz der Knochen einnehmen, tritt ein rätselhaftes Problem auf: Teile ihres Kieferknochens sterben ab und das darüber liegende Zahnfleisch heilt nie vollständig. Dieser Zustand, als medikamentenassoziierte Osteonekrose des Kiefers bezeichnet, kann Schmerzen, Infektionen und wochen- bis monatelang andauernde offene Wunden verursachen. Ärztinnen und Ärzte kennen die beteiligten Medikamente, nicht aber, warum nur ein Bruchteil der Patientinnen und Patienten betroffen ist oder weshalb die Wunden nicht verschließen. Diese Studie blickt in den lebenden Rand dieser Kieferläsionen, kartiert Millionen von Zellen und ihre Positionen, um zu verstehen, wie normale Reparaturprozesse aus dem Ruder laufen.
Ein genauer Blick auf geschädigtes Kiefergewebe
Die Forschenden konzentrierten sich auf die „peri‑läsionale“ Zone — den Rand des noch lebenden Gewebes, das toten Knochen in betroffenen Kiefern umgibt. Sie verglichen Proben von Patientinnen und Patienten mit Kieferosteonekrose mit gesundem oralen Gewebe, das bei routinemäßigen Zahnoperationen entnommen wurde. Mit einer Technik namens Imaging Mass Cytometry färbten sie jede dünne Gewebescheibe mit einem großen Antikörperpanel und bestimmten Dutzende Proteine in jeder einzelnen Zelle, während die exakte Position erhalten blieb. Das ermöglichte, das Gewebe in drei Hauptregionen zu unterteilen — Oberflächenepithel, stützendes Bindegewebe (Stroma) und Blut- und Lymphgefäße — und gleichzeitig Immunzellen, Strukturzellen und deren Aktivitätszustände zu identifizieren. 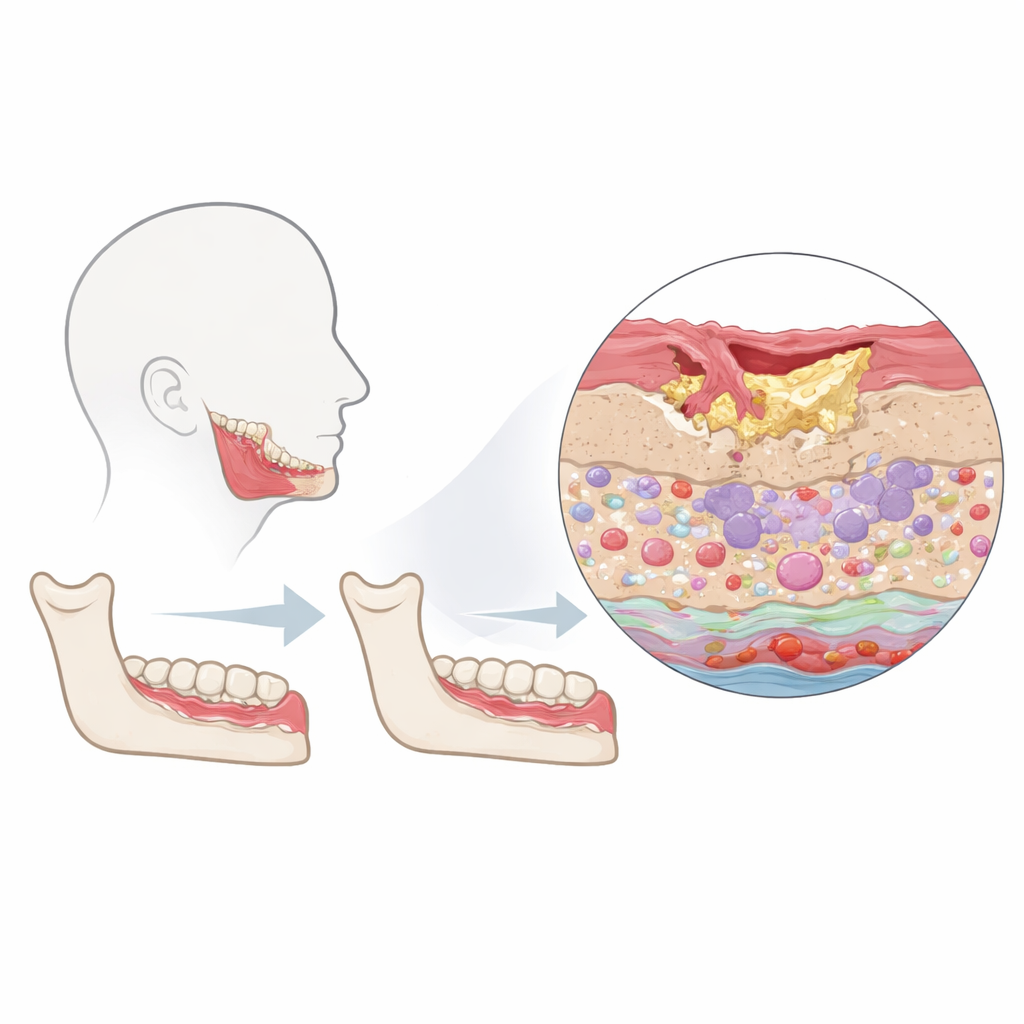
Immunzellen sammeln sich, verlieren aber ihre Orientierung
In erkrankten Kiefern durchfluteten Immunzellen vieler Typen alle Bereiche des Gewebes — Oberfläche, Stroma und Gefäße — deutlich häufiger als in gesunden Kontrollen. Ihre Organisation veränderte sich jedoch aufschlussreich. Unter normalen Bedingungen sind viele Immunzellen verstreut und zeigen nur milde Präferenzen zueinander und zu benachbarten Geweben, sodass ein ausgewogenes Überwachungsnetz entsteht. Bei Osteonekrose gingen mehrere Zelltypen, die mit Immunsuppression und chronischer Entzündung verknüpft sind — regulatorische T‑Zellen, sogenannte „erschöpfte“ T‑Zellen und M2‑ähnliche Makrophagen — von einer gegenseitigen Vermeidung zu dichten lokalen Clustern über, insbesondere rund um Gefäße. Andere Immun‑Kopplungen, die normalerweise eng mit dem Epithel zusammenarbeiten, entfernten sich. Diese Umorganisation deutet darauf hin, dass das Immunsystem anstatt einer effizienten Aufräumarbeit zu koordinieren, fragmentiert und lokal unterdrückend wird, was Infektionen und anhaltende Schäden begünstigen kann.
Gestresste Gewebe versuchen zu reparieren — und scheitern
Das Epithel über osteonekrotischem Knochen zeigte weniger typische Oberflächenzellen und eine schwächere Expression der Strukturmarker, die diese Barriere normalerweise zusammenhalten. Zugleich produzierten viele verbleibende Epithelzellen hohe Mengen an Proteinen, die mit Zellteilung und Reparatur assoziiert sind, sowie Marker für Stress, Entzündung und programmierter Zelltod. Diese Mischung weist auf einen hektischen, aber ungeordneten Versuch hin, die Oberfläche neu aufzubauen. Im darunterliegenden Stroma wurden Fibroblasten zahlreicher und aktivierter, und die gewöhnlich kollagenreiche Matrix wurde durch dicht gepackte Zellen ersetzt. Blut- und Lymphgefäße erschienen vergrößert, und deren Endothelzellen zeigten Zeichen von Proliferation, Entzündung und Sauerstoffmangel. Zusammengenommen zeichnen diese Veränderungen das Bild eines Mikromilieus zwischen Wachstum und Verletzung: Viele Zellen teilen sich, aber ebenso viele sind gestresst oder sterben. 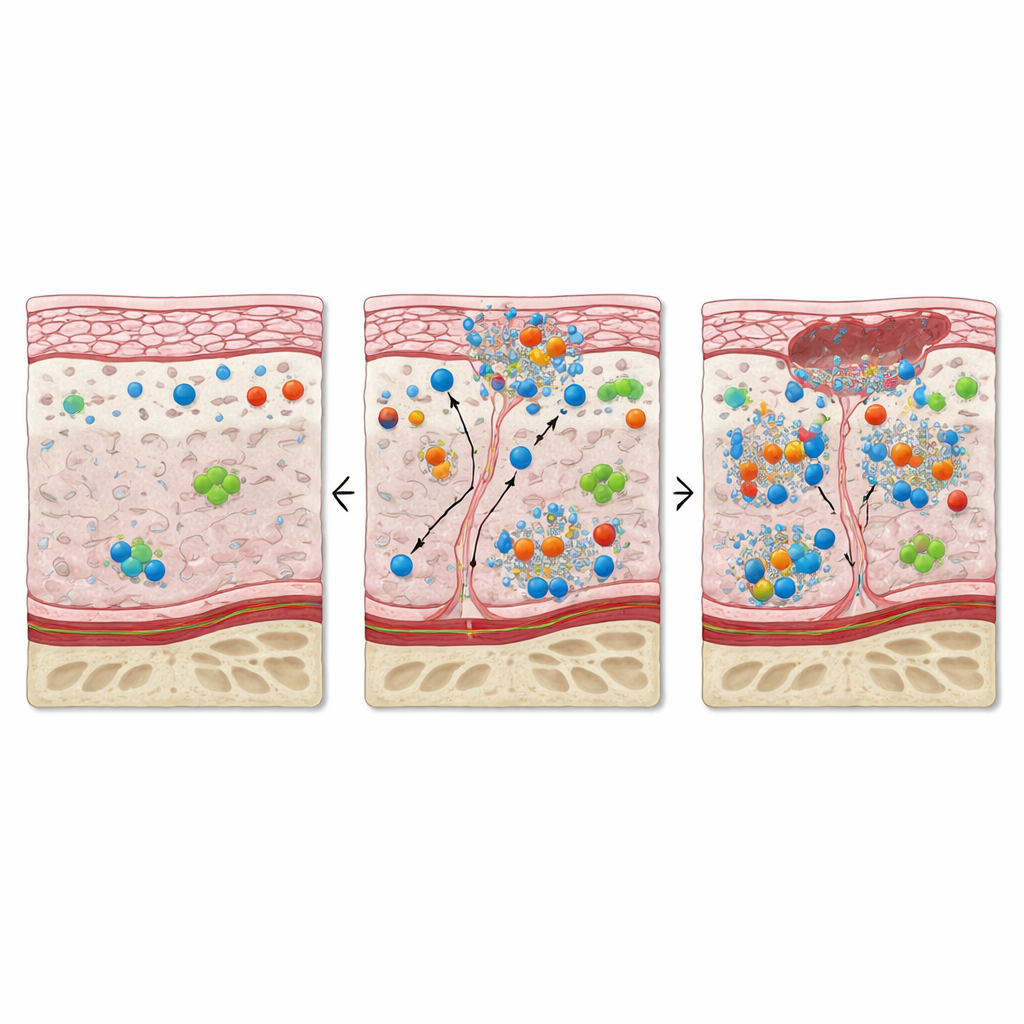
Ein verwobenes Netz aus Signalen und Räumen
Durch die Kombination ihrer räumlichen Karten mit traditionelleren Färbemethoden bestätigte das Team, dass wichtige Immunpopulationen und Signalmoleküle in erkranktem Gewebe angereichert und umpositioniert waren. Proteine wie PD‑1, die normalerweise helfen, Immunantworten zu bremsen, wurden nicht nur auf Immunzellen, sondern auch stark auf Epithelzellen exprimiert, was auf weit verbreitete „Bremsen“ der Entzündung hindeutet, die möglicherweise übermäßig angewendet werden. Marker, die mit Überlebenswegen und Migration verknüpft sind, waren in vielen Zelltypen erhöht — konsistent mit Zellen, die versuchen, sich an ein raues, chronisch entzündetes Milieu anzupassen. Wenn diese Daten jedoch in globale Muster komprimiert wurden, überschnitten sich gesunde und erkrankte Proben weiterhin erheblich, was betont, dass die entscheidenden Unterschiede ebenso sehr in der räumlichen Anordnung und funktionellen Verschiebung liegen wie in der bloßen Präsenz bestimmter Zelltypen.
Was das für Patientinnen und Patienten bedeutet
Statt eines einfachen Versagens des Knochens oder eines einzelnen „schlechten“ Zelltyps zeigt diese Arbeit Kieferosteonekrose als Systemproblem: Immunzellen, Gefäße, Bindegewebe und Oberflächenepithel sind alle umgestaltet und in einen gestressten, schlecht koordinierten Zustand verriegelt. Das Gewebe um die Läsion ist voller Zellen, die versuchen, Schäden zu reparieren, zugleich aber erschöpft, überfüllt und fehlpositioniert sind. Indem die Studie einen detaillierten Atlas darüber liefert, wer wo ist und was diese Zellen tun, bietet sie eine Landkarte für zukünftige Therapien — etwa Ansätze, die unterdrückende Immuncluster auflockern, schädliche Entzündungen dämpfen und geordnete Regeneration wiederherstellen, damit der Kiefer heilen kann.
Zitation: Cai, J., Xue, Y., Tornaas, S. et al. Imaging mass cytometry unveils functional and spatial remodeling of peri-lesional cells in jaw osteonecrosis. Commun Biol 9, 442 (2026). https://doi.org/10.1038/s42003-026-09696-7
Schlüsselwörter: Kieferosteonekrose, knochenschützende Medikamente, orale Wundheilung, immunkleines Umfeld, räumliche Gewebekartierung