Clear Sky Science · it
La imaging mass cytometry svela il rimodellamento funzionale e spaziale delle cellule peri‑lesionali nell’osteonecrosi mandibolare
Perché la guarigione della mandibola a volte fallisce
Alcune persone che assumono farmaci potenti per proteggere le ossa sviluppano un problema sconcertante: parti dell’osso della mandibola muoiono e la gengiva sovrastante non si rimargina completamente. Questa condizione, detta osteonecrosi della mandibola correlata ai farmaci, può provocare dolore, infezioni e piaghe aperte che persistono per mesi. I medici conoscono i farmaci coinvolti, ma non spiegano perché ne sia colpita solo una parte dei pazienti né perché le ferite non si richiudano. Questo studio dà uno sguardo all’interno del margine vitale di queste lesioni mandibolari, mappando milioni di cellule e le loro posizioni per capire come i normali processi di riparazione vadano fuori strada.
Uno sguardo ravvicinato al tessuto mandibolare danneggiato
I ricercatori si sono concentrati sulla zona “peri‑lesionale” — il bordo di tessuto ancora vitale che circonda l’osso morto nelle mandibole colpite. Hanno confrontato campioni da pazienti con osteonecrosi mandibolare con tessuto orale sano prelevato durante interventi odontoiatrici di routine. Utilizzando una tecnologia chiamata imaging mass cytometry, hanno colorato ogni sottile sezione di tessuto con un ampio pannello di anticorpi e poi hanno letto dozzine di proteine in ciascuna cellula mantenendone la posizione esatta. Questo ha permesso di separare il tessuto in tre regioni principali — rivestimento superficiale (epitelio), tessuto connettivo di supporto (stroma) e vasi sanguigni e linfatici — e di identificare cellule immunitarie, cellule strutturali e i loro stati di attività contemporaneamente. 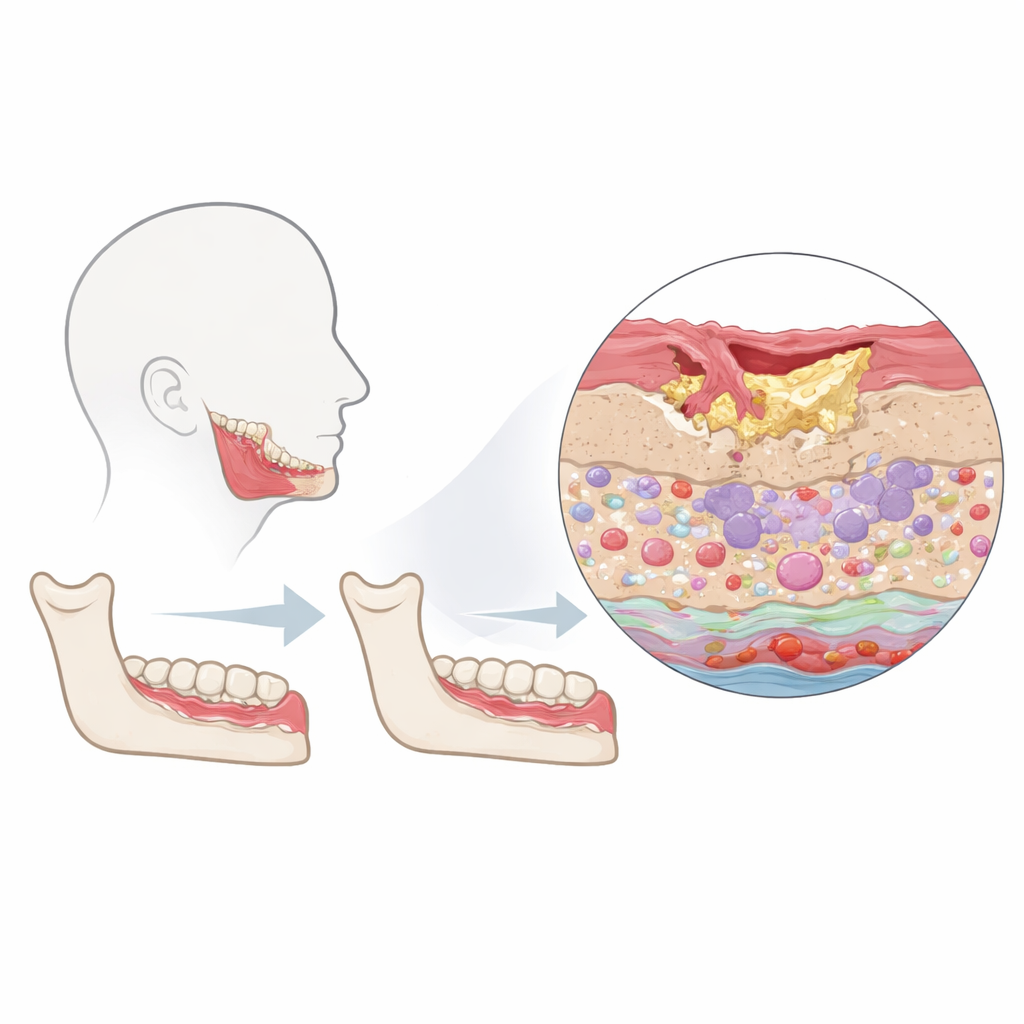
Le cellule immunitarie si radunano ma perdono la guida
Nelle mandibole malate, cellule immunitarie di molti tipi hanno invaso tutte le regioni del tessuto — superficie, stroma e vasi — molto più di quanto osservato nei controlli sani. Tuttavia, la loro organizzazione è cambiata in modi significativi. In condizioni normali molte cellule immunitarie sono distribuite e mostrano solo lievi preferenze reciproche e verso i tessuti vicini, formando una rete di sorveglianza equilibrata. Nell’osteonecrosi, diversi tipi cellulari associati a immunosoppressione e infiammazione cronica — cellule T regolatorie, le cosiddette cellule T “esauste” e macrofagi di tipo M2 — sono passati dall’evitare reciprocamente al formare stretti ammassi locali, specialmente attorno ai vasi. Altri abbinamenti immunitari che normalmente lavoravano a stretto contatto con l’epitelio si sono invece allontanati. Questo riassetto suggerisce che, invece di coordinare una pulizia efficiente, il sistema immunitario diventi frammentato e localmente soppressivo, permettendo potenzialmente a infezioni e danni di persistere.
Tessuti stressati che provano, e falliscono, a riparare
Il rivestimento della bocca sopra l’osso osteonecrotico mostrava meno cellule epiteliali tipiche e una minore espressione dei marker strutturali che normalmente mantengono questa barriera integra. Allo stesso tempo, molte delle cellule di rivestimento rimaste producevano alti livelli di proteine associate alla divisione cellulare e alla riparazione, nonché marker di stress, infiammazione e morte cellulare programmata. Questo mix indica un tentativo frenetico ma disorganizzato di rigenerare la superficie. Nel tessuto di supporto sottostante, i fibroblasti sono diventati più numerosi e attivati, e la matrice solitamente ricca di collagene è stata rimpiazzata da cellule densamente impacchettate. Vasi sanguigni e linfatici risultavano dilatati e le loro cellule di rivestimento mostravano segni di proliferazione, infiammazione e carenza di ossigeno. Insieme, questi cambiamenti dipingono il quadro di un microambiente sospeso tra crescita e danno: molte cellule si stanno dividendo, ma altrettante sono stressate o in via di morte. 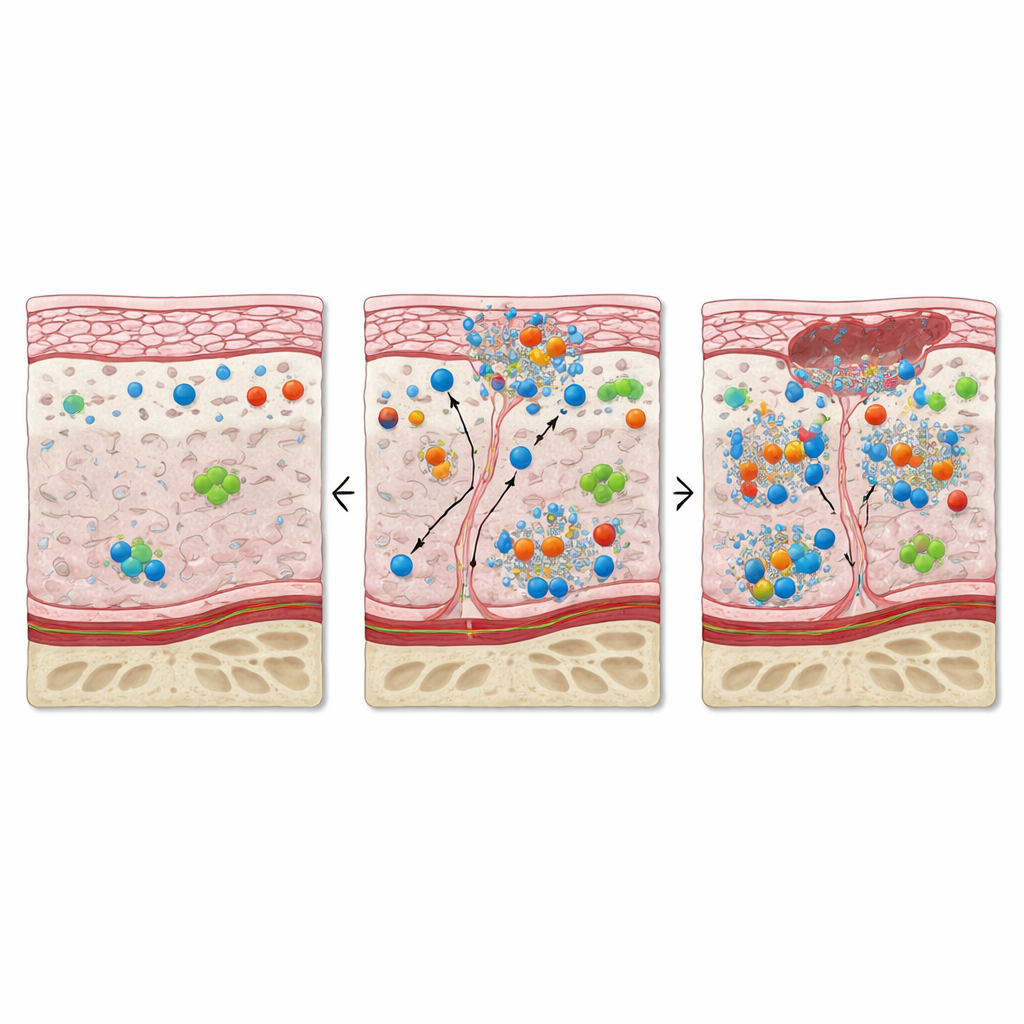
Una rete intricata di segnali e spazi
Combinando le loro mappe spaziali con metodi di colorazione più tradizionali, il gruppo ha confermato che popolazioni immunitarie chiave e molecole di segnalazione erano arricchite e riposizionate nel tessuto malato. Proteine come PD‑1, che normalmente aiutano a contenere le risposte immunitarie, erano fortemente espresse non solo sulle cellule immunitarie ma anche sulle cellule epiteliali, suggerendo la presenza diffusa di “freni” sull’infiammazione che potrebbero risultare eccessivi. Marker collegati a vie di sopravvivenza e migrazione erano elevati in molti tipi cellulari, coerente con cellule che cercano di adattarsi a un ambiente ostile e cronicamente infiammato. Eppure, quando questi dati venivano compressi in pattern globali, campioni sani e malati si sovrapponevano ancora in misura notevole, sottolineando che le differenze cruciali risiedono tanto nell’organizzazione spaziale e nello squilibrio funzionale quanto nella presenza o assenza di specifici tipi cellulari.
Cosa significa per i pazienti
Piuttosto che un semplice fallimento dell’osso o un singolo tipo cellulare “cattivo”, questo lavoro interpreta l’osteonecrosi mandibolare come un problema sistemico: cellule immunitarie, vasi sanguigni, tessuto connettivo e rivestimento superficiale sono tutti rimodellati e bloccati in uno stato stressato e poco coordinato. I tessuti attorno alla lesione sono affollati di cellule che tentano di riparare il danno, ma sono al contempo esauste, sovraffollate e mal posizionate. Fornendo un atlante dettagliato di chi è dove e cosa stanno facendo, questo studio offre una road map per terapie future — per esempio, interventi volti ad allentare ammassi immunosoppressivi, calmare l’infiammazione dannosa e ripristinare una rigenerazione ordinata in modo che la mandibola possa guarire.
Citazione: Cai, J., Xue, Y., Tornaas, S. et al. Imaging mass cytometry unveils functional and spatial remodeling of peri-lesional cells in jaw osteonecrosis. Commun Biol 9, 442 (2026). https://doi.org/10.1038/s42003-026-09696-7
Parole chiave: osteonecrosi mandibolare, farmaci protettivi per l’osso, guarigione delle ferite orali, microambiente immunitario, mappatura spaziale dei tessuti