Clear Sky Science · pl
Zmiany ekspresji genów wywołane hipoksją w embrionach N. vectensis
Dlaczego tlen ma znaczenie dla malutkich morskich embrionów
Pierwsze zwierzęta Ziemi pojawiły się w pradawnych morzach, gdzie poziomy tlenu wzrastały i spadały w czasie. To badanie stawia proste, lecz dalekosiężne pytanie: jak bardzo młode embriony zwierząt radzą sobie, gdy tlen, od którego zależą, nagle spada? Obserwując embriony niewielkiej anemony morskiej, badacze wykryli, w jaki sposób wczesne stadia życia mogą tymczasowo wstrzymać własny rozwój podczas epizodów niskiego tlenu, a następnie wznowić go, gdy warunki się poprawią. Te wnioski pomagają wyobrazić sobie, z czym mierzyło się wczesne życie zwierzęce setki milionów lat temu — i jak współczesne zwierzęta wciąż noszą molekularne ślady tych wyzwań.
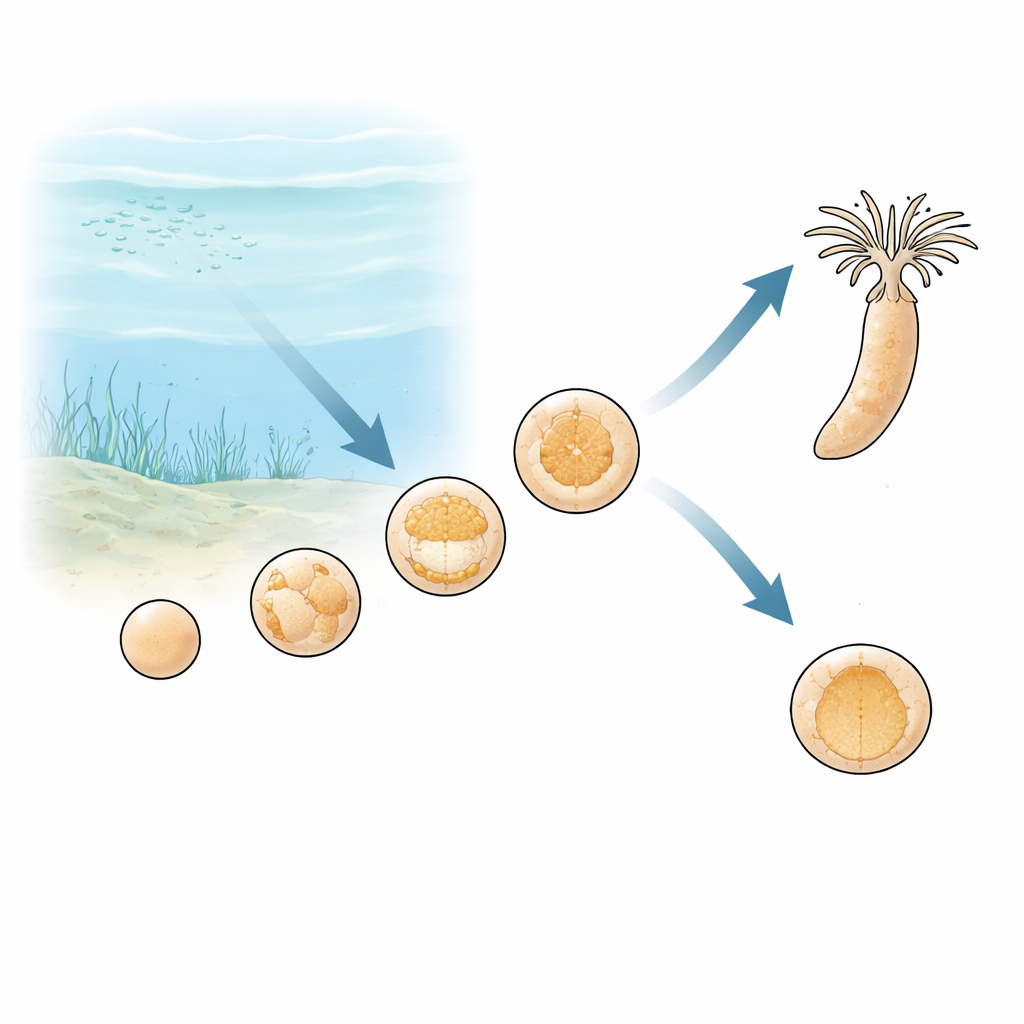
Pradawne oceany o zmiennym oddechu
Geolodzy uważają, że w erze neoproterozoicznej, ponad pół miliarda lat temu, tlen w oceanach nie tylko rósł i utrzymywał się na wysokim poziomie. Zamiast tego, zwłaszcza w płytkich przybrzeżnych morzach, w których żyły wczesne zwierzęta, poziomy tlenu prawdopodobnie wahały się w cyklach dziennych i sezonowych. Dla rozwijającego się organizmu takie wahania stanowiły poważny problem: budowanie złożonego ciała z pojedynczej komórki wymaga dużo energii, a ta energia zwykle pochodzi z metabolizmu zależnego od tlenu. Zespół wysunął hipotezę, że embriony zwierząt zajmujących wczesną pozycję w drzewie filogenetycznym mogą ujawnić, jak pierwsze metazoany przystosowały się do takich niestabilnych warunków.
Embrion anemony pod wpływem stresu
Badacze zwrócili się ku Nematostella vectensis, drobnej anemonie, która reprezentuje jedną z najwcześniejszych gałęzi drzewa zwierzęcego. Zbudowali ściśle kontrolowany system hodowlany, w którym przepływająca woda morska nad embrionami mogła być utrzymywana na normalnym poziomie tlenu lub sprowadzana do bardzo niskich wartości. W normalnych warunkach embriony przechodzą od luźnej kuli komórek do pustej sfery, a następnie do stadium zwanego gastrulacją, gdy komórki wciągają się do środka, tworząc podstawowe warstwy ciała. Gdy tlen został usunięty z wody przed lub w trakcie tego etapu fałdowania, rozwój nie zawalił się od razu. Zamiast tego embriony zatrzymały postęp i pozostały jako proste puste sfery, przy tym żywe i strukturalnie nienaruszone.
Wstrzymane, nie zniszczone
Aby sprawdzić, czy to zatrzymanie było trwałym uszkodzeniem czy kontrolowaną pauzą, zespół przywrócił tlen po kilku godzinach jego braku. Embriony, które zastały zatrzymane przed gastrulacją, wznowiły rozwój po opóźnieniu: warstwy komórkowe znów zaczęły się fałdować, a większość embrionów ostatecznie osiągnęła bardziej zaawansowane stadium gastruli. Testy znakujące dzielące się komórki ujawniły, co działo się wewnątrz. W niskim stężeniu tlenu kopiowanie DNA i podziały komórkowe praktycznie ustały. Już w ciągu jednej do dwóch godzin po reoksygenacji podziały komórek odbiły szybko, nawet zanim pojawiły się widoczne zmiany kształtu. Ten wzorzec pokazuje, że embriony wchodzą w odwracalne „quiescencyjne” (uśpione) stadium — wyciszając wzrost i ruch, aż do momentu, gdy dostępny będzie wystarczający tlen, by zasilić kolejne etapy.
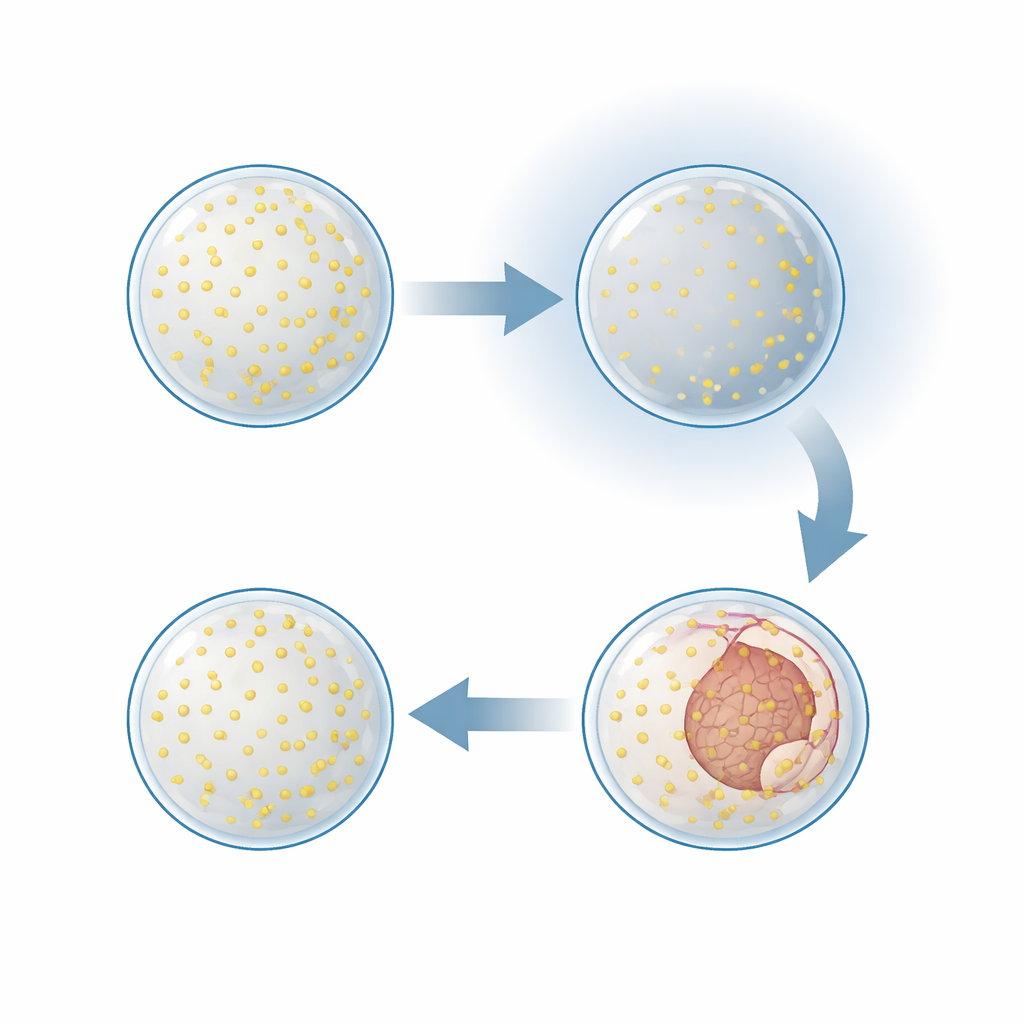
Geny wyczuwające i przystosowujące się do niskiego tlenu
Zespół następnie zbadał, które geny włączały się lub wyłączały w embrionach wystawionych na hipoksję na różnych etapach. Tysiące genów zmieniło swoją aktywność, przy najsilniejszych przesunięciach w młodszych embrionach, które były najbardziej wrażliwe na utratę tlenu. Dotknięte geny tworzyły wyraźne zestawy zależne od czasu rozwoju: na wczesnych etapach wiele z nich związanych było ze strukturami komórkowymi, obsługą chromosomów i innymi składnikami potrzebnymi do formowania tkanek; później więcej genów dotyczyło zarządzania użyciem energii, kontroli jakości białek i metabolizmu komórkowego. Pojawiły się także klasyczne ścieżki odpowiedzi na niski tlen znane z bardziej złożonych zwierząt. Kluczowe markery związane z systemem czynnika indukowanego hipoksją (HIF) oraz z sieciami odpowiedzi na stres, takimi jak sygnalizacja AMPK, odpowiedź na nieprawidłowo sfałdowane białka (unfolded protein response) i produkcja antyoksydantów, zostały aktywowane, mimo że niektóre zasadnicze geny przełącznikowe same w sobie nie zwiększyły obfitości. Ten wzorzec sugeruje, że molekularne narzędzia używane dziś przez zwierzęta do znoszenia niskiego poziomu tlenu już istniały w bardzo pradawnych liniach ewolucyjnych.
Co to oznacza dla historii zwierząt
W całości wyniki przedstawiają embrion anemony jako małego eksperta od przetrwania. Gdy tlen spada, nie umiera; aktywnie spowalnia cykl komórkowy, przekształca swoją aktywność genową i czeka w bezpiecznym trybie oczekiwania, aż warunki się poprawią, po czym rozwój jest wznawiany. Ponieważ te strategie są zbliżone do obserwowanych u robaków, owadów i kręgowców, badanie sugeruje, że wspólny, wrażliwy na tlen program genetyczny prawdopodobnie istniał u przodka współczesnych zwierząt. Dla czytelnika pozbawionego specjalistycznej wiedzy wniosek jest taki, że zdolność embrionów do wstrzymywania i ponownego uruchamiania wzrostu w odpowiedzi na zmiany poziomu tlenu mogła być kluczową innowacją, która pozwoliła złożonemu życiu zwierzęcemu rozkwitnąć w niestabilnych pradawnych morzach Ziemi.
Cytowanie: Hadife, S., Wang, H., Hongo, Y. et al. Hypoxia-induced gene expression changes in N. vectensis embryos. Sci Rep 16, 14315 (2026). https://doi.org/10.1038/s41598-026-44143-x
Słowa kluczowe: hipoksja, rozwój embrionalny, anemon morskie, zmiany poziomu tlenu, geny odpowiedzi na stres