Clear Sky Science · fr
Modifications de l’expression génique induites par l’hypoxie chez les embryons de N. vectensis
Pourquoi l’oxygène compte pour les tout petits embryons marins
Les premiers animaux de la Terre sont apparus dans des mers anciennes où les niveaux d’oxygène montaient et descendaient au fil du temps. Cette étude pose une question simple mais aux implications larges : comment de très jeunes embryons animaux font-ils face lorsqu’un apport en oxygène dont ils dépendent chute soudainement ? En observant les embryons d’une petite anémone de mer, les chercheurs ont montré comment la vie précoce peut mettre temporairement son développement en pause pendant des épisodes de faible oxygénation, puis redémarrer lorsque les conditions s’améliorent. Ces découvertes aident à imaginer ce que les premiers animaux ont affronté il y a des centaines de millions d’années — et comment les animaux d’aujourd’hui portent encore des traces moléculaires de ces défis.
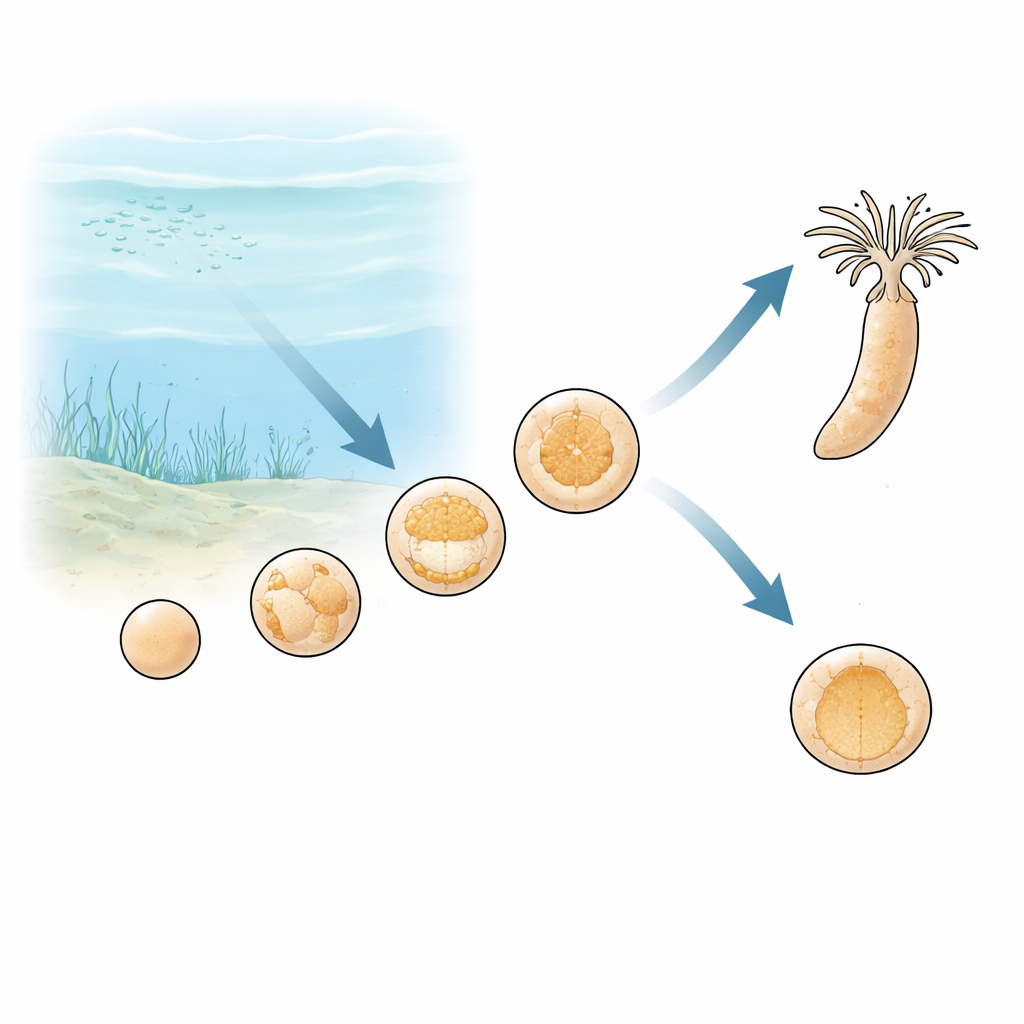
Des océans anciens au souffle changeant
Les géologues estiment que durant l’ère néoprotérozoïque, il y a plus d’un demi-milliard d’années, l’oxygène dans les océans n’a pas simplement augmenté puis resté élevé. Au contraire, notamment dans les mers côtières peu profondes où vivaient les premiers animaux, l’oxygène a probablement fluctué entre des niveaux plus riches et plus pauvres au fil des jours et des saisons. Pour tout animal en développement, de telles variations représentent un problème sérieux : construire un corps complexe à partir d’une seule cellule demande beaucoup d’énergie, et cette énergie provient généralement du métabolisme dépendant de l’oxygène. L’équipe a donc émis l’hypothèse que les embryons d’animaux appartenant aux branches anciennes pourraient révéler comment les premiers métazoaires se sont adaptés à ces conditions instables.
Un embryon d’anémone de mer sous stress
Les chercheurs se sont intéressés à Nematostella vectensis, une petite anémone de mer représentant l’une des branches les plus anciennes de l’arbre animal. Ils ont mis au point un système de culture strictement contrôlé dans lequel l’eau de mer circulant sur les embryons pouvait être maintenue à un niveau d’oxygène normal ou forcée à des niveaux extrêmement faibles. Dans des conditions normales, les embryons évoluent d’une masse lâche de cellules vers une sphère creuse, puis entrent en gastrulation, stade où les cellules s’infoldent pour former les couches corporelles de base. Lorsque l’oxygène était retiré de l’eau avant ou pendant cette phase d’infoldement, le développement ne s’effondrait pas complètement. Au lieu de cela, les embryons cessaient de progresser et restaient sous forme de sphères creuses simples, tout en restant vivants et structurellement intacts.
En pause, pas détruits
Pour déterminer si cet arrêt reflétait des dommages permanents ou une pause contrôlée, l’équipe a réintroduit de l’oxygène après plusieurs heures de privation. Les embryons qui s’étaient arrêtés avant la gastrulation ont repris le développement après un délai : les couches cellulaires ont recommencé à s’infoldre et la plupart des embryons ont finalement atteint le stade gastrula plus avancé. Des tests marquant les cellules en division ont montré ce qui se passait à l’intérieur. En faible oxygène, la réplication de l’ADN et la division cellulaire étaient presque complètement arrêtées. En une à deux heures seulement après la réoxygénation, la division cellulaire reprenait rapidement, avant même que les changements de forme visibles ne réapparaissent. Ce schéma montre que les embryons entrent dans un état réversible de « quiescence » — réduisant croissance et mouvement jusqu’à ce que suffisamment d’oxygène soit disponible pour alimenter les étapes suivantes.
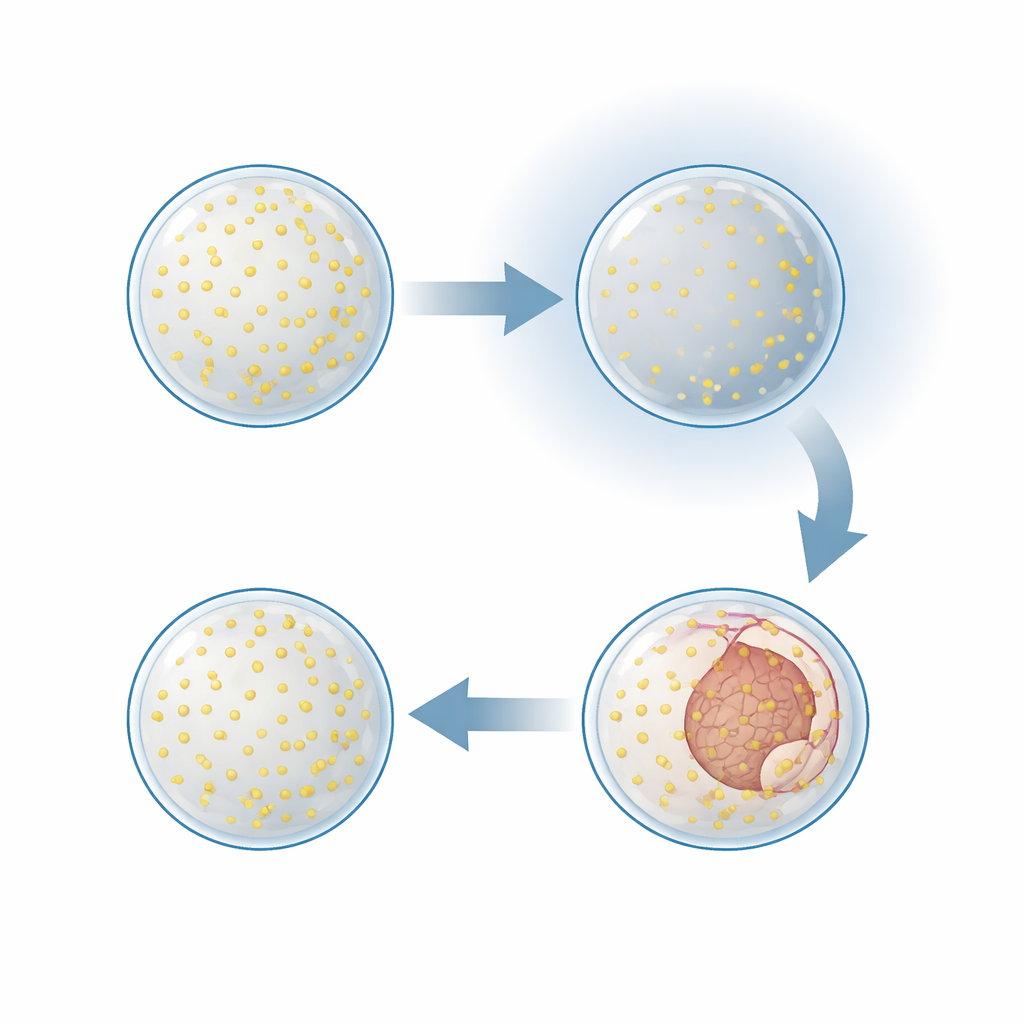
Des gènes qui détectent et s’adaptent au faible oxygène
L’équipe a ensuite examiné quels gènes s’activaient ou se désactivaient chez les embryons exposés à l’hypoxie à différents stades. Des milliers de gènes ont modifié leur activité, avec les variations les plus marquées chez les embryons plus jeunes, les plus sensibles à la perte d’oxygène. Les gènes affectés formaient des ensembles distincts selon le moment du développement : tôt, beaucoup étaient liés aux structures cellulaires, à la gestion des chromosomes et à d’autres composants nécessaires à la mise en forme des tissus ; plus tard, d’autres étaient davantage impliqués dans la gestion de l’utilisation de l’énergie, le contrôle de la qualité des protéines et le métabolisme cellulaire. Des voies classiques de réponse au faible oxygène connues chez des animaux plus complexes sont également apparues. Des gènes marqueurs clés associés au système Hypoxia Inducible Factor et à des réseaux de réponse au stress comme la signalisation AMPK, la réponse aux protéines non repliées et la production d’antioxydants ont été activés, bien que certains gènes centraux du commutateur n’aient pas eux-mêmes augmenté en abondance. Ce schéma suggère que la boîte à outils moléculaire utilisée aujourd’hui par les animaux pour supporter les faibles niveaux d’oxygène était déjà présente dans des lignées très anciennes.
Ce que cela signifie pour l’histoire des animaux
Pris dans leur ensemble, les résultats dessinent le portrait d’un embryon d’anémone comme d’un petit maître de la survie. Quand l’oxygène baisse, il ne meurt pas simplement ; il ralentit activement son cycle cellulaire, reconfigure son activité génique et attend dans un mode de maintien sûr jusqu’à ce que les conditions s’améliorent, moment où le développement reprend. Parce que ces stratégies ressemblent étroitement à celles observées chez des vers, des insectes et des vertébrés, l’étude soutient qu’un programme génétique sensible à l’oxygène et partagé était probablement en place chez l’ancêtre commun des animaux modernes. Pour un lecteur non spécialiste, la conclusion est que la capacité des embryons à mettre en pause puis à relancer leur croissance en réponse à la variation de l’oxygène a peut‑être été une innovation clé ayant permis à la vie animale complexe de prospérer dans les mers anciennes instables de la Terre.
Citation: Hadife, S., Wang, H., Hongo, Y. et al. Hypoxia-induced gene expression changes in N. vectensis embryos. Sci Rep 16, 14315 (2026). https://doi.org/10.1038/s41598-026-44143-x
Mots-clés: hypoxie, développement embryonnaire, anémone de mer, évolution de l’oxygène, gènes de réponse au stress