Clear Sky Science · nl
Hypoxie-geïnduceerde veranderingen in genexpressie in N. vectensis-embryo's
Waarom zuurstof belangrijk is voor kleine zee-embryo’s
De eerste dieren op aarde ontstonden in oeroude zeeën waar het zuurstofgehalte in de loop van de tijd op en neer ging. Deze studie stelt een eenvoudige maar verstrekkende vraag: hoe gaan zeer jonge dierlijke embryo’s om met een plotselinge daling van het zuurstof waarvan ze afhankelijk zijn? Door de embryo’s van een kleine zeeanemoon te observeren, ontdekten de onderzoekers hoe het vroege leven zijn ontwikkeling tijdelijk kan pauzeren tijdens perioden met weinig zuurstof en daarna weer kan hervatten wanneer de omstandigheden verbeteren. Deze inzichten helpen ons voor te stellen welke uitdagingen vroege dieren honderden miljoenen jaren geleden hebben gekend — en hoe hedendaagse dieren nog steeds moleculaire sporen van die uitdagingen dragen.
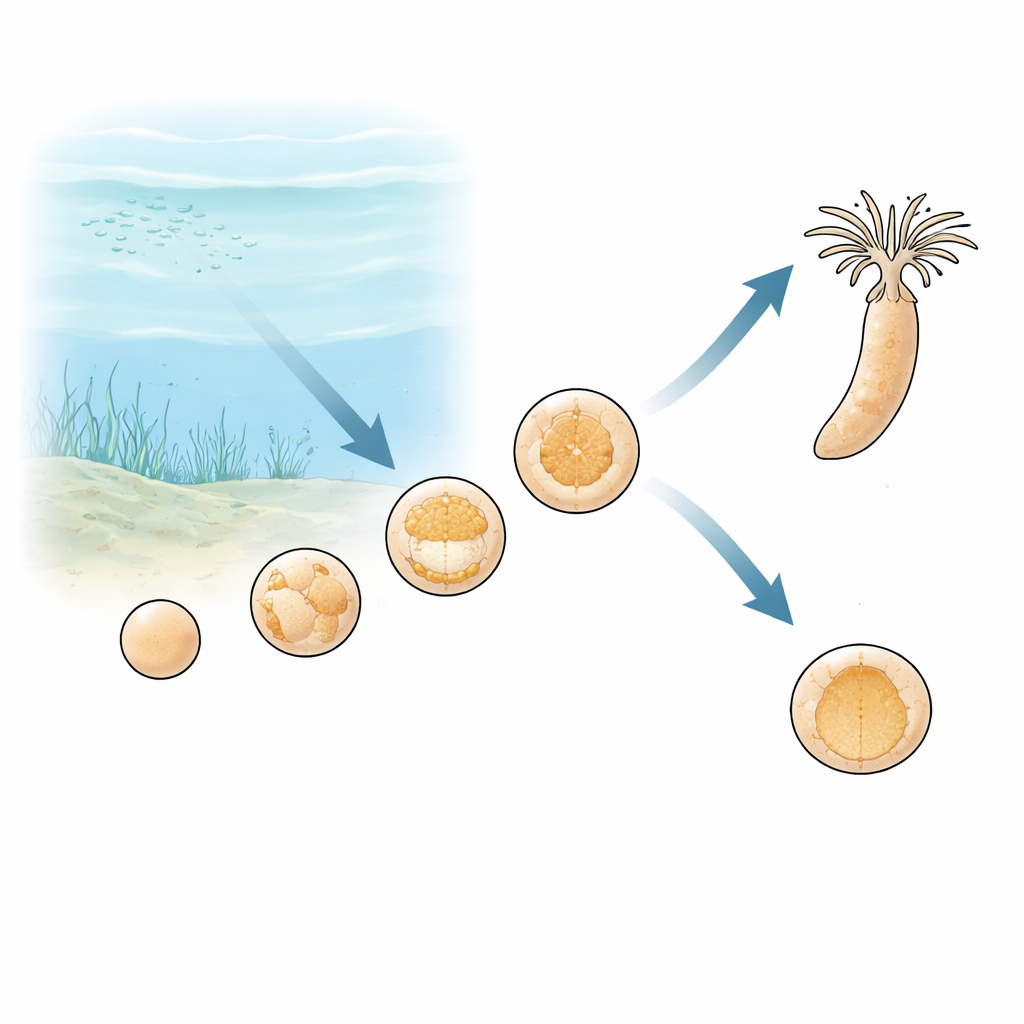
Oeroude oceanen met wisselende ademhaling
Geologen denken dat tijdens het Neoproterozoïcum, meer dan een half miljard jaar geleden, zuurstof in de oceanen niet eenvoudigweg omhoog ging en hoog bleef. In plaats daarvan schommelde het, vooral in ondiepe kustzeeën waar vroege dieren leefden, waarschijnlijk tussen rijkere en armere niveaus over dagen en seizoenen. Voor elk zich ontwikkelend dier zouden zulke schommelingen een serieus probleem vormen: het opbouwen van een complex lichaam uit één enkele cel vergt veel energie, en die energie komt gewoonlijk uit zuurstofgebonden metabolisme. Het team redeneerde dat embryo’s van vroeg aftakkende dieren kunnen onthullen hoe de eerste metazoën zich aan dergelijke onstabiele omstandigheden aanpasten.
Een zeeanemoonembryo onder stress
De onderzoekers bestudeerden Nematostella vectensis, een sterretje onder de zeeanemonen dat een van de vroegste takken van de dierenboom vertegenwoordigt. Ze bouwden een nauwkeurig gecontroleerd kweeksysteem waarin het zeewater dat over embryo’s stroomt op normaal zuurstofniveau kan worden gehouden of tot extreem lage waarden kan worden teruggebracht. Onder normale omstandigheden gaan de embryo’s van een losse celbol naar een holle bol en vervolgens naar een stadium dat gastrulatie wordt genoemd, wanneer cellen naar binnen vouwen om de basislichaamslagen te vormen. Wanneer zuurstof uit het water werd gehaald vóór of tijdens deze vouwfase, stortte de ontwikkeling niet volledig in. In plaats daarvan stopten embryo’s met voortgang en bleven ze als eenvoudige holle bollen, maar ze bleven leven en structureel intact.
Gepauzeerd, niet kapot
Om te bepalen of deze stilstand blijvende beschadiging of een gecontroleerde pauze was, herstelde het team de zuurstoftoevoer na enkele uren van tekort. Embryo’s die vóór de gastrulatie waren stilgevallen, hervatten de ontwikkeling na een vertraging: de cellagen begonnen opnieuw naar binnen te vouwen en de meeste embryo’s bereikten uiteindelijk het meer gevorderde gastrulastadium. Tests die delende cellen labelen lieten zien wat er vanbinnen gebeurde. Bij weinig zuurstof stopten DNA-replicatie en celdeling vrijwel volledig. Binnen slechts één tot twee uur na re-oxygenatie herstelde de celdeling zich snel, zelfs voordat zichtbare vormveranderingen terugkeerden. Dit patroon toont aan dat de embryo’s in een omkeerbare “quiescente” toestand gaan — ze zetten groei en beweging terug totdat er voldoende zuurstof beschikbaar is om de volgende stappen aan te drijven.
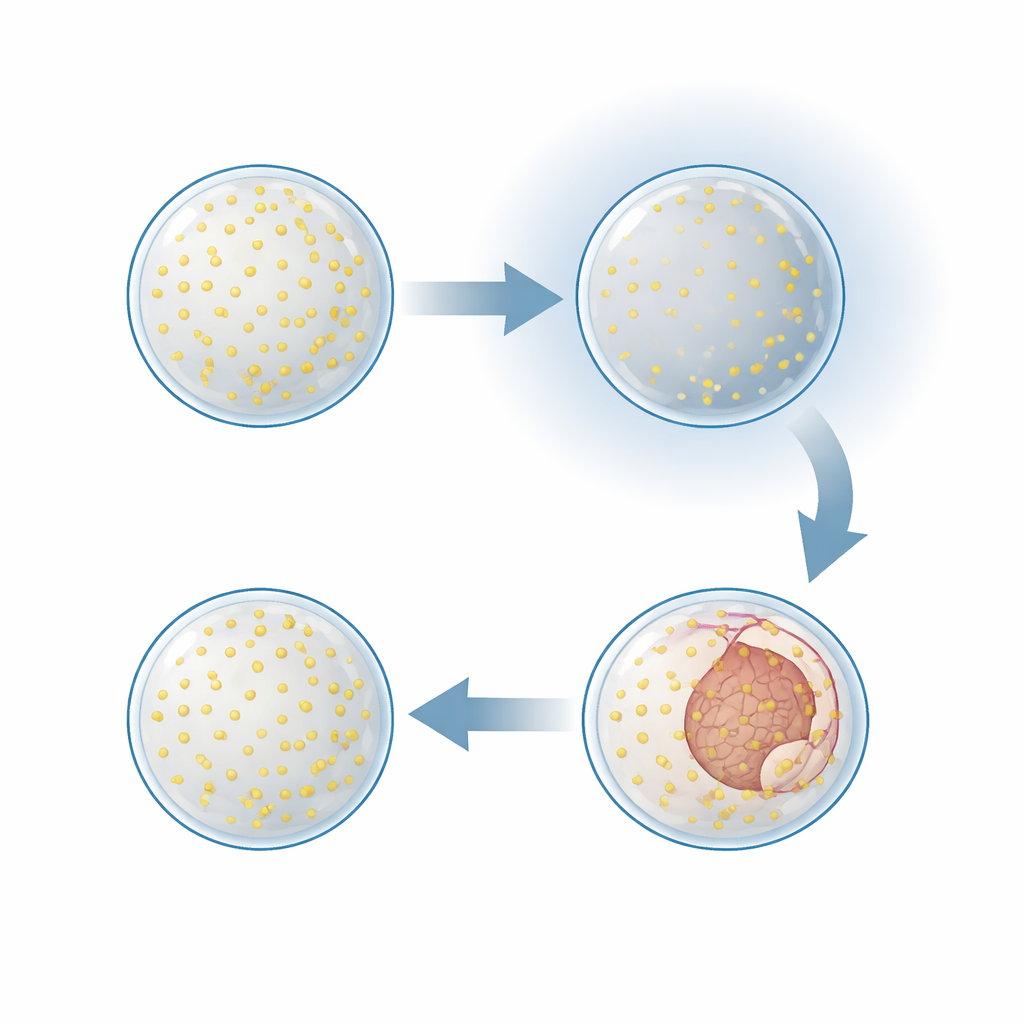
Genen die lage zuurstof detecteren en zich aanpassen
Het team onderzocht vervolgens welke genen aan- of uitgingen in embryo’s die in verschillende stadia aan hypoxie werden blootgesteld. Duizenden genen veranderden hun activiteit, met de sterkste verschuivingen in jongere embryo’s die het meest gevoelig waren voor zuurstofverlies. De aangetaste genen vormden verschillende groepen, afhankelijk van het ontwikkelingsmoment: vroeg waren veel genen verbonden met celstructuren, chromosoomverwerking en andere componenten die nodig zijn voor weefselvorming; later waren er meer genen betrokken bij het beheren van energiegebruik, eiwitkwaliteitscontrole en celmetabolisme. Klassieke lage-zuurstofroutes die bekend zijn van meer complexe dieren verschenen ook. Belangrijke markergenen geassocieerd met het Hypoxia Inducible Factor-systeem en met stress-responsnetwerken zoals AMPK-signaalvoering, de unfolded protein response en antioxidantproductie werden geactiveerd, ondanks dat sommige kernschakelaars zelf niet in hoeveelheid toenamen. Dit patroon suggereert dat de moleculaire gereedschapskist die dieren vandaag gebruiken om lage zuurstof te doorstaan al aanwezig was in zeer oude lijnages.
Wat dit betekent voor het verhaal van dieren
Gezien in samenhang portretteren de resultaten het anemoonembryo als een klein overlevingstalent. Wanneer zuurstof daalt, sterft het niet simpelweg; het vertraagt actief zijn celdeling, herschikt zijn genactiviteit en wacht in een veilige pauzestand tot de omstandigheden verbeteren, waarna de ontwikkeling hervat wordt. Omdat deze strategieën sterk lijken op die bij wormen, insecten en gewervelden, betoogt de studie dat een gedeeld, zuurstofgevoelig genetisch programma waarschijnlijk aanwezig was in de gemeenschappelijke voorouder van moderne dieren. Voor een niet-specialist is de kernboodschap dat het vermogen van embryo’s om groei te pauzeren en opnieuw te starten als reactie op veranderende zuurstof mogelijk een sleutelinnovatie was die complex dierlijk leven in de onstabiele oerzeeën van de aarde liet gedijen.
Bronvermelding: Hadife, S., Wang, H., Hongo, Y. et al. Hypoxia-induced gene expression changes in N. vectensis embryos. Sci Rep 16, 14315 (2026). https://doi.org/10.1038/s41598-026-44143-x
Trefwoorden: hypoxie, embryonale ontwikkeling, zeeanemoon, zuurstofregeling, stress-responsgenen