Clear Sky Science · de
Hypoxie-induzierte Genexpressionsänderungen in Embryonen von N. vectensis
Warum Sauerstoff für winzige Meeresembryonen wichtig ist
Die ersten Tiere der Erde entstanden in urzeitlichen Meeren, in denen der Sauerstoffgehalt im Laufe der Zeit anstieg und wieder fiel. Diese Studie stellt eine einfache, aber weitreichende Frage: Wie kommen sehr junge Tierembryonen zurecht, wenn der für sie verfügbare Sauerstoff plötzlich sinkt? Anhand der Embryonen einer kleinen Seeanemone zeigten die Forschenden, wie das frühe Leben seine Entwicklung während Sauerstoffmangelphasen vorübergehend aussetzen und nach Besserung der Bedingungen wieder aufnehmen kann. Diese Erkenntnisse helfen uns zu verstehen, welchen Herausforderungen frühes tierisches Leben vor Hunderten von Millionen Jahren gegenüberstand — und wie heutige Tiere noch molekulare Spuren dieser Herausforderungen tragen.
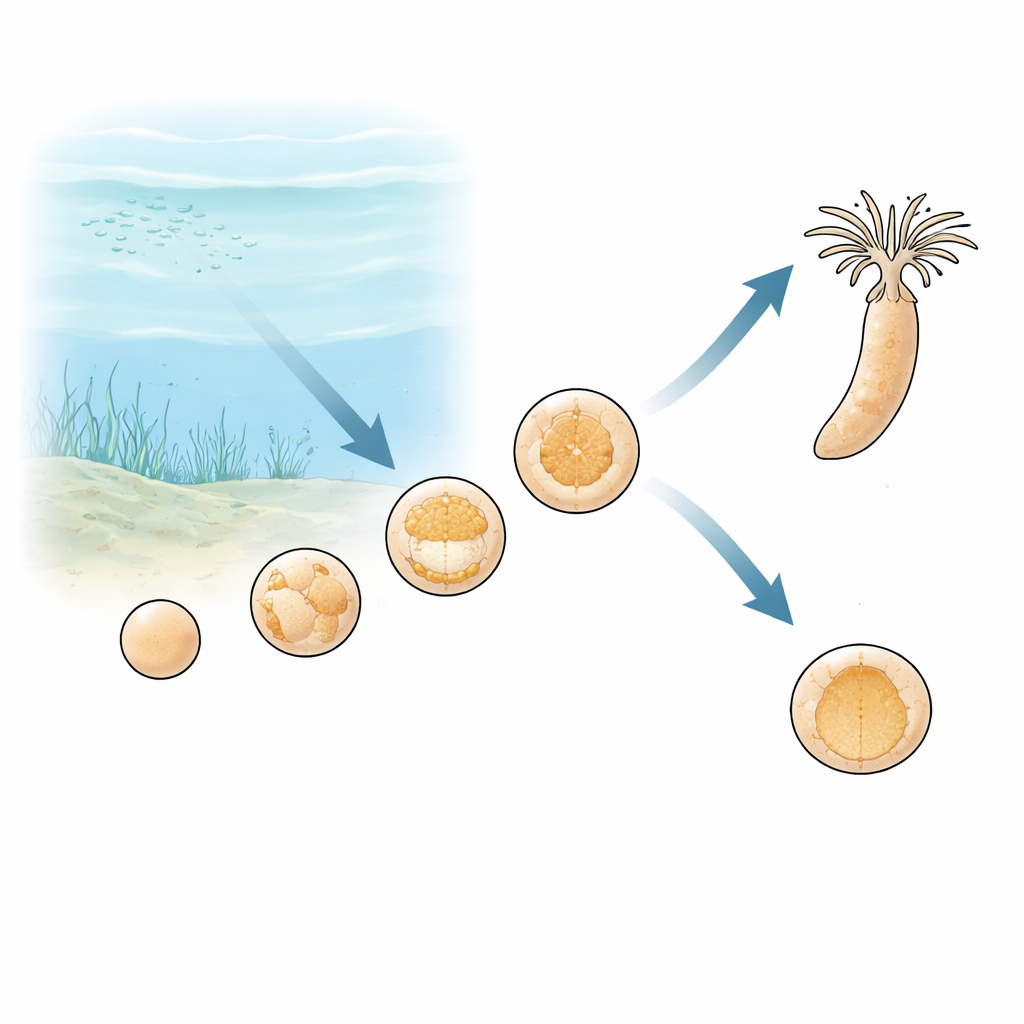
Uralte Ozeane mit schwankender Atemluft
Geologen vermuten, dass während des Neoproterozoikums, also vor mehr als einer halben Milliarde Jahren, der Sauerstoffgehalt in den Ozeanen nicht einfach kontinuierlich anstieg und hoch blieb. Stattdessen schwankte er vermutlich, besonders in flachen Küstenmeeren, in denen frühe Tiere lebten, über Tage und Jahreszeiten hinweg zwischen höheren und niedrigeren Werten. Für jedes sich entwickelnde Tier wären solche Schwankungen ein ernstes Problem: Aus einer einzelnen Zelle einen komplexen Körper zu bauen kostet viel Energie, und diese Energie stammt meist aus sauerstoffabhängigem Stoffwechsel. Das Team vermutete, dass Embryonen früh aufgetrennter Tiergruppen zeigen könnten, wie die ersten Metazoen sich an solche instabilen Bedingungen anpassten.
Ein Seeanemonen-Embryo unter Stress
Die Forschenden verwendeten Nematostella vectensis, eine Sternchen-Seeanemone, die einen der frühesten Zweige im Tierstammbaum repräsentiert. Sie bauten ein streng kontrolliertes Kultursystem, in dem das Meerwasser über die Embryonen entweder auf normalem Sauerstoffniveau gehalten oder auf extrem niedrige Werte abgesenkt werden konnte. Unter normalen Bedingungen entwickeln sich die Embryonen von einer lockeren Zellkugel zu einer hohlen Kugel und weiter zur Gastrulation, wenn Zellen nach innen falten und die grundlegenden Körperscheiden bilden. Wurde dem Wasser vor oder während dieser Faltungsphase der Sauerstoff entzogen, brach die Entwicklung nicht komplett zusammen. Stattdessen stoppten die Embryonen den Fortschritt und blieben als einfache hohle Kugeln erhalten, blieben dabei aber lebendig und strukturell intakt.
Ausgesetzt, nicht zerstört
Um zu prüfen, ob dieser Stopp bleibende Schäden oder eine kontrollierte Pause war, stellten die Forschenden nach mehreren Stunden ohne Sauerstoff den Sauerstoff wieder her. Embryonen, die vor der Gastrulation gestoppt hatten, nahmen die Entwicklung nach einer Verzögerung wieder auf: Zellschichten begannen erneut, sich einzufalten, und die meisten Embryonen erreichten schließlich das fortgeschrittenere Gastrula-Stadium. Markertests für teilende Zellen zeigten, was im Inneren geschah. Bei niedrigem Sauerstoff ruhten DNA-Replikation und Zellteilung nahezu vollständig. Innerhalb von nur ein bis zwei Stunden nach Reoxygenierung setzte die Zellteilung rasch wieder ein, noch bevor sichtbare Formveränderungen zurückkehrten. Dieses Muster zeigt, dass die Embryonen einen reversiblen „quieszenten“ Zustand einnehmen — sie drosseln Wachstum und Bewegung, bis wieder genügend Sauerstoff zur Verfügung steht, um die nächsten Entwicklungsschritte anzutreiben.
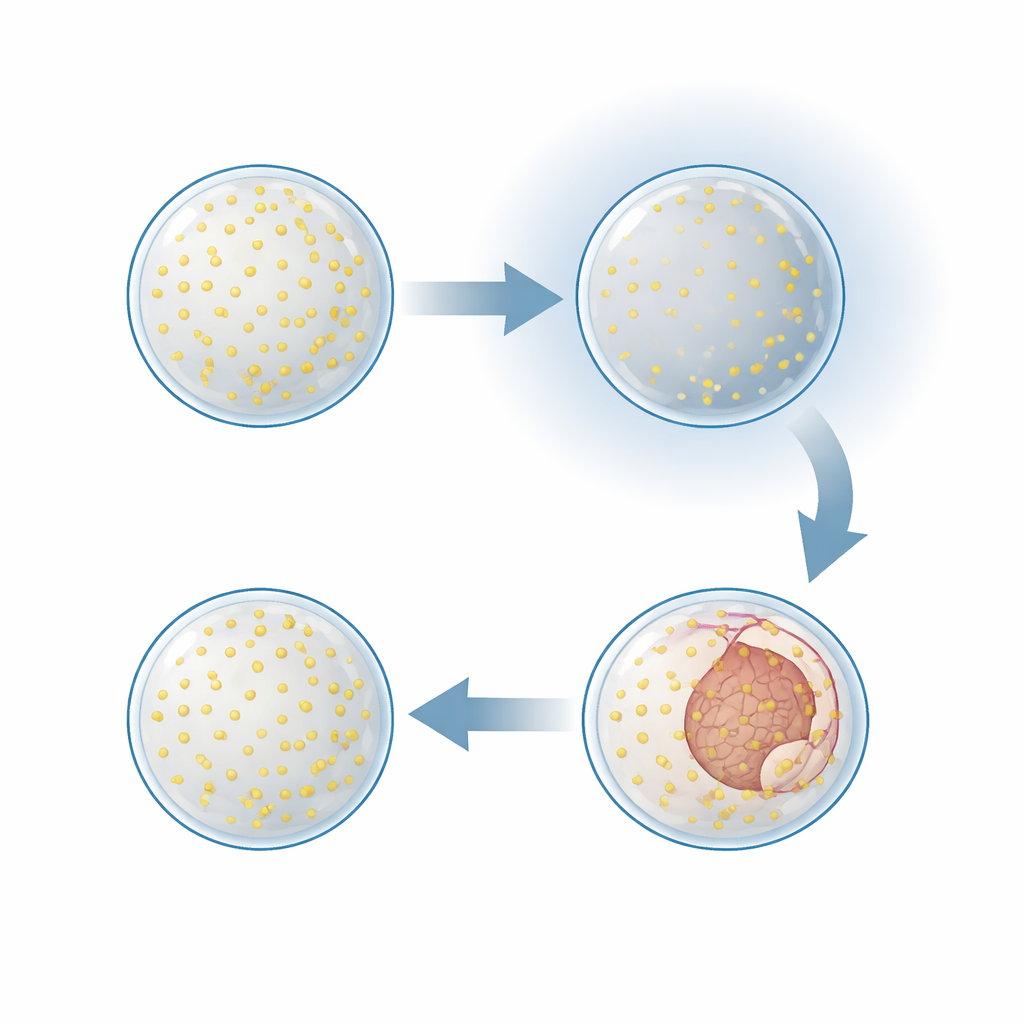
Gene, die niedrigen Sauerstoff wahrnehmen und sich anpassen
Das Team untersuchte anschließend, welche Gene in Embryonen, die in verschiedenen Stadien Hypoxie ausgesetzt waren, an- oder abgeschaltet wurden. Tausende Gene veränderten ihre Aktivität, wobei die stärksten Verschiebungen in jüngeren Embryonen auftraten, die am empfindlichsten gegenüber Sauerstoffverlust waren. Die betroffenen Gene bildeten zeitabhängige, unterschiedliche Gruppen: Früh waren viele Gene mit Zellstrukturen, Chromosomenhandhabung und anderen Komponenten verknüpft, die für die Gewebeformung nötig sind; später betrafen viele Gene das Energiemanagement, die Proteinqualitätskontrolle und den Zellstoffwechsel. Auch klassische Niedrigsauerstoff-Wege, die aus komplexeren Tieren bekannt sind, traten hervor. Schlüssel-Marker-Gene, die mit dem Hypoxia Inducible Factor-System und mit Stressreaktionsnetzwerken wie AMPK-Signalgebung, der Antwort auf fehlgefaltete Proteine und der Produktion von Antioxidantien assoziiert sind, wurden aktiviert, obwohl einige zentrale Schaltgene selbst nicht in ihrer Menge anstiegen. Dieses Muster legt nahe, dass das molekulare Repertoire, das Tiere heute zur Bewältigung von Sauerstoffmangel nutzen, bereits in sehr alten Linien vorhanden war.
Was das für die Geschichte der Tiere bedeutet
Im Überblick zeichnen die Ergebnisse das Bild eines embryonalen Überlebenskünstlers bei der Seeanemone. Sinkt der Sauerstoff, stirbt der Embryo nicht einfach; er verlangsamt aktiv seinen Zellzyklus, verändert seine Genaktivität und verharrt in einem sicheren Wartemodus, bis sich die Bedingungen bessern und die Entwicklung fortgesetzt werden kann. Da diese Strategien denen ähneln, die in Würmern, Insekten und Wirbeltieren beobachtet werden, legt die Studie nahe, dass ein gemeinsames, sauerstoffsensitives genetisches Programm wahrscheinlich schon im gemeinsamen Vorfahren moderner Tiere vorhanden war. Für eine nichtfachliche Leserschaft ist die Schlussfolgerung, dass die Fähigkeit von Embryonen, Wachstum angesichts wechselnder Sauerstoffbedingungen zu pausieren und wieder aufzunehmen, eine Schlüsselinnovation gewesen sein könnte, die dem Aufblühen komplexen tierischen Lebens in den instabilen Urmeeren der Erde ermöglichte.
Zitation: Hadife, S., Wang, H., Hongo, Y. et al. Hypoxia-induced gene expression changes in N. vectensis embryos. Sci Rep 16, 14315 (2026). https://doi.org/10.1038/s41598-026-44143-x
Schlüsselwörter: Hypoxie, Embryonalentwicklung, Seeanemone, Sauerstoffentwicklung, Stressantwort-Gene