Clear Sky Science · es
Cambios en la expresión génica inducidos por hipoxia en embriones de N. vectensis
Por qué el oxígeno importa para los diminutos embriones marinos
Los primeros animales de la Tierra surgieron en mares antiguos donde los niveles de oxígeno subían y bajaban con el tiempo. Este estudio plantea una pregunta sencilla pero de gran alcance: ¿cómo afrontan los embriones animales muy jóvenes la situación cuando el oxígeno del que dependen cae de forma repentina? Observando los embriones de una pequeña anémona de mar, los investigadores descubrieron cómo la vida temprana puede pausar temporalmente su propio desarrollo durante episodios de baja oxigenación y luego reanudarlo cuando las condiciones mejoran. Estos hallazgos nos ayudan a imaginar a qué se enfrentó la vida animal primitiva hace cientos de millones de años y cómo los animales actuales aún conservan rastros moleculares de esos desafíos.
Océanos antiguos con respiración cambiante
Los geólogos consideran que durante el Neoproterozoico, hace más de quinientos millones de años, el oxígeno en los océanos no subió y se mantuvo alto de forma permanente. Más bien, sobre todo en mares costeros someros donde vivían los primeros animales, el oxígeno probablemente fluctuó entre niveles más y menos abundantes a lo largo de días y estaciones. Para cualquier animal en desarrollo, tales oscilaciones suponen un problema serio: construir un cuerpo complejo a partir de una sola célula requiere mucha energía, y esa energía suele provenir del metabolismo dependiente del oxígeno. El equipo razonó que los embriones de animales de linajes tempranos podrían revelar cómo los primeros metazoos se adaptaron a condiciones tan inestables.
Un embrión de anémona en estrés
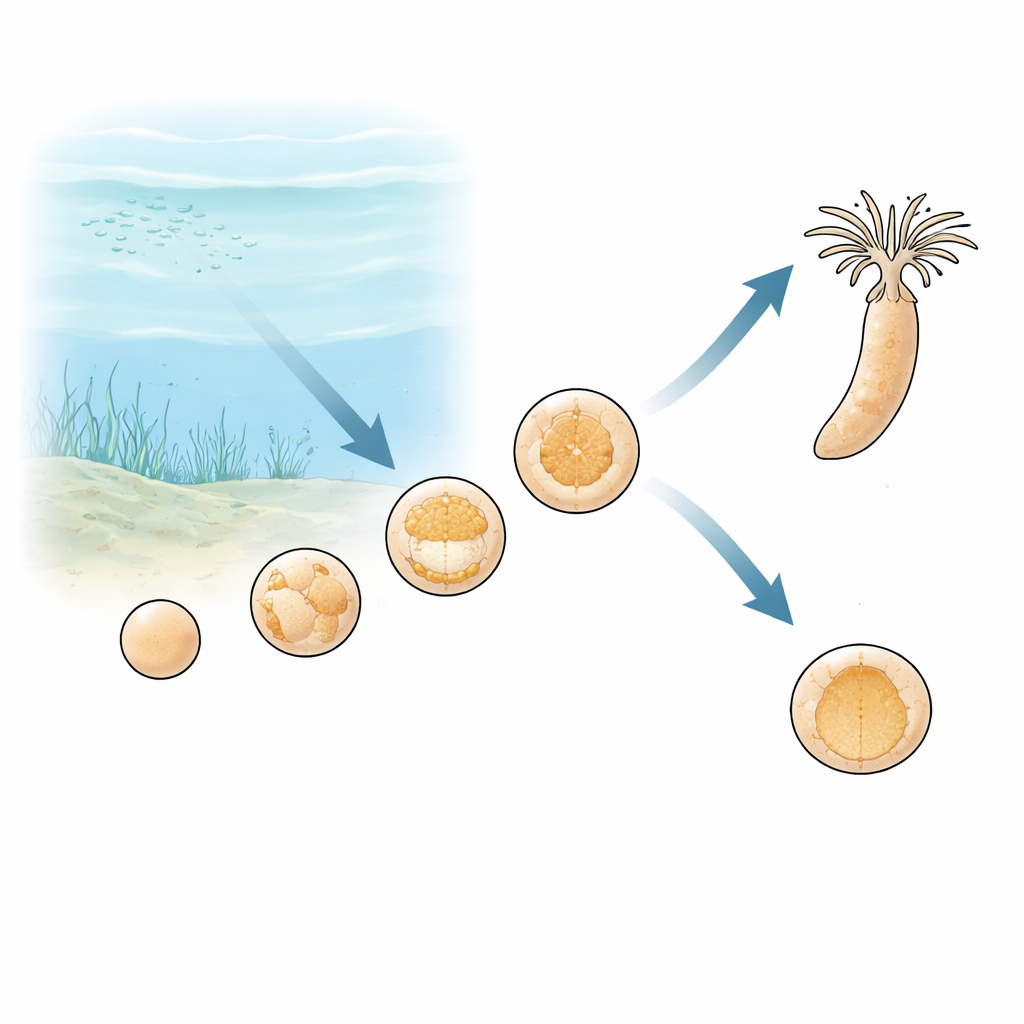
Los investigadores se centraron en Nematostella vectensis, una anémona de mar que representa una de las ramas más antiguas del árbol filogenético animal. Diseñaron un sistema de cultivo muy controlado en el que el agua de mar que fluía sobre los embriones podía mantenerse con oxígeno normal o reducirse a niveles extremadamente bajos. En condiciones normales, los embriones pasan de una masa suelta de células a una esfera hueca y después a una etapa llamada gastrulación, cuando las células se pliegan hacia el interior para formar las capas corporales básicas. Cuando el oxígeno se eliminó del agua antes o durante esta etapa de plegamiento, el desarrollo no colapsó por completo. En su lugar, los embriones dejaron de progresar y permanecieron como esferas huecas simples, aunque siguieron vivos y estructuralmente intactos.
Pausados, no destruidos
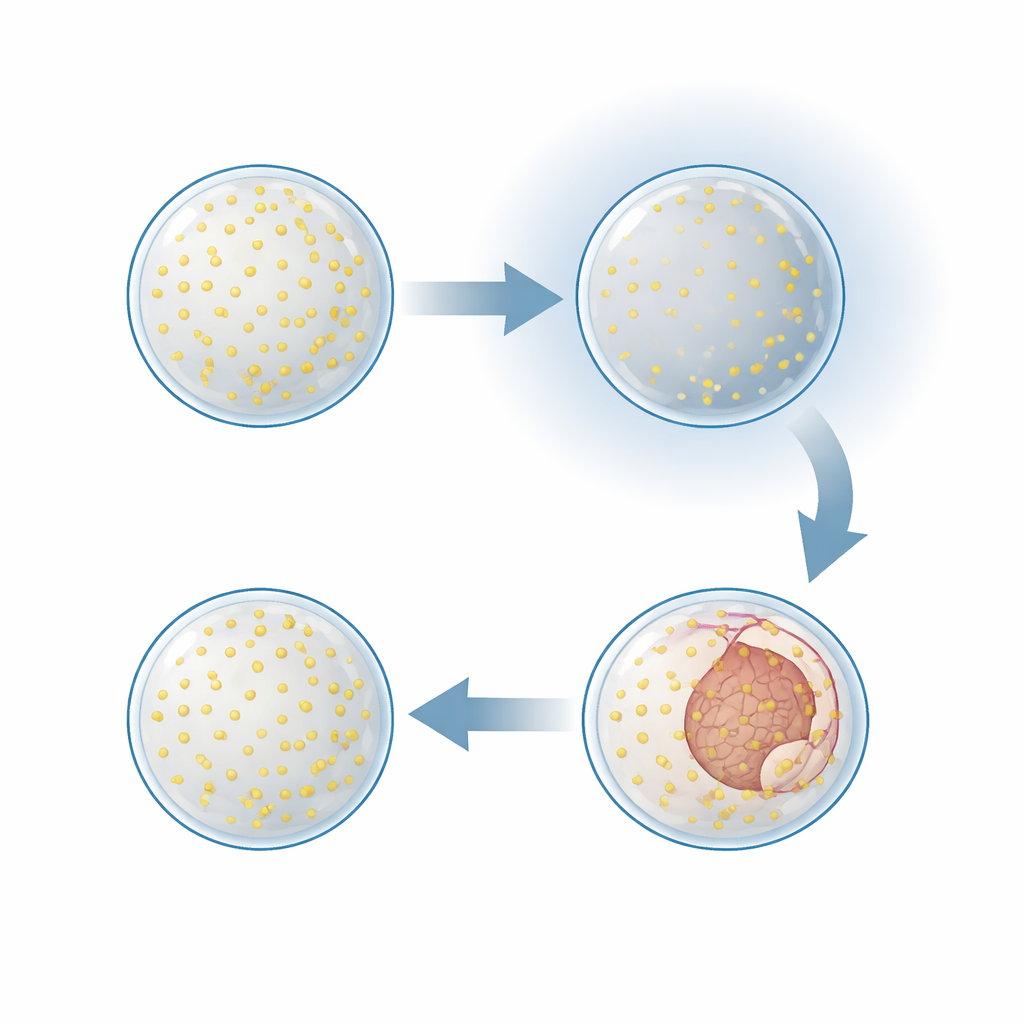
Para comprobar si esta detención era un daño permanente o una pausa controlada, el equipo restauró el oxígeno tras varias horas de privación. Los embriones que se habían detenido antes de la gastrulación reanudaron el desarrollo tras un retraso: las capas celulares volvieron a plegarse y la mayoría de los embriones alcanzó finalmente la etapa de gástrula más avanzada. Ensayos que marcan las células en división mostraron lo que ocurría en su interior. En baja oxigenación, la replicación del ADN y la división celular prácticamente se detuvieron. En apenas una o dos horas tras la reoxigenación, la división celular se recuperó rápidamente, incluso antes de que regresaran los cambios morfológicos visibles. Este patrón indica que los embriones entran en un estado reversible de “quiescencia”: reducen crecimiento y movimiento hasta que hay suficiente oxígeno para impulsar los siguientes pasos.
Genes que detectan y se adaptan a la baja oxigenación
El equipo examinó después qué genes se activaron o silenciaron en embriones expuestos a hipoxia en distintas etapas. Miles de genes cambiaron su actividad, con los cambios más marcados en embriones más jóvenes, que eran los más sensibles a la pérdida de oxígeno. Los genes afectados formaron conjuntos distintos según el momento del desarrollo: en fases tempranas muchos estaban vinculados a estructuras celulares, manejo de cromosomas y otros componentes necesarios para el moldeado de tejidos; más tarde, un mayor número se relacionó con la gestión del uso de la energía, el control de la calidad proteica y el metabolismo celular. También aparecieron vías clásicas de baja oxigenación conocidas en animales más complejos. Genes marcadores clave asociados al sistema del factor inducible por hipoxia (HIF) y a redes de respuesta al estrés como la señalización AMPK, la respuesta a proteínas desplegadas (unfolded protein response) y la producción de antioxidantes se activaron, aunque algunos genes con función de interruptor centrales no aumentaron su abundancia. Este patrón sugiere que el conjunto molecular que los animales usan hoy para soportar bajos niveles de oxígeno ya estaba presente en linajes muy antiguos.
Qué significa esto para la historia de los animales
Vistos en conjunto, los resultados presentan al embrión de anémona como un pequeño artista de la supervivencia. Cuando el oxígeno disminuye, no muere simplemente; reduce activamente su ciclo celular, reconfigura la actividad génica y espera en un estado de espera seguro hasta que las condiciones mejoran, momento en el que el desarrollo se reanuda. Dado que estas estrategias se parecen mucho a las observadas en gusanos, insectos y vertebrados, el estudio sostiene que un programa genético sensible al oxígeno y compartido probablemente ya existía en el ancestro común de los animales modernos. Para un lector general, la conclusión es que la capacidad de los embriones de pausar y reiniciar el crecimiento en respuesta a cambios en el oxígeno pudo haber sido una innovación clave que permitió que la vida animal compleja prosperara en los mares inestables de la Tierra primitiva.
Cita: Hadife, S., Wang, H., Hongo, Y. et al. Hypoxia-induced gene expression changes in N. vectensis embryos. Sci Rep 16, 14315 (2026). https://doi.org/10.1038/s41598-026-44143-x
Palabras clave: hipoxia, desarrollo embrionario, anémona de mar, evolución del oxígeno, genes de respuesta al estrés