Clear Sky Science · pl
AVPDN: uczenie odpornych na ruch i adaptacyjnych względem skali reprezentacji do wykrywania polipów w dynamicznych klatkach kolonoskopii
Dlaczego wykrywanie małych zmian jest ważne
Większość raków jelita grubego zaczyna się jako niewielkie narośla zwane polipami na wyściółce jelita. Podczas kolonoskopii lekarze starają się je zlokalizować i usunąć, zanim staną się niebezpieczne. Nowoczesne endoskopy rejestrują cały przebieg badania, ale kamera szybko się porusza, obraz często bywa rozmyty lub pełen odblasków, a polipy mogą być bardzo małe i trudne do zauważenia. W pracy tej przedstawiono nowy system komputerowy, który uczy się „widzieć” przez wizualny chaos rzeczywistych nagrań kolonoskopii, pomagając lekarzom wykrywać więcej polipów dokładnie i w czasie rzeczywistym.
Wyzwanie poruszającej się kamery
Kolonoskopia nie przypomina robienia statycznego zdjęcia — bardziej przypomina kręcenie chwiejnego, zbliżeniowego filmu wewnątrz ciała. W miarę przesuwania się endoskopu kamera trzęsie się i obraca, ściana jelita kurczy się, a przed obiektywem pojawiają się płyny i bąbelki powietrza. Ruchy te powodują rozmycie ruchu, jasne białe refleksy i nagłe zmiany pozornej wielkości tych samych struktur między klatkami. Małe polipy mogą wyglądać niemal identycznie jak fałdy tkanki i chwilowo znikać za bąbelkami lub odblaskami. Większość istniejących systemów widzenia komputerowego była pierwotnie tworzona z myślą o zdjęciach naturalnych lub zwykłych nagraniach, gdzie kamera jest stabilniejsza, a obiekty łatwiej odróżnić od tła, więc mają one trudności w takim ekstremalnym środowisku.
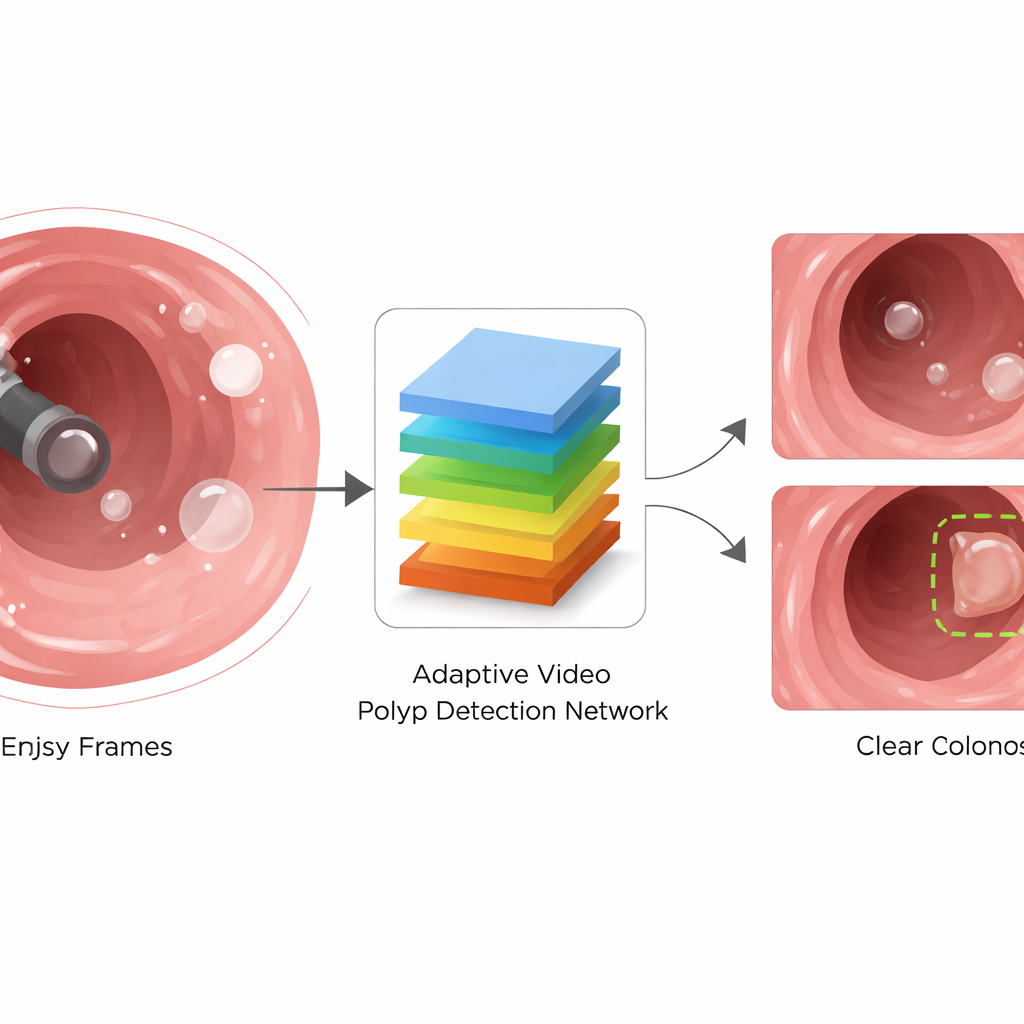
Inteligentniejszy sposób analizowania wideo kolonoskopii
Aby poradzić sobie z tymi problemami, autorzy proponują Adaptive Video Polyp Detection Network (AVPDN). W swej istocie AVPDN traktuje każdą klatkę wideo jako obraz i przepuszcza ją przez standardowy ekstraktor cech, który wychwytuje krawędzie, faktury i kolory. Zamiast na tym skończyć, dodaje jednak wyspecjalizowany etap „wzmacniania” zaprojektowany specjalnie dla kolonoskopii. Etap ten składa się z powtarzalnych bloków, które oczyszczają zaszumione sygnały, wzmacniają prawdziwie polipopodobne wzorce i śledzą polipy o wielu różnych rozmiarach. Co ważne, metoda działa na pojedynczych klatkach bez konieczności analizowania długich fragmentów wideo w czasie, co utrzymuje system wystarczająco szybkim do użycia w czasie rzeczywistym.
Filtrowanie szumu przy zachowaniu istotnych wskazówek
Pierwszy kluczowy blok nazywa się Adaptive Feature Interaction and Augmentation. Mówiąc prościej, analizuje on cechy obrazu na dwa różne sposoby jednocześnie. Jedna gałąź uwzględnia szerokie powiązania w całym obrazie, co pomaga zrozumieć ogólną scenę i nie przeoczyć odległych wskazówek o polipie. Druga gałąź jest bardziej selektywna: silnie przytłumia części obrazu o słabych lub niespójnych wzorcach, takich jak rozmycia czy odblaski. System uczy się następnie, ile ufać każdej z gałęzi dla danej klatki, mieszając je adaptacyjnie. Sprytne przetasowanie kanałów („channel shuffle”) miesza informacje między różnymi grupami cech, zachęcając sieć do odkrywania bogatszych kombinacji faktury i kształtu, które odróżniają prawdziwe polipy od niegroźnych fałdów i plamek.
Wykrywanie polipów w wielu skalach
Drugi kluczowy blok nazywa się Scale-Aware Context Integration. Polipy mogą być bardzo małe, gdy kamera jest dalej, i znacznie większe, gdy endoskop się do nich zbliża, więc system musi działać w szerokim zakresie rozmiarów. Moduł ten patrzy na scenę przez wiele „wirtualnych obiektywów” jednocześnie — niektóre skupiają się na drobnych detalach, inne obejmują szersze sąsiedztwo. Dzięki zastosowaniu splotów z dylatacją, które sięgają dalej bez utraty rozdzielczości, moduł zbiera zarówno lokalne szczegóły, jak i szeroki kontekst. Następnie łączy te perspektywy, aby sieć mogła wiarygodnie uwypuklać maleńkie polipy ukryte między fałdami, jak i większe zmiany chorobowe dominujące w polu widzenia, nawet gdy kamera porusza się szybko.
Jak dobrze działa system
Naukowcy przetestowali AVPDN na dwóch dużych publicznych zbiorach nagrań kolonoskopii, obejmujących dziesiątki tysięcy klatek od wielu pacjentów, z polipami o zróżnicowanych kształtach, rozmiarach i cechach wizualnych. Porównali swoją metodę z powszechnie stosowanymi detektorami obiektów oraz kilkoma wyspecjalizowanymi systemami do wykrywania polipów. We wszystkich kluczowych miarach — jak często polipy są poprawnie wykrywane, jak często unika się fałszywych alarmów oraz jak system równoważy te dwa cele — AVPDN konsekwentnie osiągał najlepsze wyniki. Poprawił główny wskaźnik dokładności o kilka punktów procentowych względem silnych, nowoczesnych baz, a przy tym nadal działał wystarczająco szybko do użycia w czasie rzeczywistym na obecnym sprzęcie graficznym. Skrupulatne testy ablacjne wykazały, że oba nowe moduły w istotny sposób przyczyniają się do tej przewagi.
Co to oznacza dla pacjentów
Mówiąc prosto, praca ta pokazuje, że systemy AI można wytrenować tak, by patrzyły poza rozmycie, odblaski i gwałtowne zmiany wielkości, które utrudniają analizę nagrań kolonoskopii, i by dostrajały się do charakterystycznych wzorców polipów. Poprzez oczyszczanie i ponowne ważenie informacji wizualnej wewnątrz sieci, zamiast polegać na dodatkowych czujnikach lub wolniejszej analizie wideo, AVPDN wykrywa więcej polipów przy mniejszej liczbie przeoczeń i fałszywych alarmów. Jeśli technologia ta zostanie zintegrowana z narzędziami klinicznymi, może służyć jako drugie oko podczas zabiegów, pomagając lekarzom wcześniej i pewniej zauważać subtelne zmiany oraz ostatecznie zmniejszając ryzyko, że niebezpieczny polip pozostanie nierozpoznany.
Cytowanie: Chen, Z., Lu, S. AVPDN: learning motion-robust and scale-adaptive representations for polyp detection in dynamic colonoscopy frames. Sci Rep 16, 11591 (2026). https://doi.org/10.1038/s41598-026-42286-5
Słowa kluczowe: kolonoskopia, wykrywanie polipów, AI w obrazowaniu medycznym, analiza wideo, screening raka jelita grubego