Clear Sky Science · nl
AVPDN: leren van bewegingsbestendige en schaaladaptieve representaties voor poliepdetectie in dynamische colonoscopiebeelden
Waarom het vinden van kleine gezwellen ertoe doet
De meeste colorectale kankers beginnen als kleine gezwellen, polyps genoemd, aan de bekleding van de darm. Tijdens een coloscopie proberen artsen deze polyps op te sporen en te verwijderen voordat ze gevaarlijk worden. Moderne videoscopen leggen alles vast, maar de camera beweegt snel, het beeld is vaak wazig of glanzend, en polyps kunnen klein en moeilijk zichtbaar zijn. Dit artikel introduceert een nieuw computersysteem dat leert door de visuele chaos van echte coloscopievideo’s heen te kijken, waardoor artsen meer polyps nauwkeuriger en in realtime kunnen vinden.
De uitdaging van een bewegende camera
Coloscopie is niet hetzelfde als het maken van een stilstaande foto — het lijkt meer op het filmen van een onstabiele, close-up verkenning in het lichaam. Terwijl de scoop vordert, trilt en roteert de camera, trekt de darmwand samen, en slaan vloeistoffen en luchtbellen voor de lens. Deze bewegingen veroorzaken bewegingsonscherpte, felle witte reflecties en plotselinge veranderingen in de schijnbare grootte van dezelfde structuur van het ene frame naar het andere. Kleine polyps kunnen bijna niet te onderscheiden zijn van omliggende plooien weefsel en verdwijnen soms kort achter bellen of schittering. De meeste bestaande computervisie-systemen zijn oorspronkelijk ontwikkeld voor natuurfoto’s of gewone video’s, waar de camera stabieler is en objecten eenvoudiger van de achtergrond te scheiden zijn, waardoor ze moeite hebben in deze extreme omstandigheden.
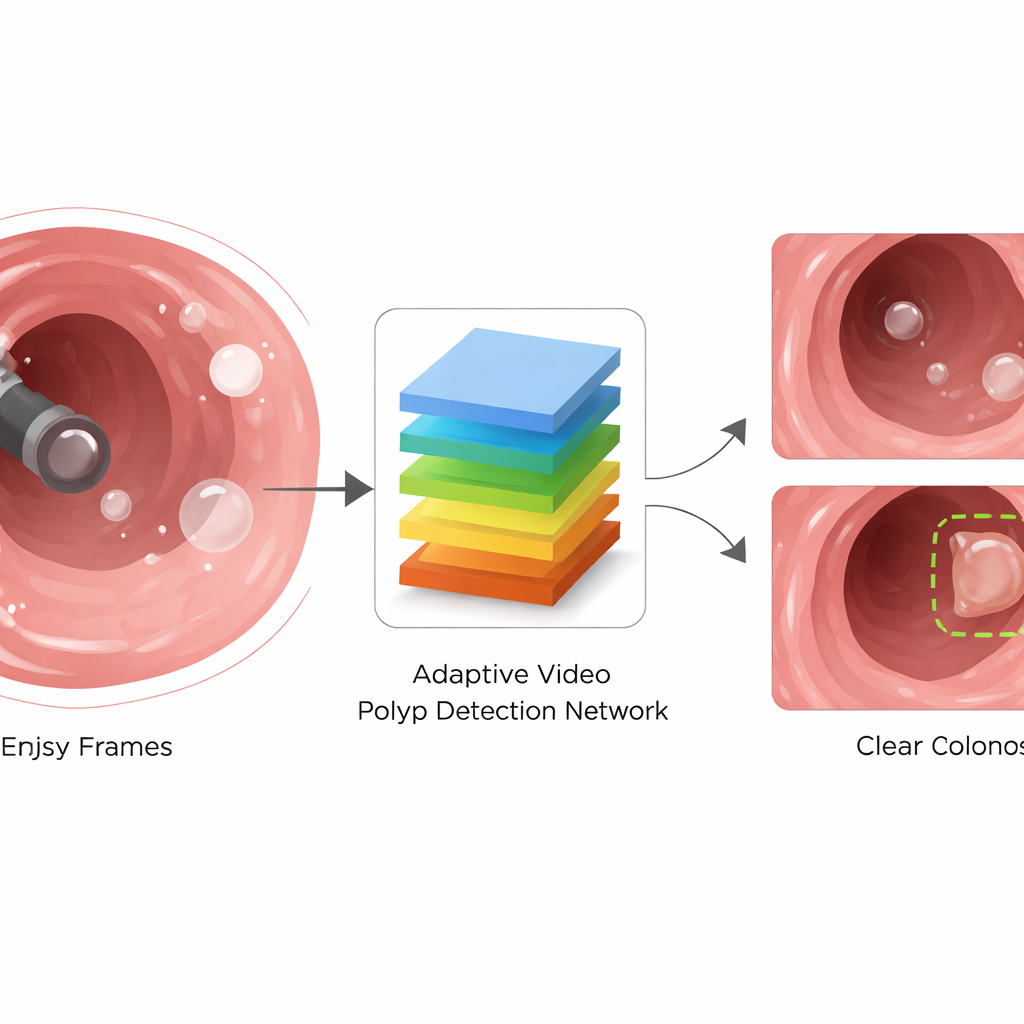
Een slimmer manier om coloscopievideo te lezen
Om met deze problemen om te gaan, stellen de auteurs het Adaptive Video Polyp Detection Network (AVPDN) voor. In de kern behandelt AVPDN elk videoframe als een afbeelding en laat het door een standaard feature-extractor lopen die randen, texturen en kleuren vastlegt. Maar in plaats van daar te stoppen, voegt het een gespecialiseerde "enhancement"-fase toe, specifiek ontworpen voor coloscopie. Deze fase bestaat uit herhaalbare blokken die ruisige signalen opruimen, echt poliepachtige patronen versterken en polyps van verschillende groottes bijhouden. Belangrijk is dat de methode frame voor frame werkt zonder lange videoreeksen in de tijd te hoeven analyseren, waardoor het systeem snel genoeg blijft voor realtime gebruik.
Ruis filteren en toch belangrijke aanwijzingen bewaren
De eerste belangrijke bouwsteen heet Adaptive Feature Interaction and Augmentation. Simpel gezegd bekijkt deze blok de beeldfeatures op twee verschillende manieren tegelijk. De ene tak beschouwt brede verbindingen over het hele beeld, wat helpt het algemene tafereel te begrijpen en geen verre aanwijzingen van een poliep te missen. De andere tak is selectiever: die speelt onderdelen van het beeld die zwakke of inconsistente patronen tonen, zoals onscherpte en schittering, sterk naar de achtergrond. Het systeem leert vervolgens hoeveel vertrouwen het in elke tak moet stellen voor elk frame en mengt ze adaptief. Een slimme "channel shuffle"-stap mengt informatie tussen verschillende groepen features, waardoor het netwerk rijkere combinaties van textuur en vorm ontdekt die echte polyps onderscheiden van onschadelijke plooien en vlekken.
Polyps zien op vele schalen
De tweede belangrijke blok heet Scale-Aware Context Integration. Polyps kunnen heel klein zijn wanneer de camera ver weg is en veel groter wanneer de scoop dichterbij komt, dus het systeem moet over een breed bereik van schalen werken. Deze module bekijkt de scène door meerdere "virtuele lenzen" tegelijk — sommige richten zich op fijne details terwijl andere een wijder buurtgebied vastleggen. Door gebruik te maken van gedilateerde filters die verder reiken zonder resolutie te verliezen, verzamelt de module zowel lokale details als brede context. Het combineert deze gezichtspunten zodat het netwerk betrouwbaar kleine polyps die tussen plooien verscholen liggen kan benadrukken, evenals grotere laesies die het gezichtsveld domineren, zelfs wanneer de camera snel beweegt.
Hoe goed het systeem presteert
De onderzoekers testten AVPDN op twee grote publieke verzamelingen van coloscopievideo’s met tienduizenden frames van vele patiënten, met polyps in uiteenlopende vormen, maten en verschijningsvormen. Ze vergeleken hun methode met veelgebruikte objectdetectors en verschillende gespecialiseerde poliepsystemen. Over alle belangrijke maatstaven — hoe vaak polyps correct worden gevonden, hoe vaak valse alarmen worden vermeden, en hoe goed het systeem deze twee doelen in balans houdt — kwam AVPDN consequent als beste uit de bus. Het verbeterde de belangrijkste accuratescore met enkele procentpunten ten opzichte van sterke moderne baselines, terwijl het nog steeds snel genoeg draaide voor realtime gebruik op huidige grafische hardware. Zorgvuldig uitgevoerde interne tests toonden aan dat elk van de twee nieuwe modules merkbaar aan dit voordeel bijdroeg.
Wat dit betekent voor patiënten
In eenvoudige bewoordingen toont dit werk aan dat een AI-systeem kan worden getraind om voorbij de onscherpte, schittering en snelle grootteveranderingen te kijken die coloscopievideo zo moeilijk maken, en zich te richten op de kenmerkende patronen van polyps. Door visuele informatie binnen het netwerk te reinigen en opnieuw te wegen in plaats van te vertrouwen op extra sensoren of tragere videoanalyse, detecteert AVPDN meer polyps met minder misses en minder valse alarmen. Als dit in klinische instrumenten wordt geïntegreerd, kan dergelijke technologie fungeren als een tweede paar ogen tijdens procedures, artsen helpen subtiele gezwellen eerder en betrouwbaarder op te merken en uiteindelijk het risico verkleinen dat een gevaarlijke poliep wordt achtergelaten.
Bronvermelding: Chen, Z., Lu, S. AVPDN: learning motion-robust and scale-adaptive representations for polyp detection in dynamic colonoscopy frames. Sci Rep 16, 11591 (2026). https://doi.org/10.1038/s41598-026-42286-5
Trefwoorden: coloscopie, polieponderkenning, medische beeldvorming AI, videoanalyse, darmkankerscreening