Clear Sky Science · pl
Mieszanie instancji Cut: metoda augmentacji danych specyficzna dla domeny stosowana do wykrywania zmian w przewodzie pokarmowym
Dlaczego lepsze dane treningowe mają znaczenie dla zdrowia jelit
Lekarze używają małych kamer, by zajrzeć do wnętrza przewodu pokarmowego i wykryć wczesne oznaki choroby, takie jak niewielkie nieprawidłowe obszary, które z czasem mogą przekształcić się w raka. Te sygnały bywają jednak bardzo subtelne, a komputery, które miałyby pomagać lekarzom je odnajdywać, potrzebują tysięcy dobrze oznakowanych obrazów, by nauczyć się, czego szukać. W artykule opisano nowy sposób „powiększania” realistycznych obrazów treningowych na komputerze, ułatwiający nauczanie systemów sztucznej inteligencji wykrywania tych trudnych do zauważenia zmian we wczesnym stadium.
Problem ukrytych miejsc ostrzegawczych
Zmiany w żołądku i jelitach — takie jak metaplazja jelitowa, wczesna dysplazja czy małe polipy — są ważnymi wczesnymi sygnałami raka, a mimo to często różnią się od zdrowej tkanki tylko nieznacznie. Eksperci ludzie czasem je przeoczają, a modele komputerowe również mają z nimi problemy, głównie dlatego, że brakuje wystarczającej liczby wysokiej jakości, starannie oznakowanych obrazów do nauki. Gromadzenie i anotowanie obrazów endoskopowych jest kosztowne, czasochłonne i etycznie wrażliwe, zwłaszcza w przypadku rzadkich typów zmian. Tradycyjne sztuczki zwiększające dane treningowe — takie jak obracanie, odbicia lustrzane czy mieszanie całych obrazów — sprawdzają się w zwykłej fotografii, lecz zwykle rozmywają lub przesuwają bardzo drobne detale i granice, które mają największe znaczenie w badaniach endoskopowych.
Od grubych wycinek i wklejek do mieszania z uwzględnieniem anatomii
Naukowcy próbowali bardziej zaawansowanych metod „wycinania i wklejania”, które kopiują widoczne zmiany z jednego obrazu i wstawiają je w inny, albo wykorzystują modele generatywne do tworzenia zupełnie nowych obrazów. Chociaż te strategie zwiększają różnorodność, często ignorują otaczającą anatomię. Wklejona zmiana może znaleźć się w nierealistycznym miejscu lub nie pasować kolorem i teksturą do pobliskiej tkanki, co obniża wiarygodność obrazów treningowych. Modele generatywne, takie jak GAN-y czy sieci dyfuzyjne, potrafią wygenerować imponujące obrazy, lecz wymagają bardzo dużych zbiorów danych, są trudne w kontroli i mogą tworzyć fikcyjne struktury nieistniejące u prawdziwych pacjentów. W zadaniach zależnych od subtelnych przesunięć koloru i drobnych wzorców powierzchni — jak w wczesnych chorobach żołądka i jelita grubego — te ograniczenia zmniejszają użyteczność obecnych metod augmentacji.
Nowy sposób wtapiania zmian w realistyczne sceny
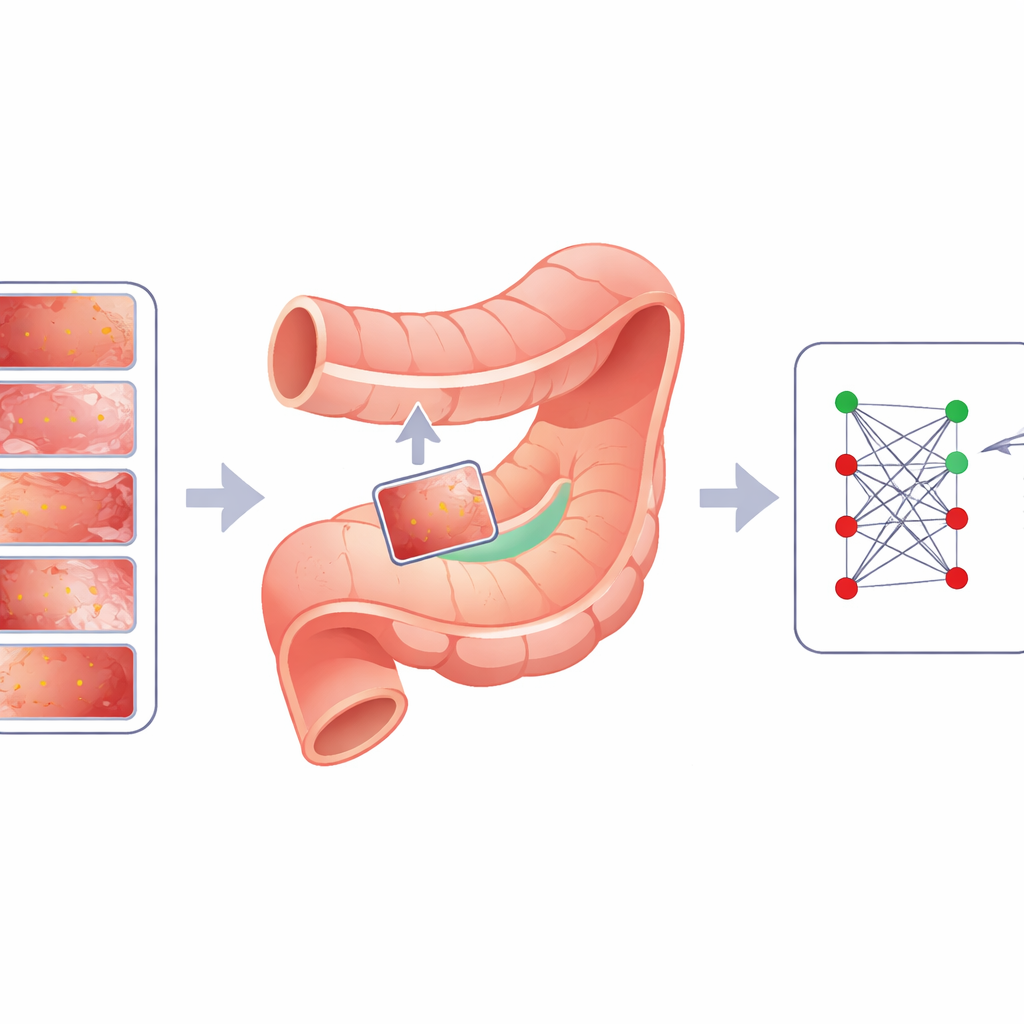
Autorzy proponują Cut Instance Mixing (CIM), podejście specyficzne dla domeny, zaprojektowane specjalnie do obrazów gastroenterologicznych. Zamiast umieszczać zmiany losowo, CIM najpierw analizuje obraz zdrowy, aby znaleźć znaczące obszary przypominające naturalne wzory błony śluzowej. Robi to poprzez grupowanie pikseli w gładkie, biologicznie prawdopodobne płaty, a następnie dzielenie ich na mniejsze, uporządkowane podobszary. Następnie CIM wybiera rzeczywistą zmianę z innego obrazu i wyszukuje podobszar, którego kolor i tekstura najlepiej pasują do otoczenia zmiany. Zmiana jest umieszczana tam i płynnie wtapiana za pomocą technik zachowujących krawędzie i oświetlenie, z regulacją (oznaczaną α) kontrolującą, jak wyraźna lub subtelna ma być zmiana. Efektem jest syntetyczny obraz, w którym zmiana wygląda, jakby naturalnie powstała w tym miejscu, a ponieważ etykieta oryginalnej zmiany jest znana, nowy obraz jest automatycznie oznakowany do treningu.
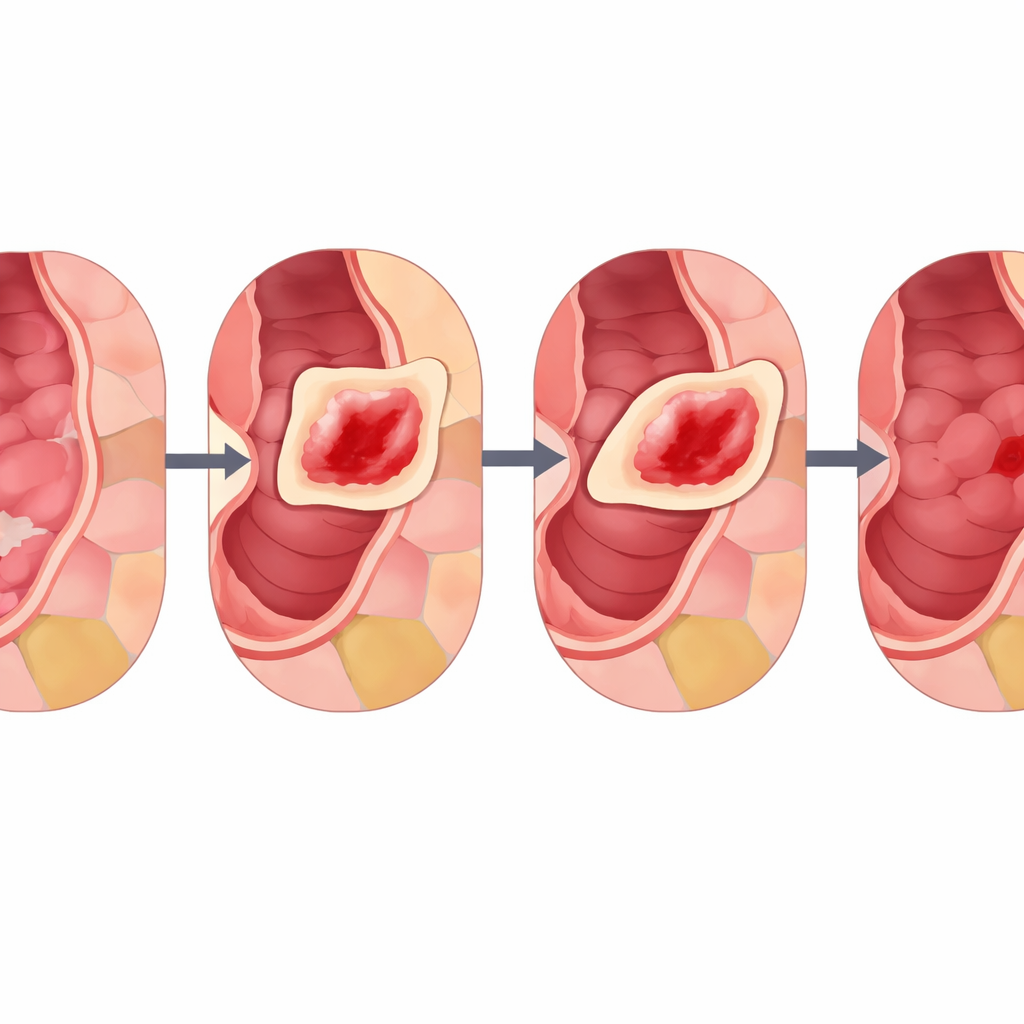
Testowanie metody
Aby sprawdzić, czy CIM rzeczywiście pomaga, zespół wytrenował ten sam model uczenia głębokiego na trzech różnych zbiorach endoskopowych: metaplazja jelitowa, dysplazja i polipy jelita grubego. Dla każdego zbioru porównano CIM ze standardowymi technikami, takimi jak MixUp, CutMix oraz prostym losowym kopiuj–wklej, stosując rygorystyczną walidację krzyżową i zewnętrzny zestaw testowy z innych szpitali w przypadku polipów. We wszystkich niemal miarach wydajności — takich jak ogólna dokładność, zdolność rozróżniania tkanki chorej od zdrowej i stabilność w kolejnych testach — CIM, szczególnie przy silniejszym wtapianiu (α około 0,8), wypadał najlepiej. Badacze przeanalizowali także mapy cieplne pokazujące, gdzie model „patrzy”, podejmując decyzje. Modele trenowane z użyciem CIM koncentrowały się precyzyjniej na prawdziwych obszarach zmian, lepiej zgadzając się z anotacjami medycznymi niż rywale, co sugeruje, że CIM pomaga sieci nauczyć się cech bardziej istotnych klinicznie zamiast skrótów czy szumów.
Co to oznacza dla przyszłych badań przesiewowych raka jelit
Mówiąc prościej, CIM daje komputerom lekarzy więcej i lepszych obrazów ćwiczebnych, wstawiając prawdziwe zmiany w wiarygodne nowe lokalizacje w sposób respektujący anatomię. Podejście to zmniejsza nierównowagę między powszechnymi a rzadkimi stanami, wzmacnia wykrywanie wczesnych i subtelnych chorób oraz działa bez użycia ciężkich, trudnych do kontrolowania modeli generatywnych czy dodatkowych sieci pomocniczych. Choć obecne badanie skupia się na decyzjach binarnych — zmiana lub brak zmiany — ta sama strategia mogłaby zostać rozszerzona na wiele typów zmian i przetestowana na innych układach narządów. Jeśli zostanie szeroko przyjęta, CIM i podobne narzędzia mieszania danych uwzględniające anatomię mogłyby uczynić wspomaganą komputerowo endoskopię bardziej niezawodną, pomagając specjalistom wcześniej i bardziej konsekwentnie wykrywać niebezpieczne zmiany w przewodzie pokarmowym.
Cytowanie: Neto, A., Almeida, E., Libânio, D. et al. Cut instance mixing: A domain-specific data augmentation method applied to gastrointestinal lesion detection. Sci Rep 16, 11941 (2026). https://doi.org/10.1038/s41598-026-42138-2
Słowa kluczowe: zmiany w przewodzie pokarmowym, obrazowanie endoskopowe, augmentacja danych, uczenie głębokie, badania przesiewowe w kierunku raka