Clear Sky Science · fr
Cut instance mixing : une méthode d’augmentation de données spécifique au domaine appliquée à la détection des lésions gastro-intestinales
Pourquoi des données d’entraînement plus intelligentes comptent pour la santé intestinale
Les médecins utilisent de petites caméras pour observer l’intérieur de notre tube digestif et repérer les signes précoces de maladie, comme de petites zones anormales qui peuvent un jour évoluer en cancer. Mais ces signaux d’alerte peuvent être extrêmement subtils, et les ordinateurs susceptibles d’aider les cliniciens à les détecter ont besoin de milliers d’images bien étiquetées pour apprendre à reconnaître ce qu’il faut chercher. Cet article présente une nouvelle façon de « faire pousser » des images d’entraînement réalistes par informatique, facilitant l’apprentissage des systèmes d’intelligence artificielle pour détecter ces lésions difficiles à voir précocement.
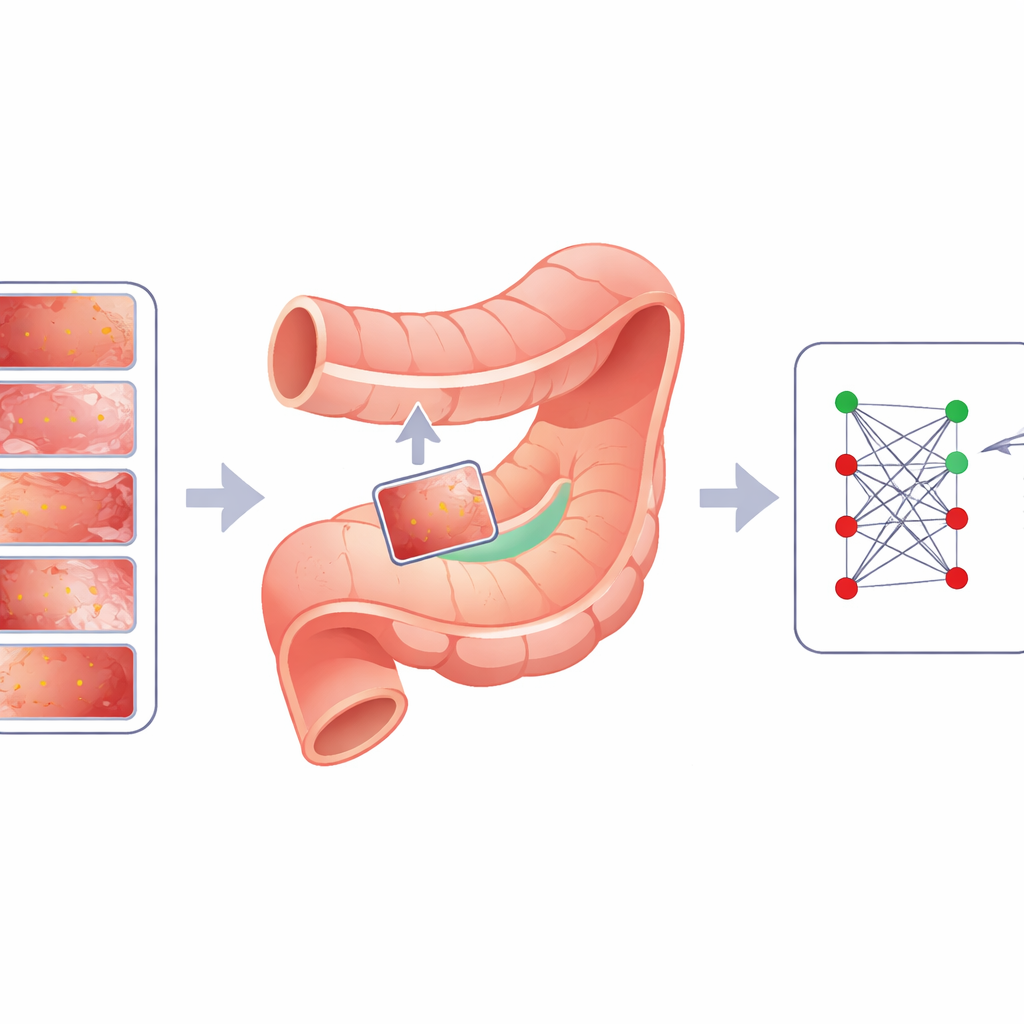
Le défi des zones d’alerte dissimulées
Les lésions de l’estomac et des intestins — comme la métaplasie intestinale, la dysplasie précoce et les petits polypes — sont des signes d’alerte précoces importants pour le cancer, mais elles ressemblent souvent très peu au tissu sain. Les experts humains les manquent parfois, et les modèles informatiques peinent également, principalement parce qu’il n’existe pas suffisamment d’images de haute qualité, soigneusement annotées, pour s’entraîner. Collecter et annoter des images endoscopiques est coûteux, chronophage et soulève des enjeux éthiques, surtout pour les types de lésions rares. Les astuces traditionnelles pour augmenter les données — comme le retournement, la rotation ou le mélange d’images entières — aident en photographie courante, mais ont tendance à estomper ou à déplacer les détails et les contours très fins qui sont essentiels dans les examens gastro-intestinaux.
Du découpage-coller grossier à un mélange conscient de l’anatomie
Des chercheurs ont tenté des méthodes « découper-coller » plus avancées qui copient des lésions visibles d’une image pour les placer dans une autre, ou utilisent des modèles génératifs pour créer des images entièrement nouvelles. Si ces stratégies augmentent la variété, elles négligent souvent l’anatomie environnante. Une lésion collée peut atterrir à un endroit irréaliste ou contraster en couleur et texture avec les tissus voisins, rendant les images d’entraînement moins crédibles. Les modèles génératifs comme les GAN ou les réseaux de diffusion peuvent produire des images impressionnantes, mais ils exigent des jeux de données très volumineux, sont difficiles à contrôler et risquent d’inventer des structures qui n’existent pas chez de vrais patients. Pour des tâches qui dépendent de légers changements de couleur et de motifs de surface très fins — comme dans les maladies précoces de l’estomac et du côlon — ces limites restreignent l’utilité des méthodes d’augmentation actuelles.
Une nouvelle façon d’introduire des lésions dans des scènes réalistes
Les auteurs présentent Cut Instance Mixing (CIM), une approche spécifique au domaine conçue spécialement pour les images gastro-intestinales. Plutôt que de placer des lésions au hasard, CIM analyse d’abord une image saine pour trouver des régions significatives qui ressemblent à de véritables motifs muqueux. Elle procède en regroupant les pixels en patchs lisses et biologiquement plausibles, puis en les divisant en sous-régions plus petites et ordonnées. Ensuite, CIM sélectionne une lésion réelle provenant d’une autre image et cherche la sous-région dont la couleur et la texture correspondent le mieux à l’environnement de la lésion. La lésion est alors positionnée là et fusionnée de manière homogène à l’aide de techniques qui préservent les contours et l’éclairage, avec un réglage (appelé α) qui contrôle l’intensité d’apparition de la lésion, forte ou subtile. Le résultat est une image synthétique où la lésion semble s’être formée naturellement à cet endroit, et comme l’étiquette de la lésion d’origine est connue, la nouvelle image est automatiquement annotée pour l’apprentissage.
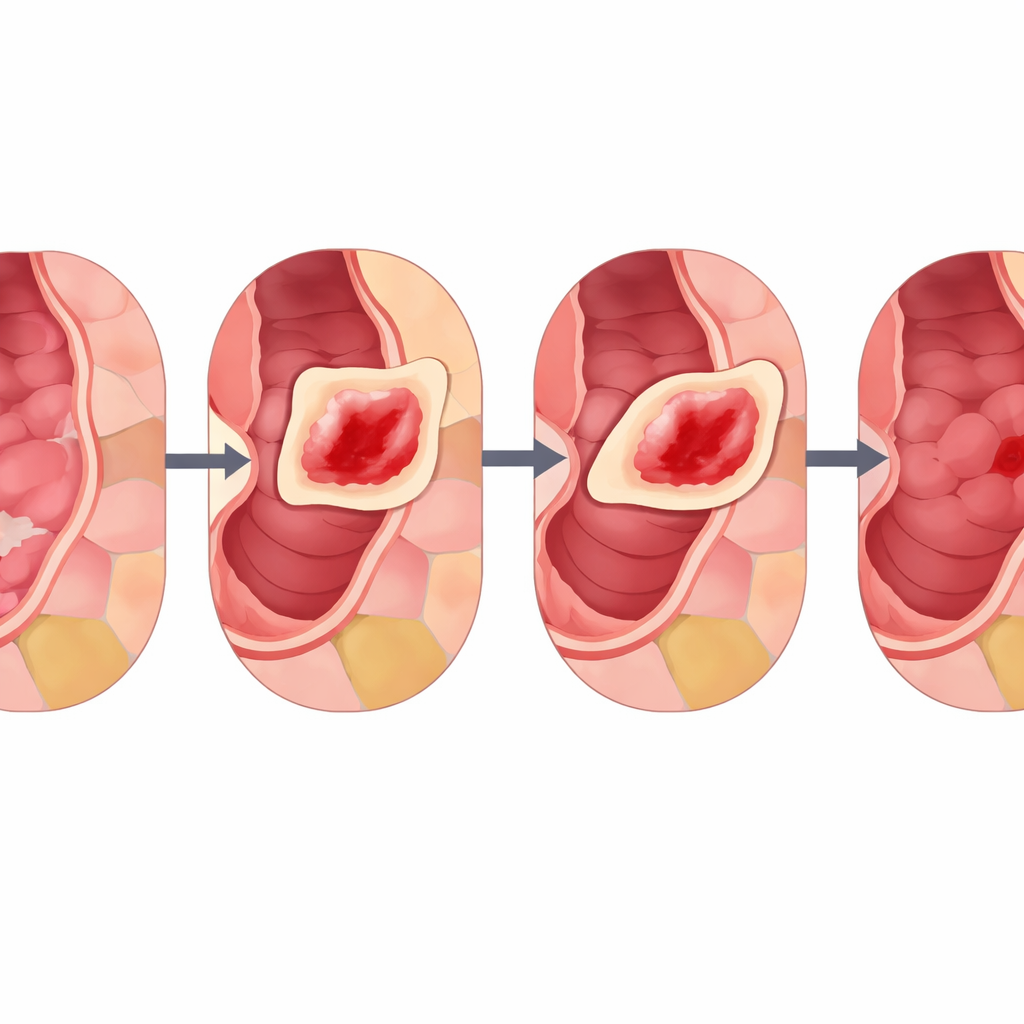
Mettre la méthode à l’épreuve
Pour vérifier si CIM aide réellement, l’équipe a entraîné le même modèle d’apprentissage profond sur trois collections endoscopiques différentes : métaplasie intestinale, dysplasie et polypes du côlon. Pour chaque jeu de données, ils ont comparé CIM à des techniques classiques comme MixUp, CutMix et un simple copier–coller aléatoire, en utilisant une validation croisée stricte et un jeu de test externe provenant d’autres hôpitaux pour le cas des polypes. Sur presque toutes les mesures de performance — telles que la précision globale, la capacité à séparer tissu malade et sain, et la stabilité sur des tests répétés — CIM, en particulier avec un mélange plus prononcé (α autour de 0,8), s’est avéré supérieur. Les chercheurs ont aussi examiné des cartes de chaleur montrant où le modèle « porte son attention » lors de ses décisions. Les modèles entraînés avec CIM se sont focalisés plus précisément sur les régions réellement lésées, correspondant mieux aux annotations médicales que les méthodes concurrentes, ce qui suggère que CIM aide le réseau à apprendre des caractéristiques plus cliniquement pertinentes plutôt que des raccourcis ou du bruit.
Ce que cela signifie pour le dépistage futur du cancer digestif
En termes simples, CIM offre aux ordinateurs des cliniciens davantage d’images d’entraînement de meilleure qualité en insérant de vraies lésions dans de nouveaux emplacements crédibles, d’une manière qui respecte l’anatomie. Cette approche réduit le déséquilibre entre conditions fréquentes et rares, renforce la détection des maladies précoces et subtiles, et fonctionne sans modèles génératifs lourds et difficiles à contrôler ni réseaux auxiliaires supplémentaires. Alors que le travail actuel se concentre sur des décisions binaires — lésion ou pas de lésion — la même stratégie pourrait être étendue à plusieurs types de lésions et testée sur d’autres systèmes d’organes. Si elle est largement adoptée, CIM et des outils similaires de « mélange » sensibles à l’anatomie pourraient rendre l’endoscopie assistée par ordinateur plus fiable, aidant les spécialistes à repérer plus tôt et plus régulièrement les modifications dangereuses du tube digestif.
Citation: Neto, A., Almeida, E., Libânio, D. et al. Cut instance mixing: A domain-specific data augmentation method applied to gastrointestinal lesion detection. Sci Rep 16, 11941 (2026). https://doi.org/10.1038/s41598-026-42138-2
Mots-clés: lésions gastro-intestinales, imagerie endoscopique, augmentation de données, apprentissage profond, dépistage du cancer