Clear Sky Science · it
Cut instance mixing: un metodo di data augmentation specifico per il dominio applicato alla rilevazione delle lesioni gastrointestinali
Perché dati di addestramento più intelligenti contano per la salute intestinale
I medici usano piccole videocamere per osservare l’interno del nostro tratto digestivo e individuare i primi segnali di malattia, come piccole aree anomale che un giorno potrebbero trasformarsi in tumore. Ma questi segnali possono essere estremamente sfumati, e i computer che potrebbero aiutare i medici a trovarli necessitano di migliaia di immagini ben etichettate per imparare cosa cercare. Questo articolo presenta un nuovo modo per “far crescere” immagini di addestramento realistici al computer, rendendo più semplice insegnare ai sistemi di intelligenza artificiale a rilevare precocemente queste lesioni difficili da vedere.
La sfida delle macchie di avvertimento nascoste
Le lesioni nello stomaco e nell’intestino — come la metaplasia intestinale, la displasia precoce e i piccoli polipi — sono importanti segnali precoci per il cancro, eppure spesso appaiono solo leggermente differenti dal tessuto sano. Anche gli esperti umani a volte le mancano, e i modelli computazionali fanno fatica, principalmente perché non esistono abbastanza immagini di alta qualità e accuratamente annotate da cui apprendere. Raccogliere e annotare immagini endoscopiche è costoso, richiede tempo e solleva questioni etiche, soprattutto per i tipi di lesione rari. I trucchi tradizionali per aumentare i dati di addestramento — come ribaltare, ruotare o fondere intere immagini — funzionano nella fotografia quotidiana, ma tendono a sfumare o spostare i dettagli e i confini molto fini che contano di più negli esami gastrointestinali.
Dal banale ritaglia-e-incolla a un mixing consapevole dell’anatomia
I ricercatori hanno provato metodi più avanzati di “ritaglia-e-incolla” che copiano lesioni visibili da un’immagine e le inseriscono in un’altra, o impiegano modelli generativi per creare immagini completamente nuove. Pur aumentando la varietà, queste strategie spesso ignorano l’anatomia circostante. Una lesione incollata può finire in una posizione irrealistica o entrare in conflitto per colore e texture con il tessuto vicino, rendendo le immagini di addestramento meno credibili. Modelli generativi come GAN e reti di diffusione possono produrre immagini impressionanti, ma richiedono dataset molto grandi, sono difficili da controllare e rischiano di inventare strutture che non esistono nei pazienti reali. Per compiti che dipendono da sottili variazioni di colore e fini pattern superficiali — come nelle malattie precoci di stomaco e colon — questi limiti riducono l’aiuto che i metodi di augmentation attuali possono offrire.
Un nuovo modo di mescolare lesioni in scene realistiche
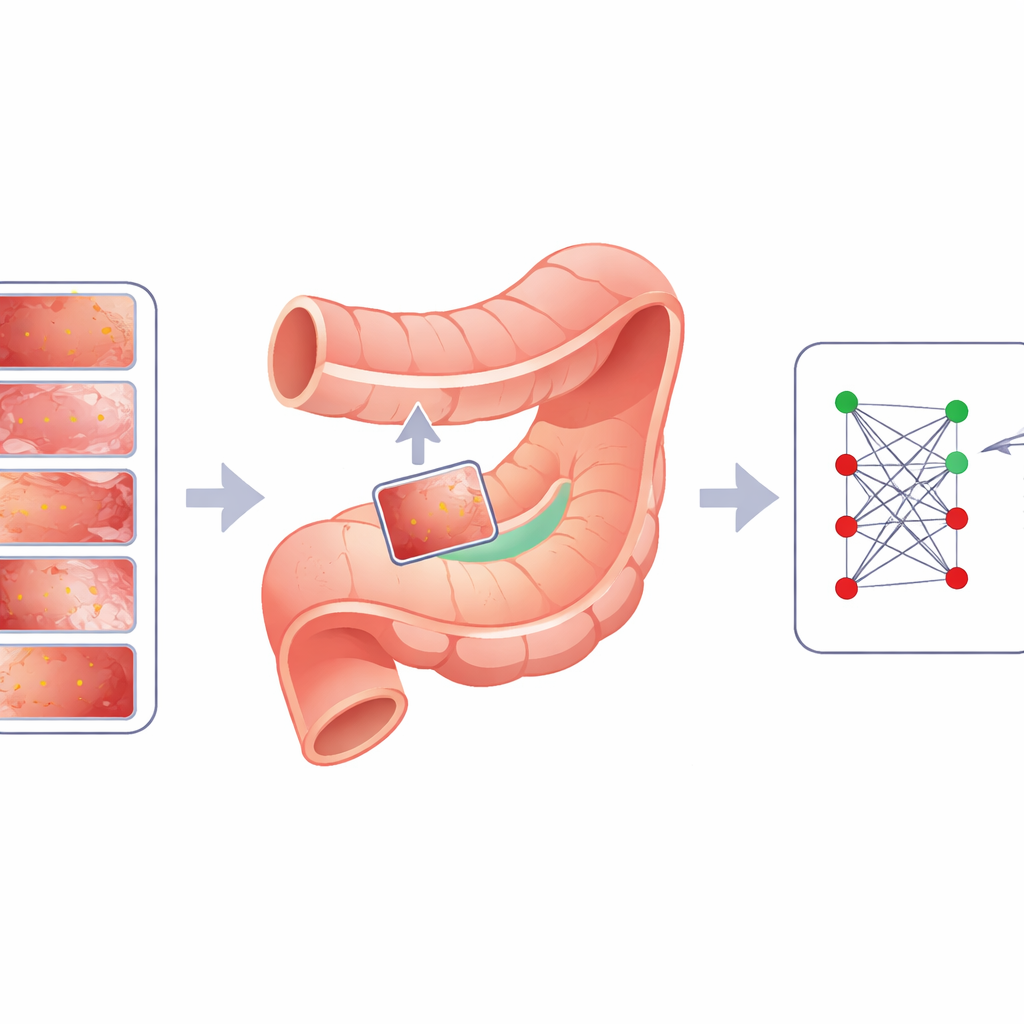
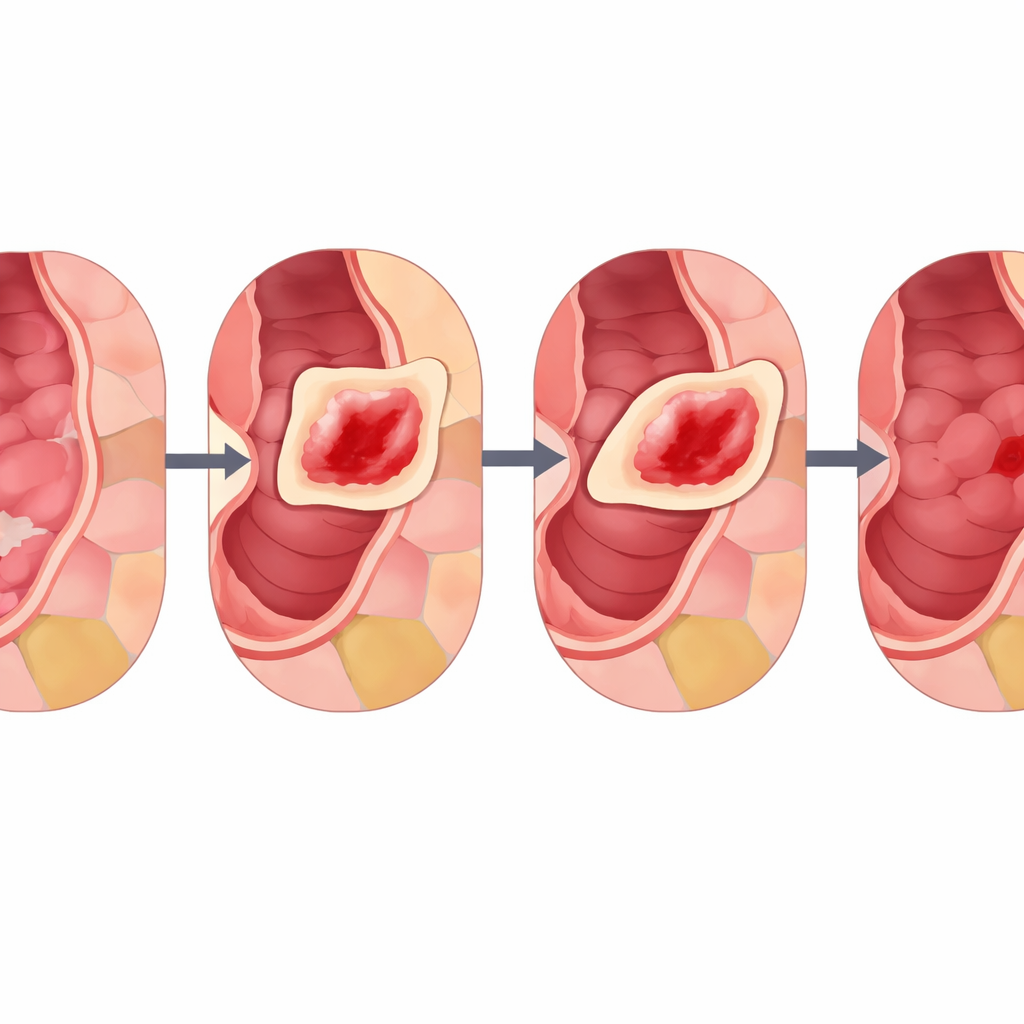
Gli autori introducono Cut Instance Mixing (CIM), un approccio specifico per il dominio progettato appositamente per le immagini gastrointestinali. Invece di posizionare le lesioni in modo casuale, CIM analizza prima un’immagine sana per trovare regioni significative che assomiglino a veri pattern mucosali. Lo fa raggruppando i pixel in patch lisce e biologicamente plausibili e poi suddividendole in sotto-regioni più piccole e ordinate. Successivamente, CIM seleziona una lesione reale da un’altra immagine e cerca la sotto-regione il cui colore e texture corrispondono maggiormente all’intorno della lesione. La lesione viene quindi posizionata lì e sfumata in modo uniforme usando tecniche che preservano i bordi e l’illuminazione, con una manopola di regolazione (chiamata α) che controlla quanto la lesione appare marcata o sottile. Il risultato è un’immagine sintetica in cui la lesione sembra essersi formata naturalmente in quel punto e, poiché l’etichetta della lesione originale è nota, la nuova immagine è automaticamente annotata per l’addestramento.
Mettere il metodo alla prova
Per verificare se CIM è veramente utile, il gruppo ha addestrato lo stesso modello di deep learning su tre collezioni endoscopiche diverse: metaplasia intestinale, displasia e polipi del colon. Per ogni dataset hanno confrontato CIM con tecniche standard come MixUp, CutMix e il semplice copy–paste casuale, usando una validazione incrociata rigorosa e un set di test esterno proveniente da altri ospedali per il caso dei polipi. Su quasi tutte le misure di prestazione — come l’accuratezza complessiva, la capacità di separare tessuto malato da quello sano e la stabilità nei test ripetuti — CIM, specialmente con una sfumatura più marcata (α intorno a 0,8), è risultato superiore. I ricercatori hanno anche esaminato mappe di calore che mostrano dove il modello “guarda” quando prende decisioni. I modelli addestrati con CIM si sono concentrati con maggiore precisione sulle regioni di lesione reali, allineandosi meglio con le annotazioni mediche rispetto ai metodi concorrenti e suggerendo che CIM aiuta la rete a imparare caratteristiche più clinicamente significative anziché scorciatoie o rumore.
Cosa significa per il futuro dello screening del cancro gastrointestinale
In termini semplici, CIM fornisce ai computer dei medici più e migliori immagini di pratica, inserendo lesioni reali in nuove posizioni credibili in modo rispettoso dell’anatomia. Questo approccio riduce lo squilibrio tra condizioni comuni e rare, rafforza la rilevazione delle malattie precoci e sottili e funziona senza modelli generativi pesanti e difficili da controllare o reti ausiliarie aggiuntive. Sebbene il lavoro attuale si concentri su decisioni binarie — lesione o nessuna lesione — la stessa strategia potrebbe essere estesa a più tipi di lesione e testata su altri sistemi d’organo. Se ampiamente adottati, CIM e strumenti simili di “mixing” anatomico-aware potrebbero rendere l’endoscopia assistita da computer più affidabile, aiutando gli specialisti a trovare cambiamenti pericolosi nel tratto digestivo in modo più precoce e coerente.
Citazione: Neto, A., Almeida, E., Libânio, D. et al. Cut instance mixing: A domain-specific data augmentation method applied to gastrointestinal lesion detection. Sci Rep 16, 11941 (2026). https://doi.org/10.1038/s41598-026-42138-2
Parole chiave: lesioni gastrointestinali, imaging endoscopico, data augmentation, deep learning, screening del cancro