Clear Sky Science · es
Mezcla de instancias recortadas: un método de aumento de datos específico del dominio aplicado a la detección de lesiones gastrointestinales
Por qué importa tener datos de entrenamiento más inteligentes para la salud intestinal
Los médicos usan cámaras diminutas para inspeccionar nuestro tracto digestivo y detectar señales tempranas de enfermedad, como pequeñas áreas anormales que algún día podrían convertirse en cáncer. Pero estas señales suelen ser muy sutiles, y los ordenadores que podrían ayudar a los médicos a encontrarlas necesitan miles de imágenes bien etiquetadas para aprender qué buscar. Este artículo presenta una nueva forma de “hacer crecer” imágenes de entrenamiento realistas en un ordenador, lo que facilita enseñar a los sistemas de inteligencia artificial a detectar estas lesiones difíciles de ver de forma temprana.
El reto de las manchas de advertencia ocultas
Las lesiones en el estómago y los intestinos —como la metaplasia intestinal, la displasia temprana y los pólipos pequeños— son señales tempranas importantes de cáncer, pero con frecuencia se ven solo ligeramente distintas del tejido sano. Los expertos humanos a veces las pasan por alto, y los modelos informáticos también tienen dificultades, principalmente porque no hay suficientes imágenes de alta calidad y bien anotadas para aprender. Recopilar y anotar imágenes endoscópicas es caro, lento y plantea cuestiones éticas, especialmente para tipos de lesiones raras. Los trucos tradicionales para aumentar los datos de entrenamiento —como volteos, rotaciones o mezclas de imágenes completas— ayudan en la fotografía cotidiana, pero tienden a difuminar o desplazar los detalles y los bordes finos que más importan en los exámenes gastrointestinales.
Del recorte y pegado burdo a la mezcla consciente de la anatomía
Los investigadores han probado métodos de “recortar y pegar” más avanzados que copian lesiones visibles de una imagen y las insertan en otra, o usan modelos generativos para crear imágenes totalmente nuevas. Si bien estas estrategias aumentan la variedad, con frecuencia ignoran la anatomía circundante. Una lesión pegada puede quedar en un lugar poco realista o chocar en color y textura con el tejido cercano, haciendo que las imágenes de entrenamiento sean menos verosímiles. Los modelos generativos como las GAN y las redes de difusión pueden producir imágenes impresionantes, pero exigen conjuntos de datos muy grandes, son difíciles de controlar y corren el riesgo de inventar estructuras que no existen en pacientes reales. Para tareas que dependen de sutiles cambios de color y patrones superficiales finos —como en las enfermedades tempranas del estómago y el colon— estas limitaciones reducen lo que los métodos de aumento actuales pueden aportar.
Una nueva forma de integrar lesiones en escenas realistas
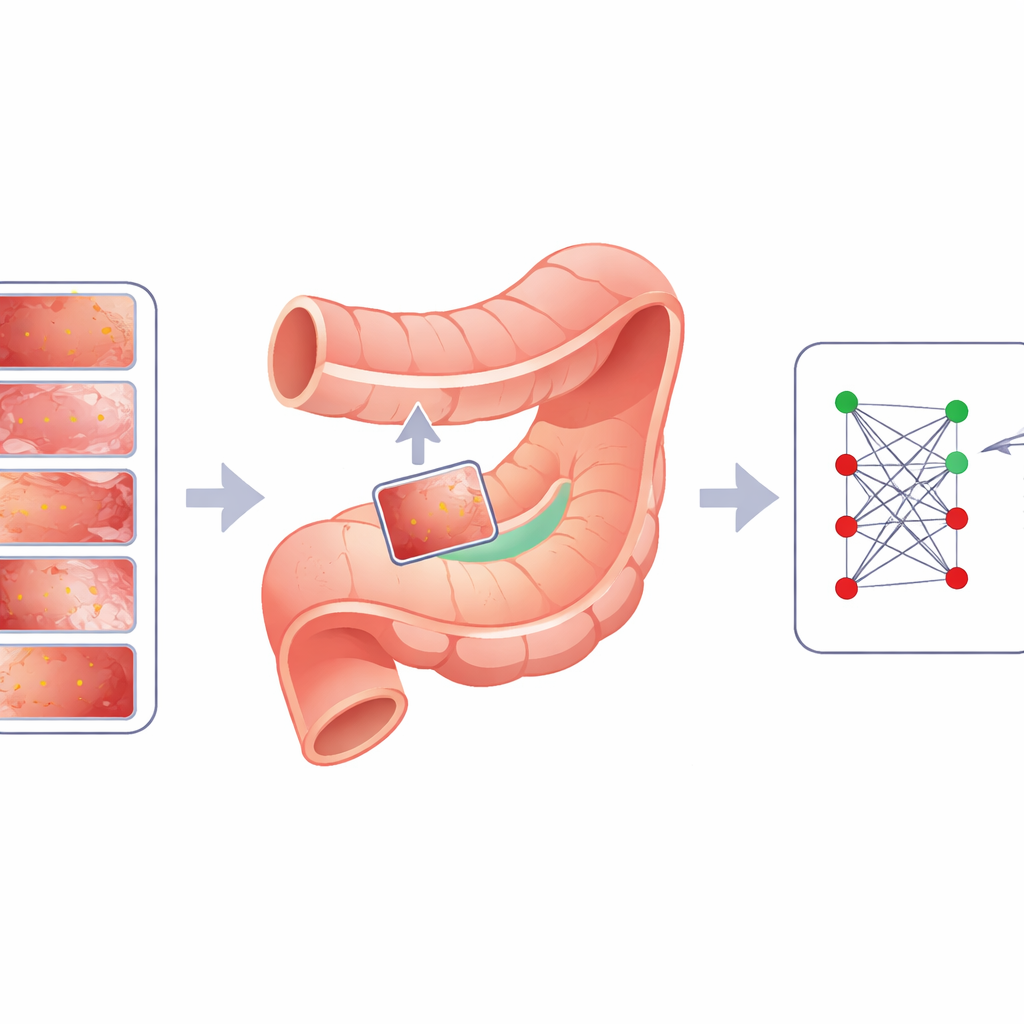
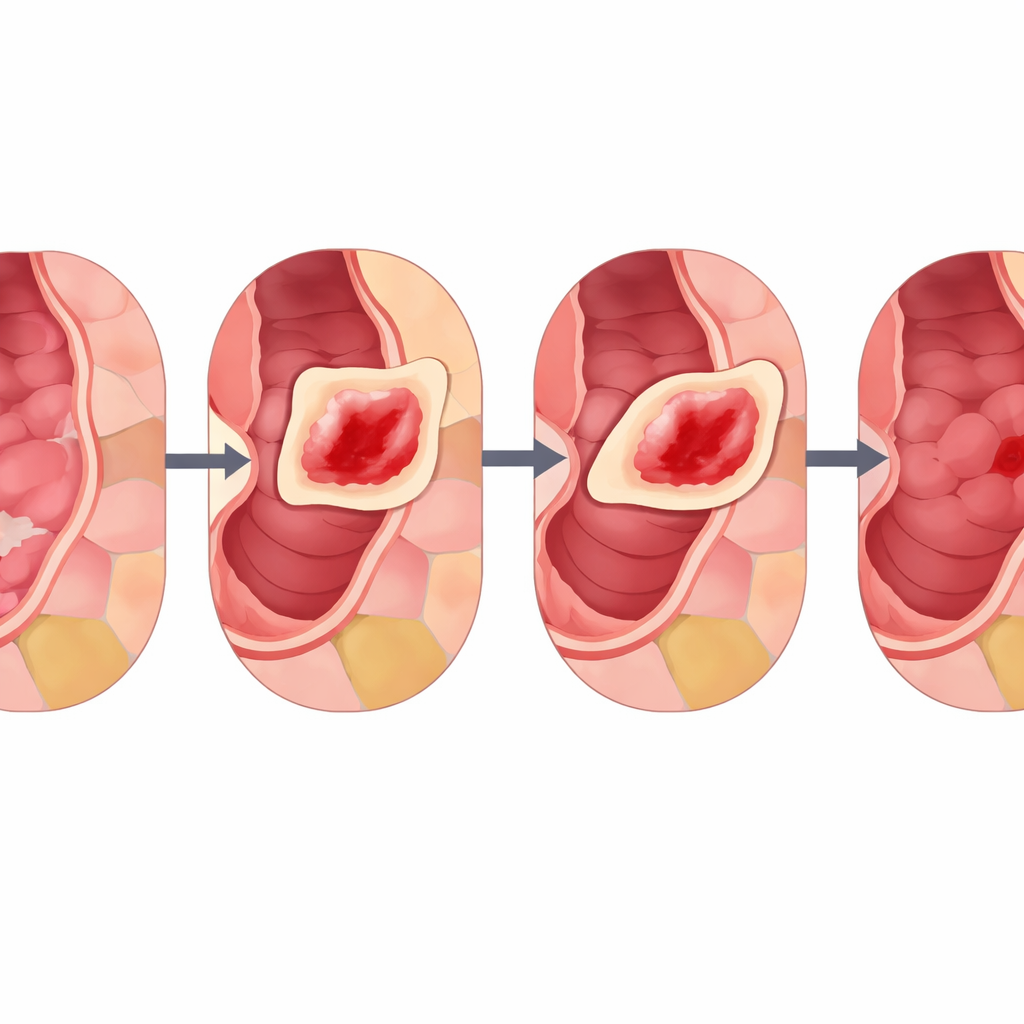
Los autores presentan Cut Instance Mixing (CIM), un enfoque específico del dominio diseñado concretamente para imágenes gastrointestinales. En lugar de colocar lesiones al azar, CIM analiza primero una imagen sana para encontrar regiones significativas que se parezcan a los patrones mucosos reales. Hace esto agrupando píxeles en parches suaves y biológicamente plausibles y luego dividiéndolos en subregiones más pequeñas y ordenadas. A continuación, CIM selecciona una lesión real de otra imagen y busca la subregión cuyo color y textura coincidan más con el entorno de la lesión. La lesión se posiciona allí y se mezcla de forma suave usando técnicas que preservan los bordes y la iluminación, con un control (denominado α) que regula cuán fuerte o sutil aparece la lesión. El resultado es una imagen sintética donde la lesión parece haberse formado naturalmente en ese lugar, y dado que la etiqueta de la lesión original se conoce, la nueva imagen queda automáticamente anotada para entrenamiento.
Poniendo el método a prueba
Para comprobar si CIM realmente ayuda, el equipo entrenó el mismo modelo de aprendizaje profundo en tres colecciones endoscópicas diferentes: metaplasia intestinal, displasia y pólipos de colon. Para cada conjunto de datos, compararon CIM con técnicas estándar como MixUp, CutMix y el simple copiado y pegado aleatorio, usando una validación cruzada estricta y un conjunto de prueba externo procedente de otros hospitales en el caso de los pólipos. En casi todas las métricas de rendimiento —como la precisión global, la capacidad de separar tejido enfermo del sano y la estabilidad en pruebas repetidas— CIM, especialmente con una mezcla más intensa (α alrededor de 0,8), obtuvo los mejores resultados. Los investigadores también inspeccionaron mapas de calor que muestran dónde “mira” el modelo cuando toma decisiones. Los modelos entrenados con CIM se centraron con mayor precisión en las regiones lesionadas verdaderas, coincidiendo mejor con las anotaciones médicas que los métodos rivales y sugiriendo que CIM ayuda a la red a aprender características más clínicamente relevantes en lugar de atajos o ruido.
Qué significa esto para el cribado futuro del cáncer intestinal
En términos sencillos, CIM ofrece a los ordenadores de los médicos más y mejores imágenes de práctica al insertar lesiones reales en ubicaciones nuevas y creíbles de una manera que respeta la anatomía. Este enfoque reduce el desequilibrio entre condiciones comunes y raras, refuerza la detección de enfermedades tempranas y sutiles, y funciona sin modelos generativos pesados y difíciles de controlar ni redes auxiliares adicionales. Aunque el trabajo actual se centra en decisiones binarias —lesión o no lesión— la misma estrategia podría ampliarse a múltiples tipos de lesión y probarse en otros sistemas de órganos. Si se adopta ampliamente, CIM y herramientas similares de “mezcla” de datos conscientes de la anatomía podrían hacer la endoscopia asistida por ordenador más fiable, ayudando a los especialistas a encontrar cambios peligrosos en el tracto digestivo de forma más precoz y consistente.
Cita: Neto, A., Almeida, E., Libânio, D. et al. Cut instance mixing: A domain-specific data augmentation method applied to gastrointestinal lesion detection. Sci Rep 16, 11941 (2026). https://doi.org/10.1038/s41598-026-42138-2
Palabras clave: lesiones gastrointestinales, imagen endoscópica, aumento de datos, aprendizaje profundo, cribado del cáncer