Clear Sky Science · pl
Otoczka endogennego retrowirusa pawiana (ERV) pseudotypowana na wektorach lentivirusowych przewyższa ludzkie ERV-lentivektory w transdukcji komórek T, B, NK i HSPC
Przekształcanie wirusów w pożyteczne ciężarówki dostawcze
Współczesne terapie genowe często opierają się na wyjałowionych wirusach, które działają jak mikroskopijne ciężarówki dostawcze, przenosząc korekcyjne geny do krwi i komórek odpornościowych pacjentów. Jednak nie wszystkie „ciężarówki” wirusowe równie dobrze docierają do właściwych miejsc. W tym badaniu porównano dwa takie pojazdy — jeden oparty na wirusie pawiana, drugi na ludzkim endogennym wirusie — aby sprawdzić, który efektywniej dostarcza geny do kluczowych komórek odpornościowych i krwiotwórczych komórek macierzystych, istotnych dla przyszłych terapii przeciwnowotworowych, immunologicznych i genowych. 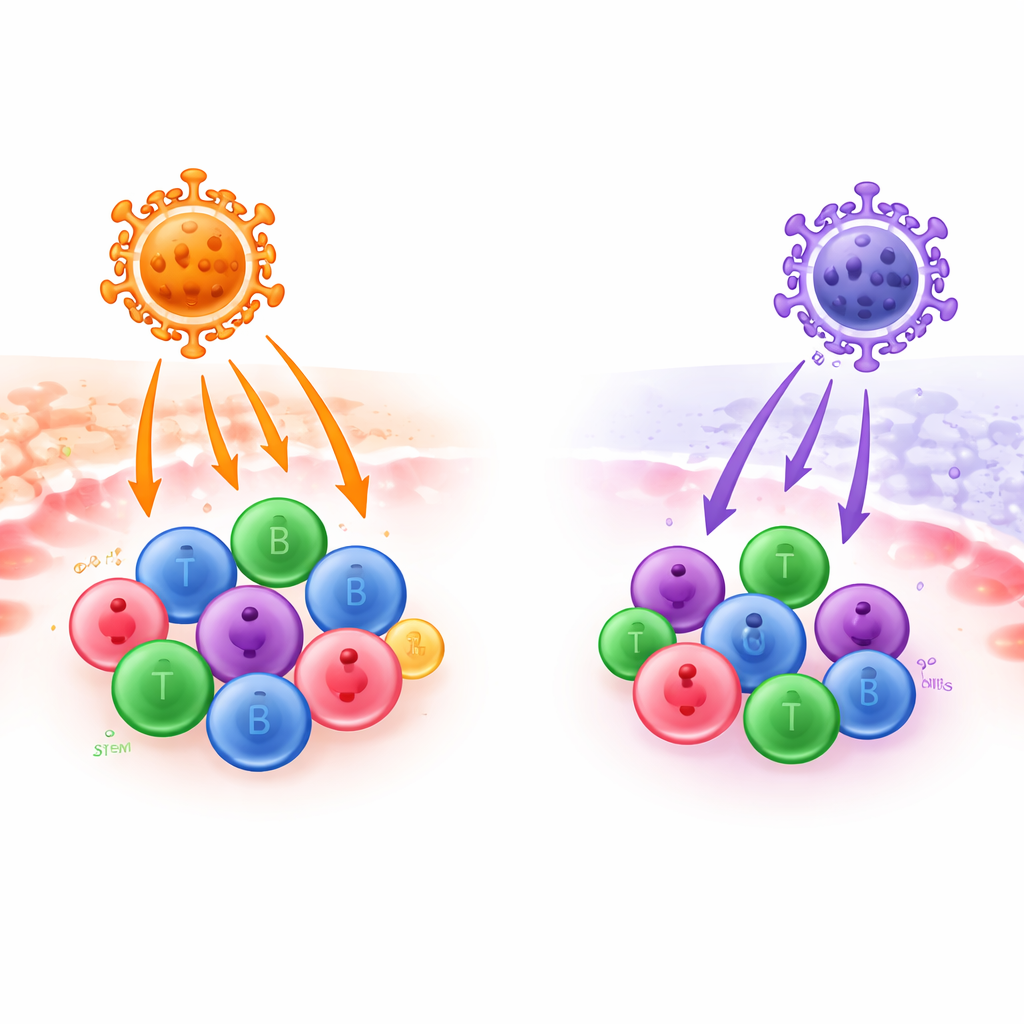
Dlaczego wybór otoczki wirusowej ma znaczenie
Aby zmieniać funkcję komórek odpornościowych, takich jak limfocyty T, limfocyty B, komórki natural killer (NK) i hematopoetyczne komórki macierzyste, badacze terapii genowej często używają wektorów lentivirusowych: unieszkodliwionych wirusów, które potrafią wprowadzić nowe DNA do genomu komórki. Zewnętrzna powłoka, czyli otoczka tych wektorów, decyduje o tym, które komórki mogą one zakażać, wiążąc się z określonymi „drzwiami” na powierzchni komórki. Powszechnie stosowana otoczka VSV-G ma trudności z komórkami odpoczywającymi, ponieważ jej docelowy receptor jest tam rzadki. Oznacza to, że lekarze muszą silnie pobudzać komórki mieszankami czynników wzrostu przed transferem genów — krok, który może niezamierzenie zmieniać tożsamość komórek lub osłabiać potencjał regeneracyjny komórek macierzystych.
Otoczki pawiana kontra ludzkie
Autorzy skupili się na dwóch otoczkach, które wykorzystują ten sam zestaw komórkowych „drzwi”: transportery ASCT-1 i ASCT-2, naturalnie obfite na wielu komórkach krwi i układu odpornościowego. Jedna otoczka pochodzi od endogennego retrowirusa pawiana (BaEV), druga od ludzkiego endogennego retrowirusa z rodziny W (HERV-W), znanego między innymi z udziału w tworzeniu łożyska. Zespół skonstruował wektory lentivirusowe z każdą z tych otoczek i starannie zoptymalizował ich produkcję. Choć testowali kilka zmodyfikowanych wariantów ludzkiej otoczki, niemodyfikowana wersja HERV-W dała ostatecznie najwyższe użyteczne plony wektorów spośród wersji ludzkich, choć nadal przy niższych mianach niż wektory oparte na pawianie. 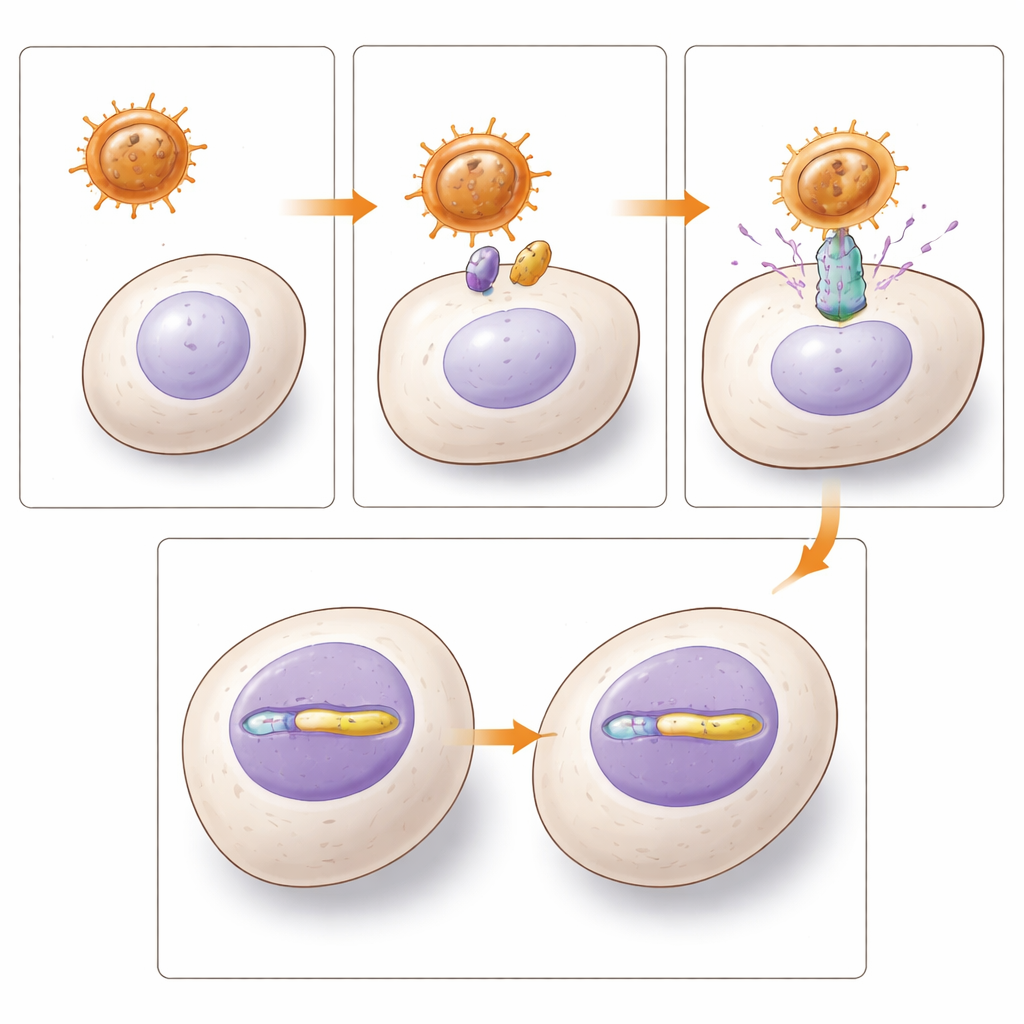
Jak dobrze każdy wektor dociera do komórek odpornościowych
Następnie badacze sprawdzili, jak efektywnie każdy typ wektora potrafi wprowadzić gen reporterowy do ludzkich komórek odpornościowych pobranych od dawców. W limfocytach T stymulowanych przez receptor antygenowy — sytuacji podobnej do przygotowania komórek do terapii CAR-T — oba wektory działały, ale wektor pawiani rutynowo modyfikował około dwukrotnie więcej komórek niż wektor ludzki przy tej samej dawce. Przy łagodniejszej stymulacji sygnałami przeżycia IL-7 i IL-15 różnica się pogłębiła: wektory pawiana docierały do około 70–80% limfocytów T, podczas gdy wektory HERV‑W osiągały jedynie około 10%. Zastosowane do limfocytów B i komórek NK, wektory pawiana ponownie wypadały wyraźnie lepiej — umożliwiały wysoką efektywność transfekcji przy umiarkowanych dawkach, podczas gdy otoczka ludzka wymagała znacznie większych dawek, aby osiągnąć niższe poziomy modyfikacji.
Dotarcie do źródła: ludzkie krwiotwórcze komórki macierzyste
Ponieważ hematopoetyczne komórki macierzyste i progenitorowe (CD34+ HSPC) stoją u szczytu hierarchii krwiotwórczej, są naturalnym celem korekcji wrodzonych chorób krwi. Zespół wykazał, że oba wektory mogą modyfikować te komórki po krótkiej ekspozycji na czynniki wzrostu. Jednak wektor oparty na pawianie osiągał silną transfekcję przy średnich dawkach, podczas gdy wektor HERV‑W wymagał dużo wyższych dawek, aby uzyskać podobne wyniki. Aby sprawdzić, czy zmodyfikowane komórki macierzyste nadal potrafią odbudować układ krwiotwórczy przypominający ludzki, badacze przeszczepili je do wyspecjalizowanej immunodeficjentnej linii mysiej (NBSGW), która wspiera rozwój ludzkiej krwi. U wszystkich sześciu myszy otrzymujących komórki traktowane BaEV ponad 80% ludzkich komórek we wszystkich badanych tkankach — szpiku kostnym, śledzionie, grasicy i krwi — nosiło wprowadzony gen. W przeciwieństwie do tego, tylko jedna z pięciu myszy otrzymujących komórki traktowane HERV‑W osiągnęła taki poziom; kilka wykazywało znacznie niższe procenty, co ujawniło bardziej zmienną i mniej niezawodną wydajność.
Co to oznacza dla przyszłych terapii genowych
Dla laika kluczowy wniosek jest taki, że nie wszystkie wirusowe „ciężarówki” dostawcze są jednakowe, nawet jeśli wydaje się, że używają tych samych drzwi do wejścia do komórek. W tym bezpośrednim porównaniu otoczka pochodzenia pawianiego pozwalała na bardziej konsekwentne i wysokopoziomowe dostarczanie genów do szerokiego zakresu ludzkich komórek odpornościowych i krwiotwórczych komórek macierzystych niż otoczka ludzka HERV‑W. To sprawia, że wektory lentivirusowe oparte na BaEV są szczególnie atrakcyjne dla terapii, które wymagają efektywnej i łagodnej reprogramacji limfocytów T, B, komórek NK i komórek macierzystych bez nadmiernej pre-stymulacji. Otoczka ludzka nadal wypada lepiej od niektórych tradycyjnych opcji i może być użyteczna w określonych sytuacjach, ale obecnie otoczka pawiana wygląda na bardziej wydajne i niezawodne narzędzie dla wielu terapii genowych i komórkowych nowej generacji.
Cytowanie: Périan, S., Castellano, E., Costa, C. et al. Baboon endogenous retrovirus (ERV) envelope pseudotyped lentiviral vectors outperform human ERV lentivectors for transduction of T, B, NK and HSPCs. Gene Ther 33, 144–155 (2026). https://doi.org/10.1038/s41434-025-00587-w
Słowa kluczowe: wektory lentivirusowe, terapia genowa, komórki układu odpornościowego, hematopoetyczne komórki macierzyste, otoczki wirusowe