Clear Sky Science · it
I vettori lentivirali pseudotipizzati con l’involucro del retrovirus endogeno di babbuino (ERV) superano i lentivettori da ERV umano per la trasduzione di T, B, NK e HSPC
Trasformare i virus in utili mezzi di consegna
Le terapie geniche moderne spesso si basano su virus svuotati che funzionano come microscopici mezzi di consegna, trasportando geni correttivi nelle cellule del sangue e del sistema immunitario dei pazienti. Ma non tutti i “mezzi” virali sono ugualmente efficaci nel raggiungere le destinazioni desiderate. Questo studio confronta due di questi veicoli — uno derivato da un virus di babbuino e uno da un virus endogeno umano — per valutare quale riesca a trasferire i geni in modo più efficiente nelle principali cellule immunitarie e nelle cellule staminali del sangue, centrali per le future terapie contro il cancro, le malattie immunitarie e quelle genetiche. 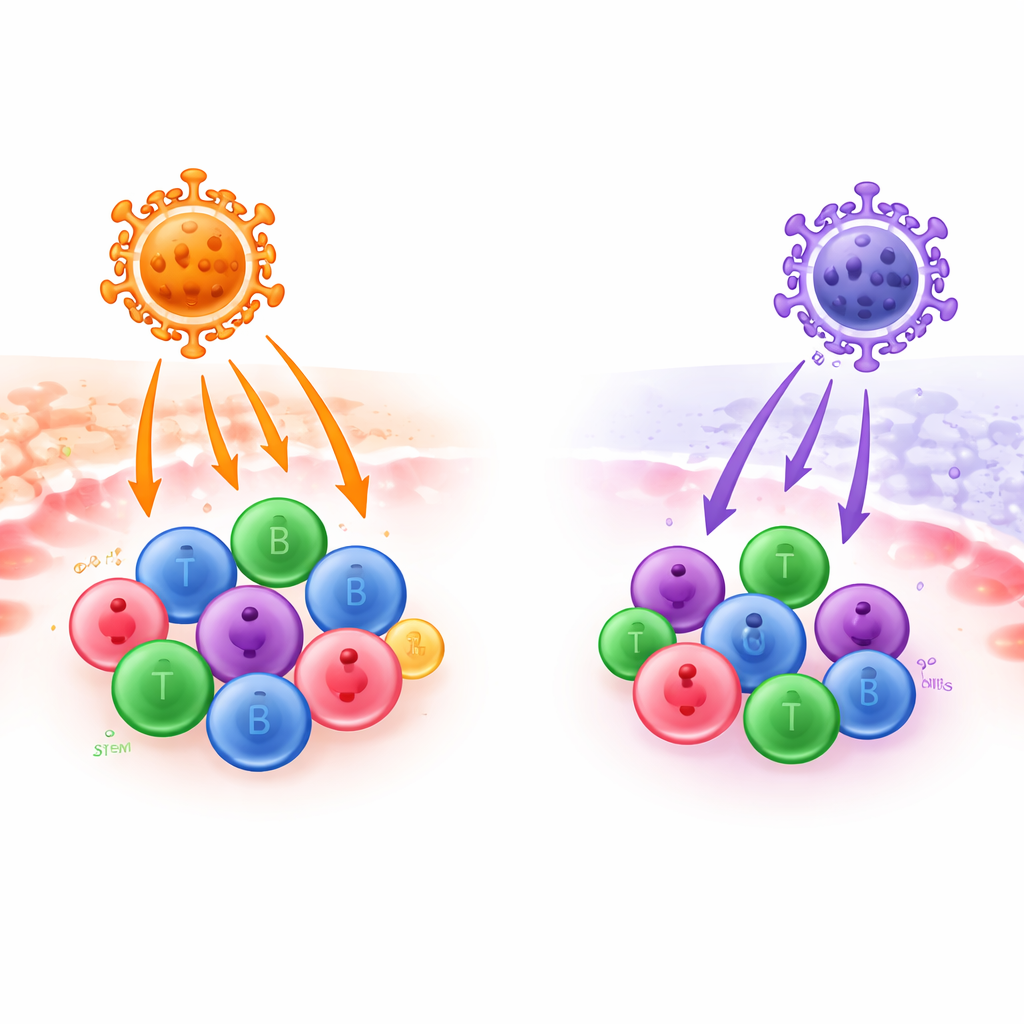
Perché la scelta dell’involucro virale conta
Per modificare il comportamento di cellule immunitarie come le cellule T, B, le natural killer (NK) e le cellule staminali ematopoietiche, i ricercatori di terapia genica spesso impiegano vettori lentivirali: virus inattivati in grado di inserire nuovo DNA nel genoma cellulare. Il rivestimento esterno, o involucro, di questi vettori determina quali cellule possono essere infettate legandosi a specifiche proteine “porta” sulla superficie cellulare. Un involucro ampiamente usato, chiamato VSV-G, fatica con le cellule immunitarie a riposo perché la sua proteina di ingresso è scarsa in quel contesto. Ciò costringe i clinici a stimolare fortemente le cellule con cocktail di segnali di crescita prima del trasferimento genico, un passaggio che può alterare involontariamente l’identità cellulare o ridurre il potenziale rigenerativo delle cellule staminali.
Babbuino contro involucri virali umani
Gli autori si sono concentrati su due involucri che entrambi usano la stessa coppia di “porte” cellulari, proteine di trasporto note come ASCT-1 e ASCT-2, naturalmente abbondanti in molte cellule del sangue e del sistema immunitario. Un involucro proviene da un retrovirus endogeno di babbuino (BaEV) e l’altro da un retrovirus endogeno umano della famiglia W (HERV-W), noto soprattutto per il suo ruolo nella formazione della placenta. Il gruppo ha ingegnerizzato vettori lentivirali con ciascun involucro e ha ottimizzato accuratamente la loro produzione. Sebbene siano state testate diverse versioni modificate dell’involucro umano, la versione non modificata di HERV-W ha in realtà prodotto i più alti rendimenti utilizzabili tra le versioni umane testate, sebbene a titoli ancora inferiori rispetto ai vettori basati sul babbuino. 
Quanto bene ogni vettore raggiunge le cellule immunitarie
I ricercatori hanno quindi valutato quanto efficacemente ciascun tipo di vettore potesse introdurre un gene reporter in cellule immunitarie umane prelevate da donatori. Nelle cellule T stimolate attraverso il recettore per l’antigene — una situazione simile alla preparazione delle cellule T per le terapie CAR-T — entrambi i vettori hanno funzionato, ma il vettore derivato dal babbuino ha sistematicamente prodotto circa il doppio delle cellule modificate rispetto al vettore umano a pari dose. Con una stimolazione più lieve, usando segnali di sopravvivenza come IL-7 e IL-15, il divario è aumentato drasticamente: i vettori babbuino hanno raggiunto circa il 70–80% delle cellule T, mentre i vettori HERV-W hanno raggiunto solo circa il 10%. Applicati a cellule B e NK, il vettore babbuino ha nuovamente mostrato prestazioni nettamente superiori. Poteva indurre elevati livelli di trasferimento genico a dosi relativamente modeste, mentre l’involucro umano richiedeva dosi molto più alte per ottenere livelli di modifica inferiori.
Raggiungere la fonte: le cellule staminali del sangue umane
Poiché le cellule staminali e progenitrici ematopoietiche (CD34+ HSPC) stanno al vertice della gerarchia ematica, sono bersagli ideali per correggere malattie del sangue ereditarie. Il team ha dimostrato che entrambi i vettori possono modificare queste cellule staminali dopo una breve esposizione a fattori di crescita. Tuttavia, il vettore basato sul babbuino ha ottenuto un robusto trasferimento genico a dosi medie, mentre il vettore HERV-W ha richiesto dosaggi molto più elevati per risultati simili. Per verificare se le cellule staminali modificate fossero ancora in grado di ricostituire un sistema ematico di tipo umano, i ricercatori le hanno trapiantate in una speciale linea murina immunodeficiente (NBSGW) che supporta lo sviluppo ematico umano. In tutti e sei i topi che hanno ricevuto cellule trattate con BaEV, oltre l’80% delle cellule umane nel midollo osseo, nella milza, nel timo e nel sangue portava il gene introdotto. Al contrario, solo uno dei cinque topi che hanno ricevuto cellule trattate con HERV-W ha raggiunto quel livello; diversi animali mostravano percentuali molto più basse, rivelando prestazioni più variabili e meno affidabili.
Che cosa significa per le future terapie geniche
Per il pubblico generale, il messaggio chiave è che non tutti i mezzi virali di consegna sono equivalenti, anche se sembrano usare le stesse porte per entrare nelle cellule. In questo confronto diretto, l’involucro derivato dal babbuino ha consentito una consegna genica più coerente e di alto livello in un’ampia gamma di cellule immunitarie umane e nelle cellule staminali del sangue rispetto all’involucro umano HERV-W. Ciò rende i vettori lentivirali basati su BaEV particolarmente attraenti per terapie che richiedono una riprogrammazione efficiente e delicata di cellule T, B, NK e staminali senza eccessiva pre-stimolazione. L’involucro umano mostra comunque prestazioni migliori rispetto ad alcune opzioni tradizionali e può essere utile in situazioni specifiche, ma attualmente l’involucro del babbuino sembra lo strumento più potente e affidabile per molte terapie geniche e cellulari di nuova generazione.
Citazione: Périan, S., Castellano, E., Costa, C. et al. Baboon endogenous retrovirus (ERV) envelope pseudotyped lentiviral vectors outperform human ERV lentivectors for transduction of T, B, NK and HSPCs. Gene Ther 33, 144–155 (2026). https://doi.org/10.1038/s41434-025-00587-w
Parole chiave: vettori lentivirali, terapia genica, cellule del sistema immunitario, cellule staminali ematopoietiche, involucri virali