Clear Sky Science · ar
متجهات لنتيفيروس مُغلفة بغلاف فيروس رتريوفيروسي داخلي للقرد البابون تتفوق على متجهات رتروية بشرية لغلاف ERV في نقل الجينات إلى الخلايا T وB وNK وخلايا السلف المكوّنة للدم
تحويل الفيروسات إلى شاحنات توصيل مفيدة
تعتمد العلاجات الجينية الحديثة غالبًا على فيروسات مُعطّلة تعمل مثل شاحنات توصيل ميكروسكوبية، تحمل جينات تصحيحية إلى خلايا الدم والجهاز المناعي لدى المرضى. لكن ليست كل "الشاحنات" الفيروسية جيدة بنفس القدر في الوصول إلى الوجهات الصحيحة. تقارن هذه الدراسة بين مركبتين من هذه المركبات — إحداهما مبنية على فيروس قرد البابون والأخرى على فيروس بشري داخلي — لمعرفة أيهما يستطيع توصيل الجينات بكفاءة أكبر إلى الخلايا المناعية الرئيسية وخلايا السلف الدموية التي تمثل محور العلاجات المستقبلية للسرطان والاضطرابات المناعية والأمراض الوراثية. 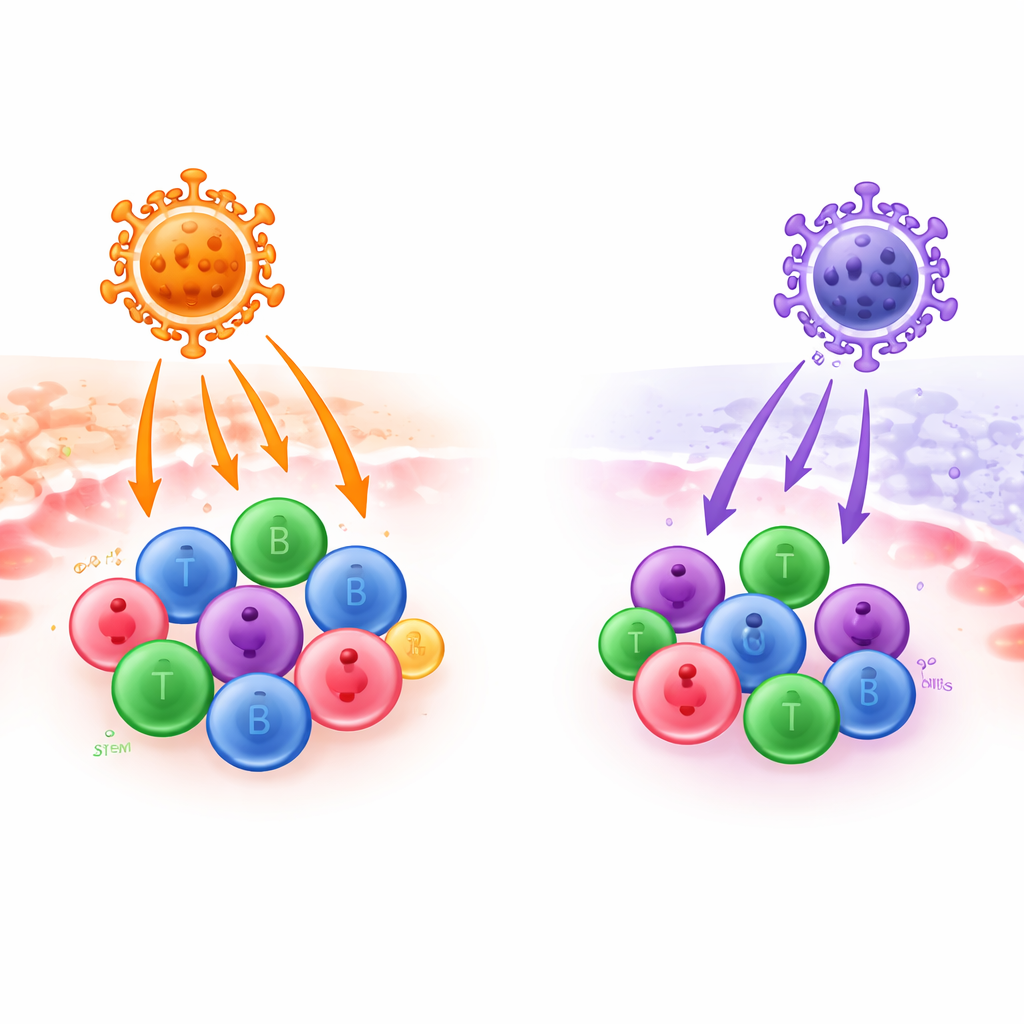
لماذا يهم اختيار الغلاف الفيروسي
لتغيير سلوك خلايا مناعية مثل الخلايا T وB والخلايا القاتلة الطبيعية (NK) وخلايا السلف المكوّنة للدم، يستخدم الباحثون في العلاج الجيني غالبًا متجهات لنتيفيروس: فيروسات مُعطّلة يمكنها إدخال حمض نووي جديد إلى جينوم الخلايا. يحدد الغلاف الخارجي، أو الغلاف، لهذه المتجهات الخلايا التي يمكنها دخولها عبر الارتباط ببروتينات "البوابات" المحددة على سطح الخلية. الغلاف المستخدم على نطاق واسع، المسمى VSV-G، يواجه صعوبة مع الخلايا المناعية الراقدة لأن بروتين البوابة الذي يستخدمه نادر هناك. وهذا يعني أن الأطباء يضطرون إلى تحفيز الخلايا بقوة بمزيجات من إشارات النمو قبل نقل الجين، وهي خطوة قد تغير هوية الخلية أو تقلل من القدرة التجددية للخلايا الجذعية بشكل غير مقصود.
أغلفة فيروس البابون مقابل الأغلفة الفيروسية البشرية
ركز المؤلفون على غلافين يستخدمان الزوج نفسه من بوابات الخلايا، بروتينات نقل معروفة باسم ASCT-1 وASCT-2، التي تتواجد بشكل طبيعي بوفرة على كثير من خلايا الدم والمناعة. أحد الأغلفة مشتق من فيروس رتروفي روسي داخلي للبابون (BaEV)، والآخر من فيروس رتروفي داخلي بشري من عائلة W (HERV-W)، المعروف أكثر بدوره في تكوين المشيمة. صمّم الفريق متجهات لنتيفيروس مزوّدة بكل غلاف وقام بتحسين إنتاجها بعناية. ورغم أنهم اختبروا عدة نسخ مُعدّلة من الغلاف البشري، فإن النسخة غير المعدلة من HERV-W أنتجت فعليًا أعلى عوائد متجه قابلة للاستخدام، وإن كانت بعواصم أقل من المتجهات المبنية على البابون.
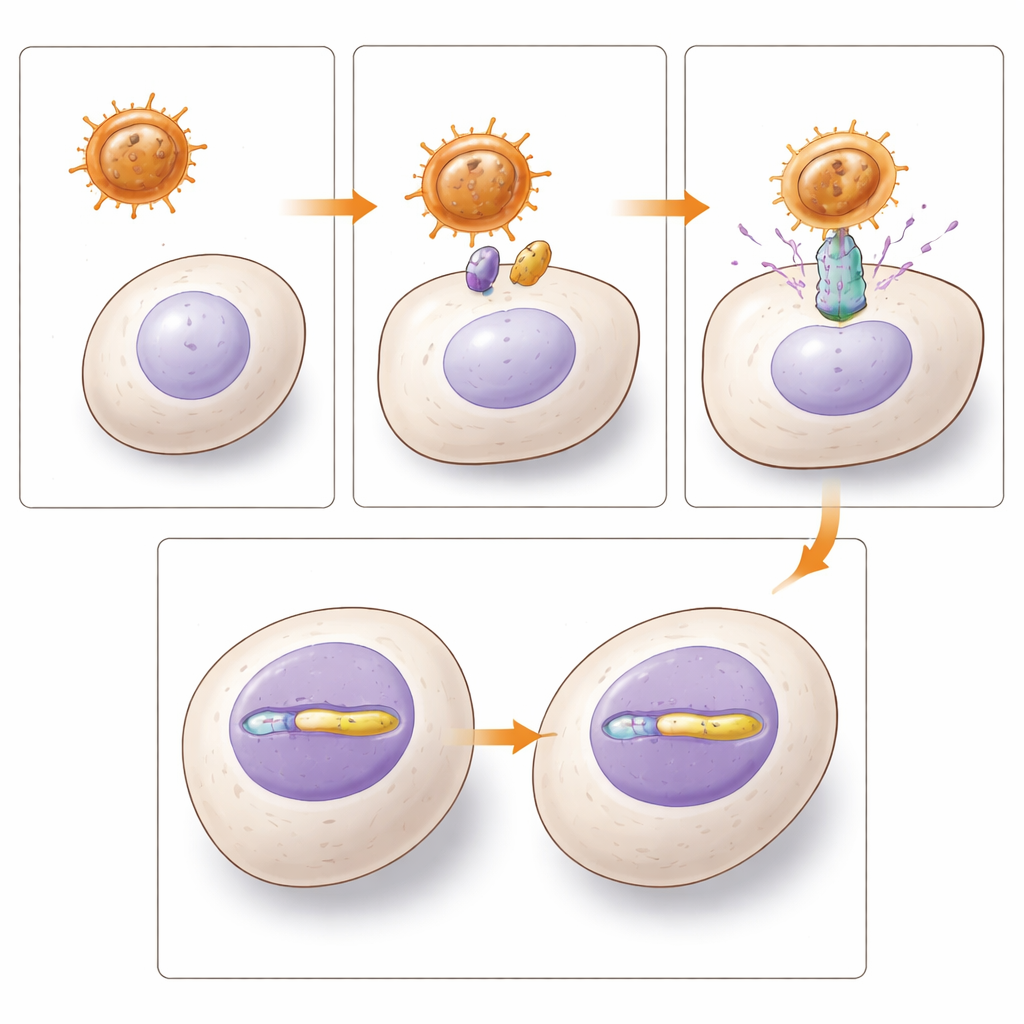
مدى وصول كل متجه إلى الخلايا المناعية
سأل الباحثون بعد ذلك مدى كفاءة كل نوع من المتجهات في إدخال جين تقرير إلى خلايا مناعية بشرية تم جمعها من متبرعين. في خلايا T المحفّزة عبر مستقبل المستضد — حالة تشبه إعداد خلايا T لعلاجات CAR-T — عملت كلا المتجهتين، لكن متجه البابون أنتج بانتظام نحو ضعف عدد الخلايا المعدّلة مقارنة بالمتجه البشري عند نفس الجرعة. تحت تحفيز أخف بإشارات البقاء IL-7 وIL-15، اتسع الفارق بشكل كبير: وصلت متجهات البابون إلى نحو 70–80% من خلايا T، بينما وصلت متجهات HERV-W إلى حوالي 10% فقط. عند التطبيق على خلايا B وNK، تفوّق متجه البابون مرة أخرى بوضوح. فقد أتاح نقل جيني عاليًا بجرعات متواضعة نسبيًا، بينما احتاج غلاف HERV-W إلى جرعات أعلى بكثير لتحقيق مستويات تعديل أدنى.
الوصول إلى المصدر: خلايا السلف الدموية البشرية
بما أن خلايا السلف والمُقدِّرة المكوّنة للدم (CD34+ HSPCs) تشغل قمة تسلسل الدم، فهي أهداف رئيسية لتصحيح أمراض الدم الوراثية. أظهر الفريق أن كلا المتجهين قادران على تعديل هذه الخلايا بعد تعرض قصير لعوامل النمو. ومع ذلك، حقق المتجه المعتمد على البابون نقلًا جينيًا قويًا بجرعات متوسطة، بينما تطلب متجه HERV-W جرعات أعلى بكثير للحصول على نتائج مماثلة. وللتحقق مما إذا كانت الخلايا المعدّلة لا تزال قادرة على إعادة بناء جهاز دموي شبيه بالبشر، زرع الباحثون هذه الخلايا في سلالة فئران متخصصة ناقصة المناعة (NBSGW) تدعم تطور الدم البشري. في جميع الفئران الست التي تلقت خلايا عولجت بـBaEV، حملت أكثر من 80% من الخلايا البشرية في نخاع العظم والطحال والقصبة الدموية والدم الجين المُدخل. في المقابل، وصلت فأر واحد من بين خمسة تلقى خلايا معالجة بـHERV-W إلى ذلك المستوى؛ وأظهرت عدة فئران نسبًا أقل بكثير، مما كشف عن أداء أكثر تباينًا وأقل موثوقية.
ماذا يعني هذا لمستقبل العلاجات الجينية
للقارئ غير المتخصص، الرسالة الأساسية هي أن ليس كل شاحنة توصيل فيروسية متساوية، حتى لو بدت وكأنها تستخدم نفس الأبواب للدخول إلى الخلايا. في هذه المقارنة المباشرة، سمح الغلاف المشتق من البابون بتوصيل جينات بمستويات أعلى وأكثر ثباتًا إلى مجموعة واسعة من الخلايا المناعية البشرية وخلايا السلف الدموية مقارنةً بغلاف HERV-W البشري. وهذا يجعل المتجهات المعتمدة على BaEV جذابة بشكل خاص للعلاجات التي تعتمد على إعادة برمجة فعالة ولطيفة لخلايا T وB وNK والخلايا الجذعية دون تحفيز مفرط مسبقًا. لا يزال الغلاف البشري يتفوق على بعض الخيارات التقليدية وقد يكون مفيدًا في حالات معينة، لكن غلاف البابون يبدو حاليًا الأداة الأقوى والأكثر موثوقية للعديد من علاجات الخلايا والجينات من الجيل التالي.
الاستشهاد: Périan, S., Castellano, E., Costa, C. et al. Baboon endogenous retrovirus (ERV) envelope pseudotyped lentiviral vectors outperform human ERV lentivectors for transduction of T, B, NK and HSPCs. Gene Ther 33, 144–155 (2026). https://doi.org/10.1038/s41434-025-00587-w
الكلمات المفتاحية: متجهات لنتيفيروس, العلاج الجيني, الخلايا المناعية, الخلايا الجذعية المكونة للدم, أغلفة فيروسية