Clear Sky Science · pl
SPT6 utrzymuje homeostazę naskórka, hamując pętlę sprzężenia zwrotnego NF-κB i zapobiegając nadmiernemu zapaleniu
Dlaczego ważne jest wyciszenie alarmu skórnego
Skóra to nasz największy organ i pierwsza bariera wobec świata zewnętrznego. Aby nas chronić, komórki skóry muszą szybko wykrywać zagrożenia, a jednocześnie unikać wywoływania niepotrzebnych alarmów, które prowadzą do przewlekłego zaczerwienienia, łuszczenia i bólu. W tym badaniu opisano, jak mało znane białko SPT6 pomaga utrzymać system alarmowy skóry pod kontrolą. Gdy SPT6 zostaje utracone w kluczowych komórkach skóry, tkanka przechyla się w kierunku zapalenia przypominającego łuszczycę i wolniej się goi po urazie, co ujawnia, jak delikatna jest równowaga między ochroną a nadreakcją.
Jak komórki skóry działają jako przednie wartownie
Zewnętrzna warstwa skóry, naskórek, składa się z keratynocytów — komórek, które nieustannie się odnawiają i tworzą szczelną barierę. Te komórki robią znacznie więcej niż biernie siedzieć; wyczuwają drobnoustroje i uszkodzenia oraz uwalniają sygnały chemiczne przyciągające komórki odpornościowe. Autorzy postawili pytanie, czy specjalne komórki przypominające komórki macierzyste u podstawy naskórka nie tylko podnoszą alarm, ale także aktywnie tłumią nadmierne zapalenie. Skoncentrowali się na SPT6, białku pomagającym genom w prawidłowym włączaniu, by sprawdzić, czy działa jako wbudowany hamulec sygnałów zapalnych.
Gdy strażnik zostaje usunięty ze skóry myszy
Używając genetycznie zmodyfikowanych myszy, zespół selektywnie usunął gen Supt6 (kodujący SPT6) w keratynocytach podstawnych. W ciągu kilku dni zwierzęta rozwinęły pogrubioną, łuszczącą się skórę na grzbiecie, uszach i łapach, wraz z utratą włosów i spadkiem masy ciała. Badania mikroskopowe i ultrastrukturalne wykazały charakterystyczne cechy obserwowane w łuszczycy: nadmiernie pogrubiały naskórek, przylegające warstwy martwych komórek na powierzchni, nieprawidłowe połączenia międzykomórkowe oraz naciek komórek odpornościowych w tkance. Pomimo tych dramatycznych zmian skórnych, inne miejsca nabłonkowe pozytywne dla K14, takie jak język i przełyk, pozostały strukturalnie prawidłowe, co wskazuje na rolę SPT6 skoncentrowaną w skórze.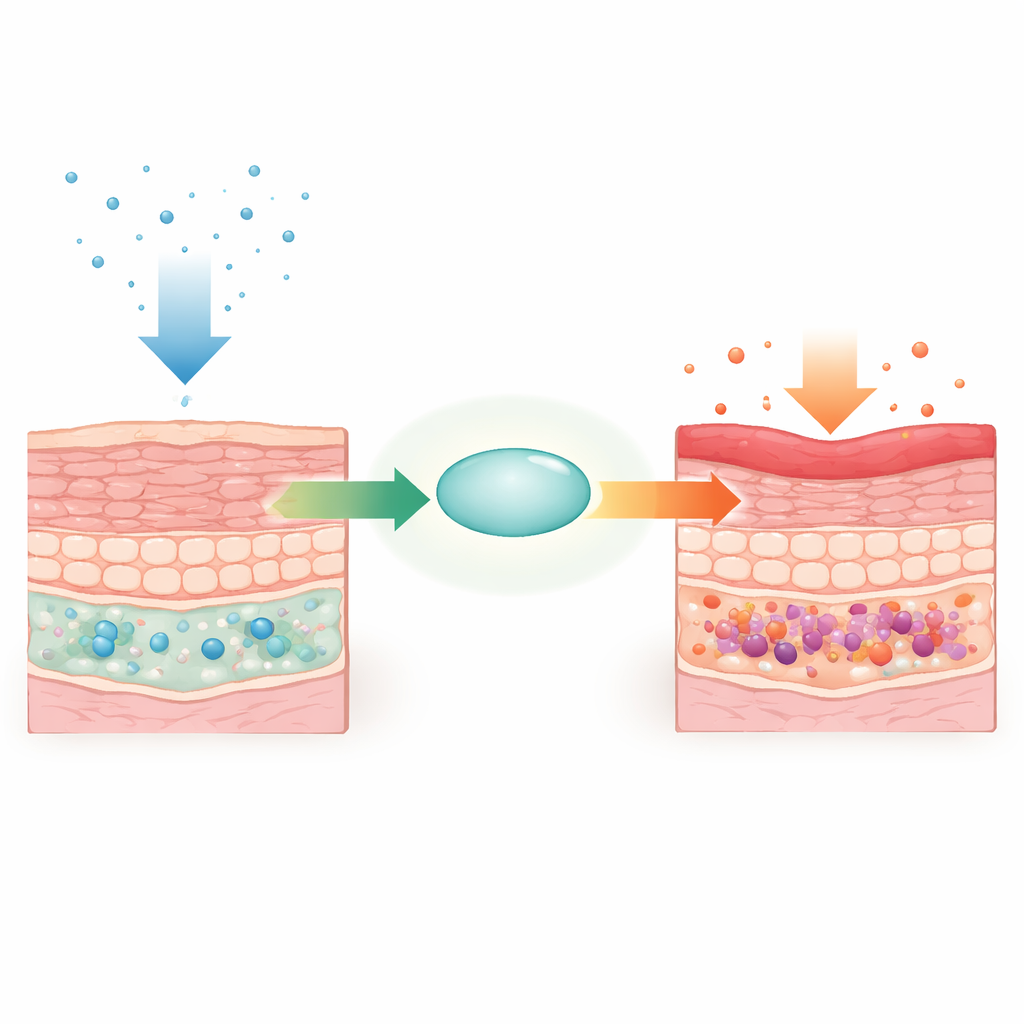
Zapalenie przy jednoczesnym przedwczesnym dojrzewaniu skóry i wolniejszej naprawie
Profilowanie aktywności genów ujawniło, że tysiące genów zmieniło ekspresję po utracie SPT6. Szlaki związane z adhezją komórkową i naprawą Wnt zostały osłabione, podczas gdy geny kontrolujące podział komórek, dojrzewanie skóry i odpowiedzi zapalne były znacznie zwiększone. Markery późnej różnicowania naskórka były podwyższone, co oznacza, że skóra wydawała się nadmiernie „dojrzała”, ale zaburzona. Gdy badacze wykonali rany pełnej grubości, myszy pozbawione SPT6 goiły się znacząco wolniej. Wiele genów związanych z szlakiem Wnt — znanym z napędzania wzrostu włosów i zamykania ran — wykazywało obniżenie, a wcześniejsze dane o wiązaniu pokazywały, że SPT6 lokalizuje się przy kilku z tych genów naprawczych. Sugeruje to, że SPT6 wspiera zdrową regenerację, jednocześnie powstrzymując programy zapalne.
Podpis przypominający łuszczycę, który pochodzi z wnętrza
Geny związane z zapaleniem, takie jak Il1b, Il6, Tnf i S100a8/a9, były wyraźnie zwiększone w skórze pozbawionej SPT6. Wzorzec zmian genetycznych silnie przypominał ten obserwowany w standardowym modelu mysim łuszczycy i w ludzkich zmianach łuszczycowych. Neutrofile gromadziły się na powierzchni skóry w strukturach przypominających mikroabscesy Munro, klasyczną cechę łuszczycy. Jednak eliminacja bakterii za pomocą szerokospektralnych antybiotyków, badania pod kątem grzybów i powszechnych wirusów skórnych, a nawet transfer mikrobiomu skórnego między myszami nie zmieniły przebiegu choroby. Sekwencjonowanie RNA pojedynczych komórek wykazało, że konkretne podgrupy keratynocytów podstawnych i pośrednich się rozszerzyły i przyjęły silnie zapalne oraz pro‑różnicujące programy, co wskazuje, że napęd choroby pochodzi z samych keratynocytów, a nie z najeżdżających drobnoustrojów.
Jak SPT6 blokuje samo-wzmacniającą pętlę zapalną
Zbliżając się do mechanizmu, badacze studiowali ludzkie keratynocyty w hodowli. Gdy obniżyli poziom SPT6, a następnie naśladowali sygnały wirusowe lub uszkodzeniowe, komórki uwolniły falę genów zapalnych kontrolowanych przez NF-κB, główny przełącznik odpowiedzi immunologicznych. Lek blokujący NF-κB częściowo odwrócił ten wzrost i złagodził zapalenie skóry u myszy pozbawionych SPT6. Zespół odkrył następnie, że SPT6 wiąże region wzmacniający (enhancer) w pobliżu genu RELA, który koduje kluczową podjednostkę NF-κB, p65. Bez SPT6 więcej p65 wiązało zarówno ten enhancer, jak i promotor RELA, tworząc pętlę dodatniego sprzężenia zwrotnego: p65 napędza większą aktywność własnego genu, co z kolei dodatkowo zwiększa ekspresję genów zapalnych.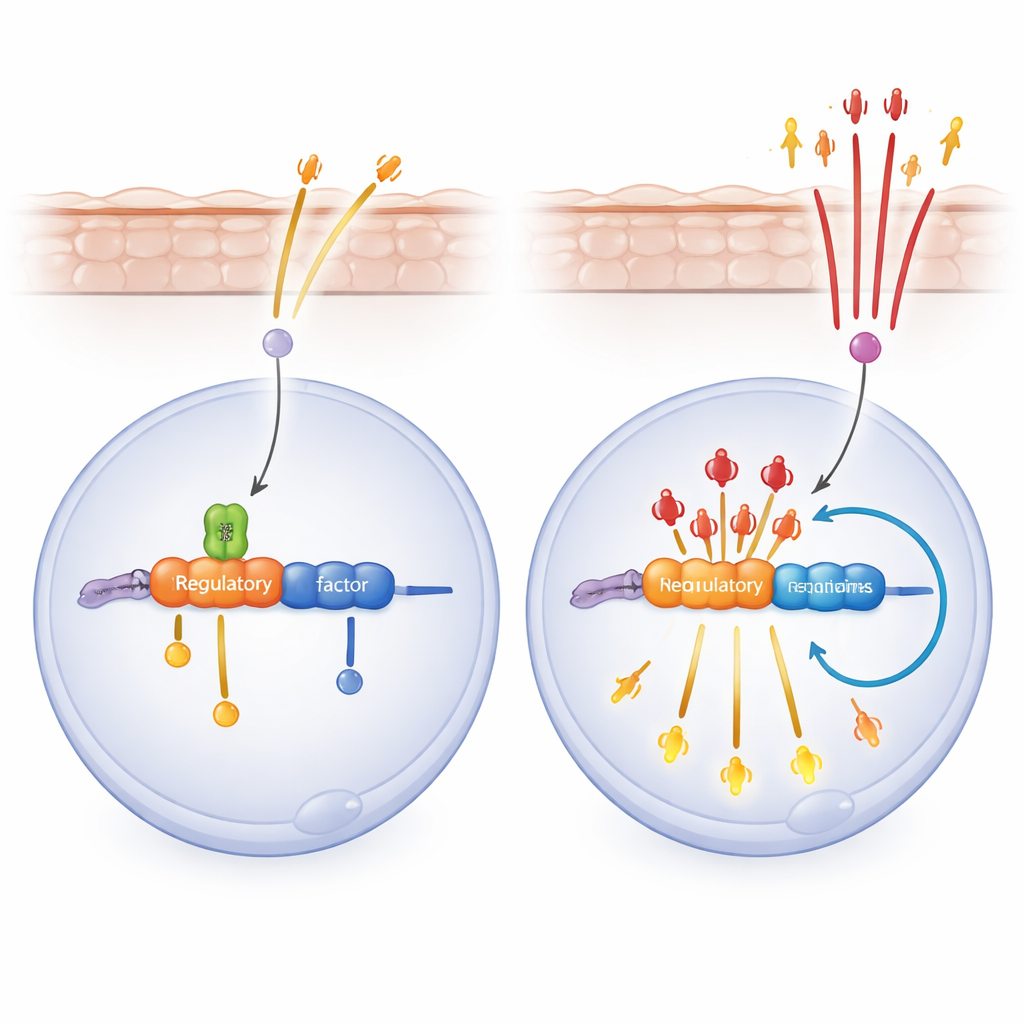
Co to oznacza dla zrozumienia i leczenia chorób skóry
Dla czytelnika niebędącego specjalistą przekaz jest taki, że skóra jest z natury skłonna do zapalnej reakcji, ale pozostaje spokojna tylko dlatego, że wewnętrzne hamulce, takie jak SPT6, stale tłumią odpowiedź. Gdy SPT6 zostanie usunięte z keratynocytów podstawnych, komórki te nadmiernie różnicują się, wysyłają silniejsze sygnały alarmowe i wprowadzają tkankę w stan przypominający łuszczycę oraz utrudnione gojenie ran, wszystko to bez wyraźnej infekcji. Pokazując, że SPT6 powstrzymuje pętlę sprzężenia zwrotnego NF-κB przy genie RELA, praca ta uwypukla precyzyjny punkt kontroli, który mógłby być celem terapii łagodzącej przewlekłe zapalenie skóry przy jednoczesnym zachowaniu zdolności organizmu do walki z prawdziwymi zagrożeniami.
Cytowanie: Sun, Y., Xu, S., Wang, D. et al. SPT6 maintains epidermal homeostasis by inhibiting an NF-κB-positive feedback loop to prevent excessive inflammation. Cell Mol Immunol 23, 471–490 (2026). https://doi.org/10.1038/s41423-026-01410-1
Słowa kluczowe: zapalenie skóry, łuszczyca, keratynocyty, szlak sygnalizacji NF-kappaB, gojenie ran