Clear Sky Science · fr
SPT6 maintient l’homéostasie épidermique en inhibant une boucle de rétroaction positive NF-κB pour prévenir une inflammation excessive
Pourquoi il est important d’apaiser le système d’alarme de la peau
La peau est notre plus grand organe et notre première barrière contre le monde extérieur. Pour nous protéger, les cellules cutanées doivent détecter rapidement le danger, tout en évitant de déclencher des alertes inutiles qui conduisent à des rougeurs chroniques, des desquamations et des douleurs. Cette étude révèle comment une protéine peu connue, SPT6, aide à maîtriser le système d’alarme cutané. Lorsque SPT6 est perdu dans des cellules clés de la peau, le tissu bascule vers une inflammation de type psoriasique et la guérison après blessure est ralentie, montrant combien l’équilibre entre protection et réaction excessive est fragile.
Comment les cellules cutanées jouent les sentinelles de première ligne
La couche externe de la peau, l’épiderme, est composée de kératinocytes — des cellules qui se renouvellent en permanence et forment une barrière étanche. Ces cellules font bien plus que rester passives ; elles détectent les microbes et les lésions et libèrent des signaux chimiques qui attirent les cellules immunitaires. Les auteurs se sont demandé si des cellules particulières de type souches, situées à la base de l’épiderme, n’étaient pas seulement capables de lancer des alertes, mais aussi d’atténuer activement une inflammation excessive. Ils se sont concentrés sur SPT6, une protéine qui aide les gènes à s’activer correctement, pour savoir si elle agit comme un frein intégré aux signaux inflammatoires.
Quand un gardien est retiré de la peau de la souris
En utilisant des souris génétiquement modifiées, l’équipe a supprimé de façon sélective le gène Supt6 (qui produit SPT6) dans les kératinocytes basaux. En quelques jours, les animaux ont développé une peau épaissie et squameuse sur le dos, les oreilles et les pattes, accompagnée d’une perte de poils et d’une perte de poids. Des études en microscopie et en ultrastructure ont montré des caractéristiques typiques du psoriasis : un épiderme excessivement épais, des couches collantes de cellules mortes à la surface, des attaches intercellulaires défectueuses et un afflux de cellules immunitaires dans le tissu. Malgré ces changements cutanés spectaculaires, d’autres sites épithéliaux positifs pour K14, comme la langue et l’œsophage, restaient structurellement normaux, indiquant un rôle centré sur la peau pour SPT6.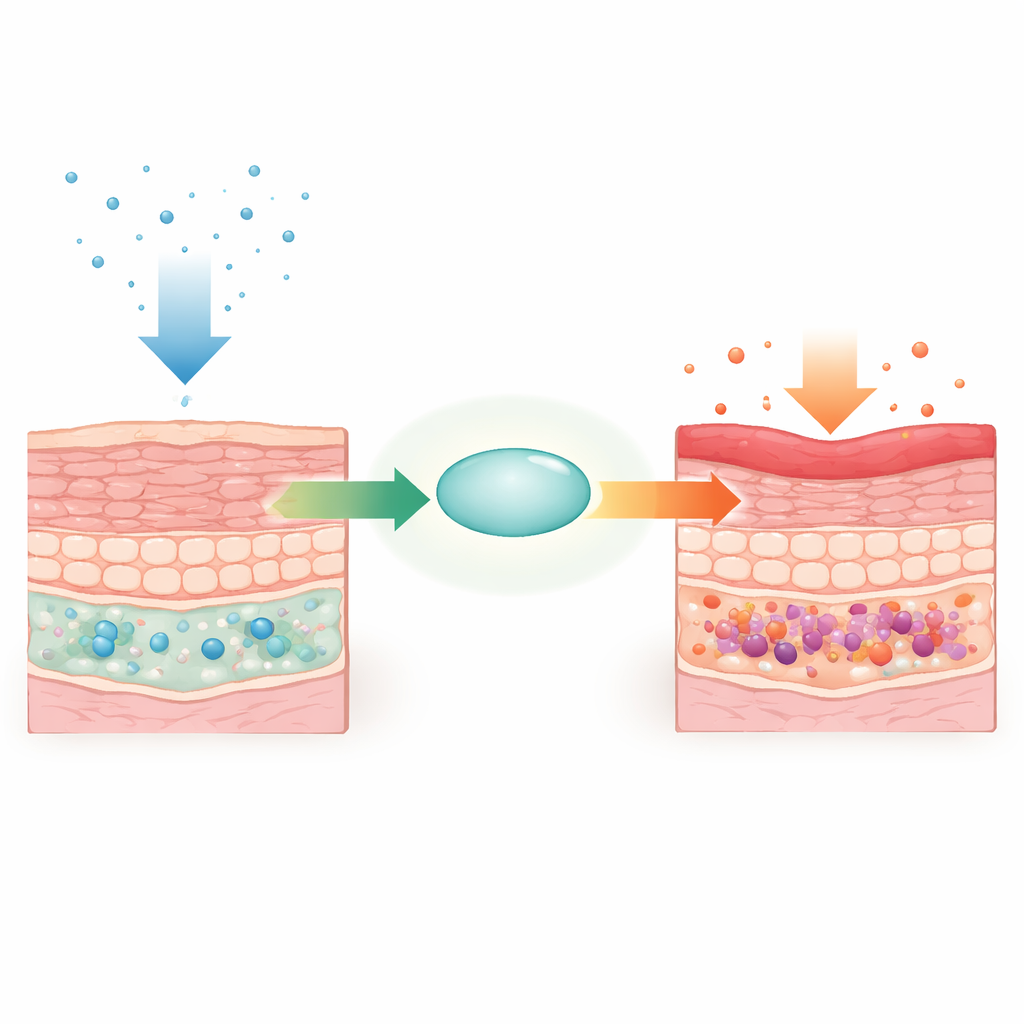
Une peau inflammée mais trop mature et une réparation plus lente
Le profilage de l’activité génique a révélé que des milliers de gènes changeaient lorsque SPT6 était absent. Les voies d’adhésion cellulaire et de réparation Wnt étaient diminuées, tandis que les gènes contrôlant la division cellulaire, la maturation cutanée et les réponses inflammatoires étaient fortement augmentés. Des marqueurs de différenciation épidermique tardive étaient élevés, ce qui signifie que la peau paraissait excessivement « mature » mais désordonnée. Lorsque les chercheurs ont infligé des plaies en pleine épaisseur, les souris déficientes en SPT6 cicatrisaient significativement plus lentement. De nombreux gènes impliqués dans la voie Wnt — connue pour stimuler la croissance des poils et la fermeture des plaies — étaient réduits, et des données de liaison antérieures montraient que SPT6 est présent sur plusieurs de ces gènes de réparation. Cela suggère que SPT6 soutient une régénération saine tout en maintenant sous contrôle les programmes inflammatoires.
Une signature de type psoriasique qui émerge de l’intérieur
Des gènes liés à l’inflammation tels que Il1b, Il6, Tnf et S100a8/a9 étaient fortement augmentés dans la peau déficiente en SPT6. Le schéma de modifications géniques ressemblait fortement à celui observé dans un modèle murin standard du psoriasis et dans des lésions psoriasiques humaines. Des neutrophiles s’accumulaient à la surface cutanée dans des structures rappelant les microabcès de Munro, caractéristique classique du psoriasis. Pourtant, l’élimination des bactéries avec des antibiotiques à large spectre, le dépistage de champignons et de virus cutanés courants, et même le transfert de microbes cutanés entre souris n’ont pas modifié la maladie. Le séquençage unicellulaire de l’ARN a montré que des sous-groupes spécifiques de kératinocytes basaux et intermédiaires se sont étendus et ont adopté des programmes fortement inflammatoires et pro-différenciation, indiquant que la poussée vers la maladie provient des kératinocytes eux-mêmes plutôt que de microbes envahissants.
Comment SPT6 bloque une boucle inflammatoire auto-amplificatrice
En se penchant sur le mécanisme, les chercheurs ont étudié des kératinocytes humains en culture. Lorsqu’ils ont réduit SPT6 puis simulé des signaux viraux ou de dommage, les cellules ont déclenché une vague de gènes inflammatoires contrôlés par NF-κB, un commutateur majeur des réponses immunitaires. Un médicament qui bloque NF-κB a partiellement inversé cette poussée et réduit l’inflammation cutanée chez les souris déficientes en SPT6. L’équipe a ensuite découvert que SPT6 se lie à une région amplificatrice (enhancer) proche du gène RELA, qui code pour la sous-unité clé p65 de NF-κB. En l’absence de SPT6, davantage de p65 se liait à la fois à cet enhancer et au promoteur de RELA, créant une boucle de rétroaction positive : p65 stimule l’activité de son propre gène, ce qui à son tour amplifie l’expression des gènes inflammatoires.
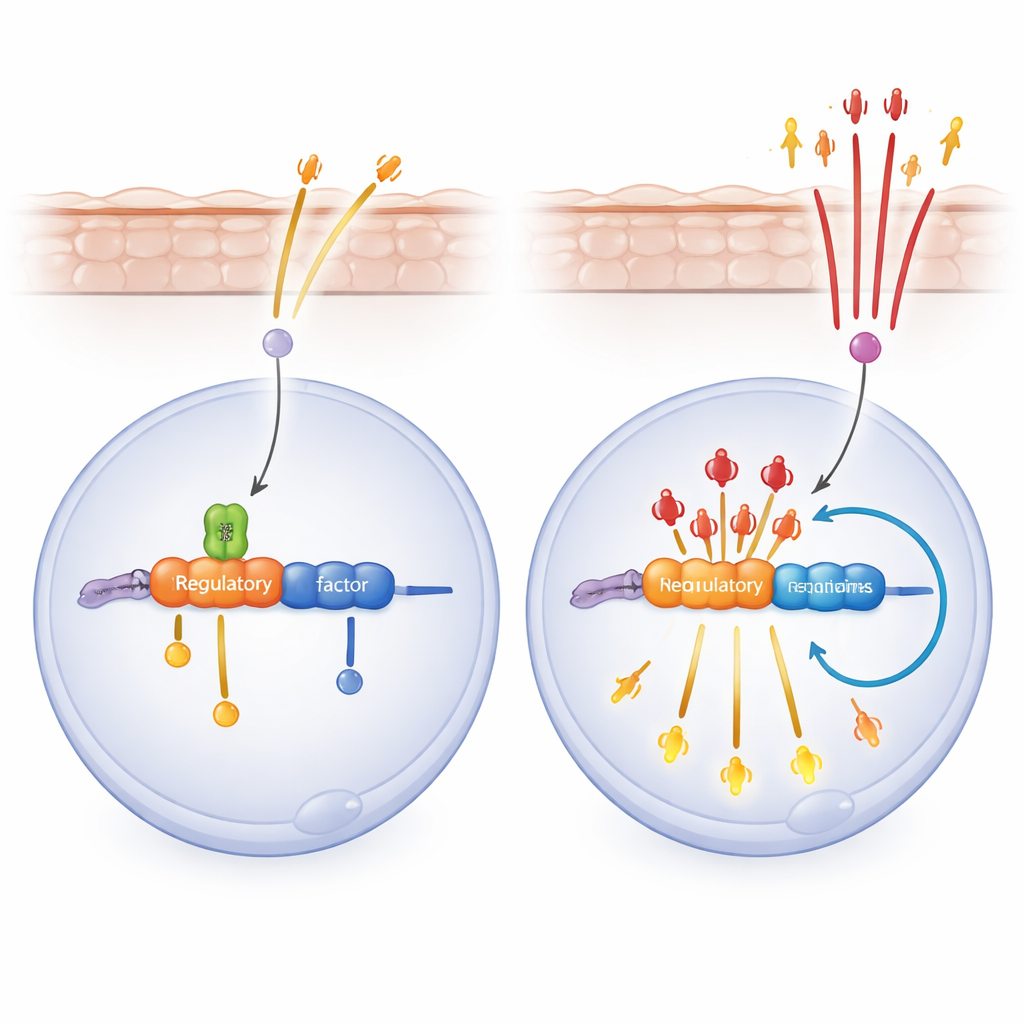
Ce que cela signifie pour la compréhension et le traitement des maladies cutanées
Pour un lecteur non spécialiste, le message est que la peau est naturellement prête à déclencher l’inflammation, mais qu’elle reste silencieuse uniquement parce que des freins internes comme SPT6 maintiennent constamment la réponse sous contrôle. Lorsque SPT6 est supprimé des kératinocytes basaux, ces cellules se sur-différencient, envoient des signaux de détresse plus puissants et entraînent le tissu dans une maladie de type psoriasique et une mauvaise cicatrisation, le tout sans infection évidente. En montrant que SPT6 restreint une boucle de rétroaction NF-κB au niveau du gène RELA, ce travail met en évidence un point de contrôle précis qui pourrait être ciblé pour apaiser l’inflammation cutanée chronique tout en préservant la capacité de l’organisme à combattre de véritables menaces.
Citation: Sun, Y., Xu, S., Wang, D. et al. SPT6 maintains epidermal homeostasis by inhibiting an NF-κB-positive feedback loop to prevent excessive inflammation. Cell Mol Immunol 23, 471–490 (2026). https://doi.org/10.1038/s41423-026-01410-1
Mots-clés: inflammation cutanée, psoriasis, kératinocytes, signalisation NF-kappaB, cicatrisation