Clear Sky Science · de
SPT6 erhält die epidermale Homöostase, indem es eine NF-κB-Positive-Rückkopplungsschleife hemmt, um übermäßige Entzündung zu verhindern
Warum es wichtig ist, das Alarmsystem der Haut zu beruhigen
Die Haut ist unser größtes Organ und unsere erste Schutzschicht gegen die Außenwelt. Um uns zu schützen, müssen Hautzellen Gefahren schnell erkennen, aber unnötige Alarme vermeiden, die zu chronischer Rötung, Schuppung und Schmerzen führen. Diese Studie zeigt, wie ein wenig bekanntes Protein namens SPT6 das Alarmsystem der Haut unter Kontrolle hält. Geht SPT6 in wichtigen Hautzellen verloren, kippt das Gewebe in eine psoriasisähnliche Entzündung und heilt nach Verletzung langsamer — ein Hinweis darauf, wie fragil das Gleichgewicht zwischen Schutz und Überreaktion ist.
Wie Hautzellen als Frontwächter agieren
Die äußerste Hautschicht, das Epithel (Epidermis), besteht aus Keratinozyten — Zellen, die sich ständig erneuern und eine dichte Barriere bilden. Diese Zellen sind nicht passiv; sie erkennen Erreger und Schäden und geben chemische Signale ab, die Immunzellen herbeirufen. Die Autoren fragten, ob spezielle, stammzellähnliche Zellen an der Basis der Epidermis nicht nur Alarme auslösen, sondern auch übermäßige Entzündungen aktiv dämpfen. Sie konzentrierten sich auf SPT6, ein Protein, das hilft, Gene richtig zu aktivieren, um zu prüfen, ob es als eingebautes Bremssystem für entzündliche Signale fungiert.
Wenn ein Wächter aus der Maus-Haut entfernt wird
Mit genetisch veränderten Mäusen löschte das Team selektiv das Supt6-Gen (das SPT6 produziert) in basalen Keratinozyten. Innerhalb weniger Tage entwickelten die Tiere verdickte, schuppige Haut am Rücken, an den Ohren und Pfoten, begleitet von Haarverlust und Gewichtsabnahme. Mikroskopie und Ultrastrukturanalysen zeigten typische Merkmale, wie sie bei Psoriasis vorkommen: eine übermäßig verdickte Epidermis, klebrige Schichten abgestorbener Zellen an der Oberfläche, fehlerhafte Zell-Zell-Verbindungen und eine Ansammlung von Immunzellen im Gewebe. Trotz dieser dramatischen Hautveränderungen blieben andere K14-positive Epithelstellen wie Zunge und Speiseröhre strukturell normal, was auf eine hautspezifische Rolle von SPT6 hindeutet.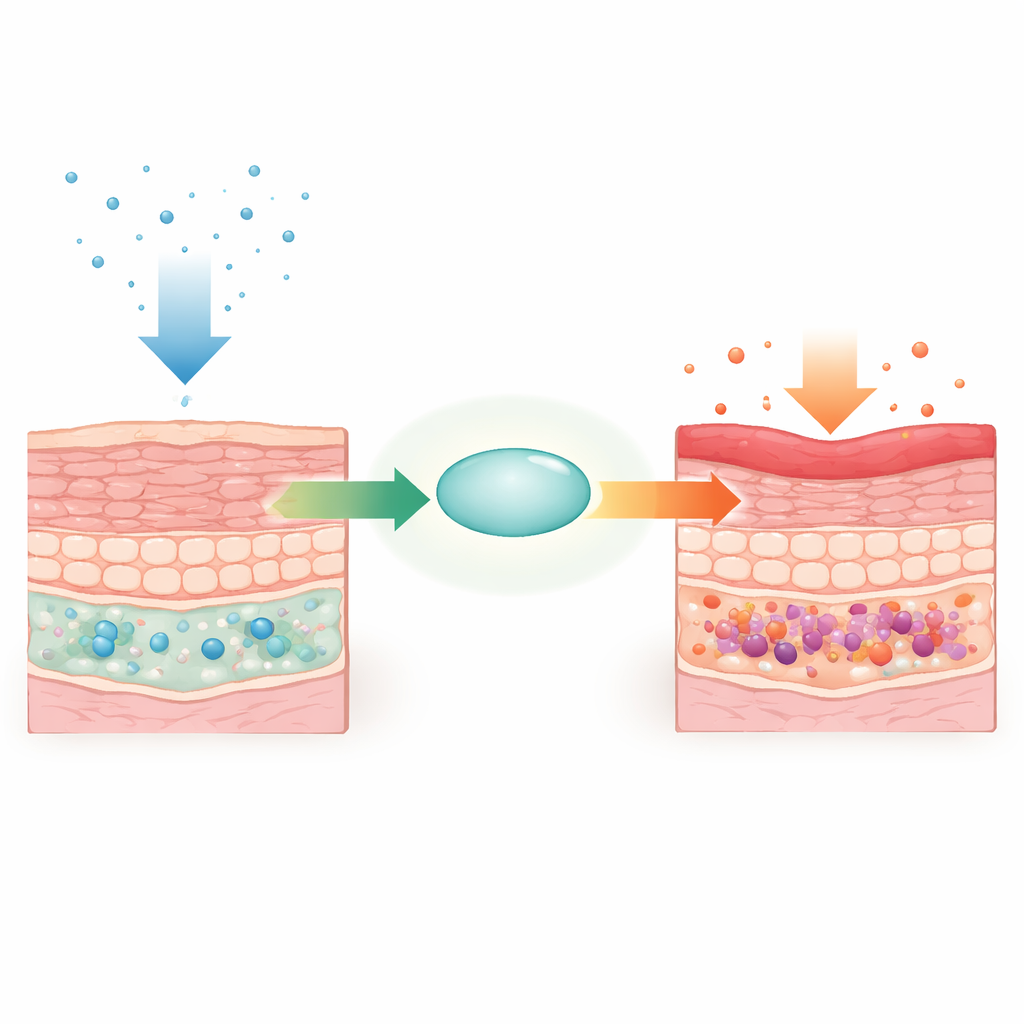
Entzündete, aber überreife Haut und langsamere Reparatur
Die Genexpressionsprofile zeigten, dass beim Verlust von SPT6 Tausende von Genen umgeschaltet wurden. Zelladhäsions- und Wnt-Reparaturwege wurden herunterreguliert, während Gene, die Zellteilung, Hautreifung und entzündliche Reaktionen steuern, stark erhöht waren. Marker der späten epidermalen Differenzierung waren angehoben, was bedeutet, dass die Haut übermäßig „reif“ wirkte, aber gleichzeitig ungeordnet war. Bei Vollschichtwunden heilten SPT6-defiziente Mäuse deutlich langsamer. Viele Gene der Wnt-Signalkette — bekannt dafür, Haarwachstum und Wundverschluss zu fördern — waren vermindert, und frühere Bindungsdaten zeigten, dass SPT6 an mehreren dieser Reparaturgene sitzt. Das legt nahe, dass SPT6 gesunde Regeneration unterstützt, während es entzündliche Programme im Zaum hält.
Eine psoriasisähnliche Signatur, die von innen entsteht
Entzündungsbezogene Gene wie Il1b, Il6, Tnf und S100a8/a9 waren in SPT6-defizienter Haut stark erhöht. Das Muster der Genänderungen ähnelte stark dem eines etablierten Mausmodells für Psoriasis und menschlichen psoriatischen Läsionen. Neutrophile sammelten sich an der Hautoberfläche in Strukturen, die an Munro-Mikroabszesse erinnern, ein klassisches Psoriasis-Merkmal. Das Eliminieren von Bakterien mit Breitbandantibiotika, das Screening auf Pilze und gängige Hautviren und sogar das Übertragen von Hautmikrobiota zwischen Mäusen veränderte die Erkrankung jedoch nicht. Einzelzell-RNA-Sequenzierung zeigte, dass spezifische basale und intermediäre Keratinozyten-Untergruppen expandierten und hochentzündliche sowie pro-differenzierende Programme annahmen, was darauf hinweist, dass die treibende Kraft der Erkrankung von den Keratinozyten selbst ausgeht und nicht von eindringenden Mikroben.
Wie SPT6 eine sich selbst verstärkende Entzündungsschleife blockiert
Bei der Untersuchung des Mechanismus studierten die Forscher menschliche Keratinozyten in Kultur. Reduzierten sie SPT6 und simulierten anschließend virale oder Schadenssignale, entfesselten die Zellen eine Welle entzündlicher Gene, die von NF-κB gesteuert werden, einem Hauptschalter für Immunantworten. Ein Wirkstoff, der NF-κB blockiert, kehrte diese Welle teilweise um und linderte die Hautentzündung bei SPT6-defizienten Mäusen. Das Team entdeckte dann, dass SPT6 an eine Enhancer-Region nahe dem RELA-Gen bindet, das die wichtige NF-κB-Untereinheit p65 kodiert. Ohne SPT6 binden mehr p65-Moleküle sowohl an diesen Enhancer als auch an den RELA-Promoter, wodurch eine positive Rückkopplungsschleife entsteht: p65 fördert die Aktivität seines eigenen Gens und verstärkt dadurch weiter die Expression entzündlicher Gene.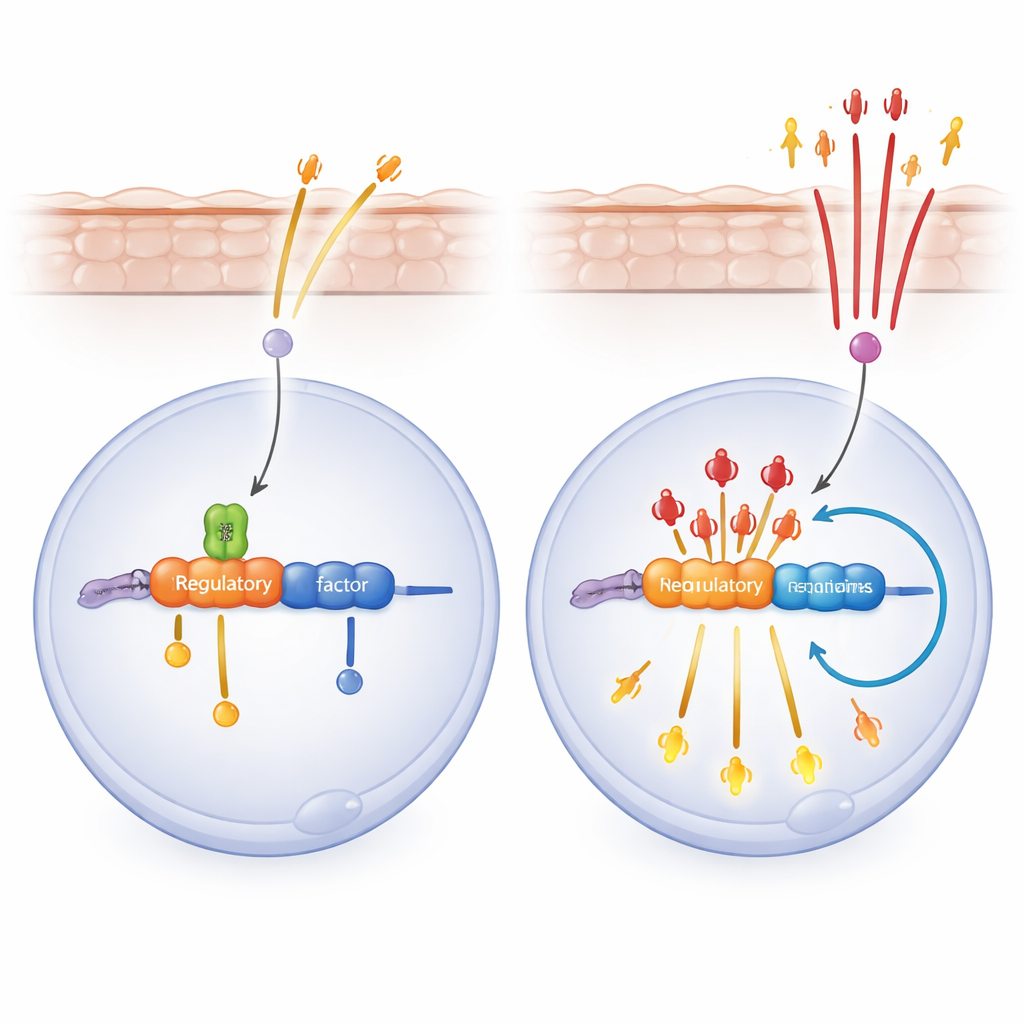
Was das für das Verständnis und die Behandlung von Hautkrankheiten bedeutet
Für Laien lautet die Botschaft: Die Haut ist von Natur aus bereit, Entzündungen auszulösen, bleibt aber still, weil interne Bremsen wie SPT6 die Reaktion ständig kontrollieren. Wird SPT6 in basalen Keratinozyten entfernt, differenzieren diese Zellen übermäßig, senden stärkere Alarmzeichen und ziehen das Gewebe in eine psoriasisähnliche Erkrankung mit schlechter Wundheilung — und das ohne offensichtliche Infektion. Indem gezeigt wird, dass SPT6 eine NF-κB-Rückkopplungsschleife am RELA-Gen einschränkt, hebt diese Arbeit einen spezifischen Kontrollpunkt hervor, der gezielt angegangen werden könnte, um chronische Hautentzündungen zu beruhigen und gleichzeitig die Fähigkeit des Körpers zu erhalten, echte Bedrohungen zu bekämpfen.
Zitation: Sun, Y., Xu, S., Wang, D. et al. SPT6 maintains epidermal homeostasis by inhibiting an NF-κB-positive feedback loop to prevent excessive inflammation. Cell Mol Immunol 23, 471–490 (2026). https://doi.org/10.1038/s41423-026-01410-1
Schlüsselwörter: Hautentzündung, Psoriasis, Keratinozyten, NF-kappaB-Signalgebung, Wundheilung