Clear Sky Science · it
SPT6 mantiene l’omeostasi epidermica inibendo un circuito di retroazione positivo NF-κB per prevenire un’infiammazione eccessiva
Perché è importante calmare il sistema d’allarme della pelle
La pelle è il nostro organo più esteso e la prima barriera contro il mondo esterno. Per proteggerci, le cellule cutanee devono rilevare rapidamente i pericoli, ma evitare di attivare falsi allarmi che provocano arrossamento cronico, desquamazione e dolore. Questo studio rivela come una proteina poco conosciuta chiamata SPT6 aiuti a mantenere sotto controllo il sistema d’allarme cutaneo. Quando SPT6 viene perso in cellule cutanee chiave, il tessuto si sposta verso un’infiammazione simile alla psoriasi e guarisce più lentamente dopo un danno, rivelando quanto sia fragile l’equilibrio tra protezione e sovra‑reazione.
Come le cellule della pelle agiscono da sentinelle in prima linea
Lo strato esterno della pelle, l’epidermide, è costituito da cheratinociti—cellule che si rinnovano continuamente e formano una barriera compatta. Queste cellule fanno molto più che restare passive; avvertono la presenza di germi e danni e rilasciano segnali chimici che richiamano cellule immunitarie. Gli autori hanno chiesto se particolari cellule staminali‑like alla base dell’epidermide non solo lanciassero segnali d’allarme, ma attenuassero attivamente l’infiammazione eccessiva. Si sono concentrati su SPT6, una proteina che aiuta i geni ad attivarsi correttamente, per vedere se agisce come un freno incorporato sui segnali infiammatori.
Quando un guardiano viene rimosso dalla pelle del topo
Usando topi geneticamente modificati, il gruppo ha cancellato selettivamente il gene Supt6 (che codifica SPT6) nei cheratinociti basali. Nel giro di giorni, gli animali hanno sviluppato pelle ispessita e squamosa sul dorso, sulle orecchie e sulle zampe, insieme a perdita di pelo e calo di peso. Microscopia e studi ultrastrutturali hanno mostrato caratteristiche tipiche della psoriasi: epidermide eccessivamente spessa, strati appiccicosi di cellule morte in superficie, giunzioni cellula‑cellula difettose e afflusso di cellule immunitarie nel tessuto. Nonostante questi cambiamenti cutanei drammatici, altri siti epiteliali positivi per K14 come lingua ed esofago sono rimasti strutturalmente normali, indicando un ruolo mirato di SPT6 nella pelle.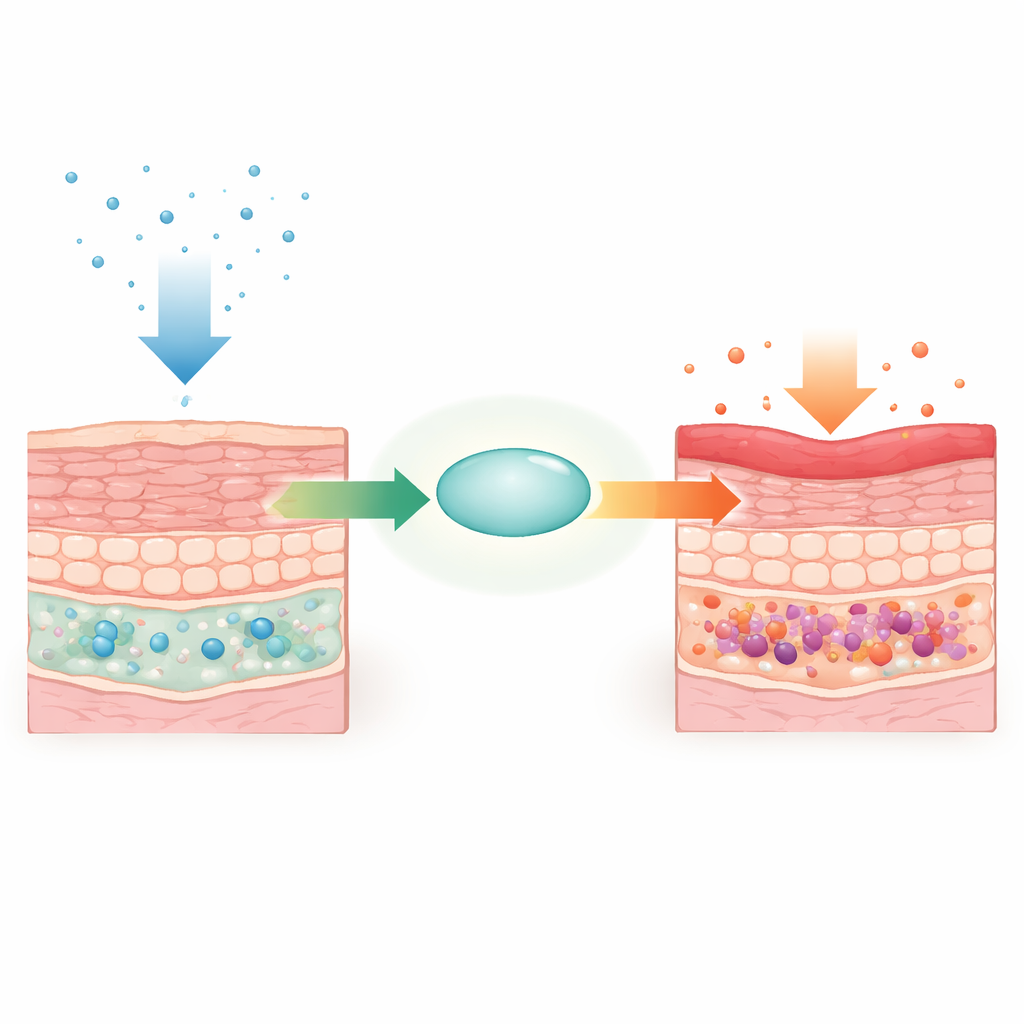
Pelle infiammata ma ipermatura e guarigione rallentata
Il profilo dell’attività genica ha rivelato che migliaia di geni sono cambiati quando SPT6 è venuto meno. Le vie di adesione cellulare e la via Wnt coinvolta nella riparazione sono risultate attenuate, mentre i geni che controllano divisione cellulare, maturazione della pelle e risposte infiammatorie sono stati fortemente potenziati. I marcatori della differenziazione epidermica tardiva erano aumentati, il che significa che la pelle appariva eccessivamente “matura” ma disordinata. Quando i ricercatori hanno creato ferite a tutto spessore, i topi privi di SPT6 hanno guarito significativamente più lentamente. Molti geni della via Wnt—nota per guidare crescita del pelo e chiusura delle ferite—erano ridotti, e dati precedenti di binding mostravano che SPT6 si lega a diversi di questi geni di riparazione. Ciò suggerisce che SPT6 supporta una rigenerazione sana mantenendo sotto controllo i programmi infiammatori.
Una firma simile alla psoriasi che nasce dall’interno
I geni correlati all’infiammazione come Il1b, Il6, Tnf e S100a8/a9 sono risultati fortemente aumentati nella pelle carente di SPT6. Il pattern di variazione genica somigliava molto a quello osservato in un modello murino standard di psoriasi e nelle lesioni psoriasiche umane. I neutrofili si sono accumulati sulla superficie cutanea in strutture ricordanti i microascessi di Munro, una caratteristica classica della psoriasi. Tuttavia, eliminare i batteri con antibiotici ad ampio spettro, eseguire screening per funghi e virus cutanei comuni, e persino trasferire microbi della pelle tra i topi non ha modificato la malattia. L’RNA‑sequenziamento single‑cell ha mostrato che sottoinsiemi specifici di cheratinociti basali e intermedi si sono espansi e hanno adottato programmi altamente infiammatori e pro‑differenziazione, indicando che la spinta verso la malattia proviene dai cheratinociti stessi e non da microbi invasivi.
Come SPT6 blocca un circuito infiammatorio auto‑amplificante
Per approfondire il meccanismo, i ricercatori hanno studiato cheratinociti umani in coltura. Quando hanno ridotto SPT6 e poi simulato segnali virali o da danno, le cellule hanno scatenato un’ondata di geni infiammatori controllati da NF‑κB, un interruttore maestro delle risposte immunitarie. Un farmaco che blocca NF‑κB ha parzialmente invertito questa ondata e attenuato l’infiammazione cutanea nei topi privi di SPT6. Il gruppo ha poi scoperto che SPT6 si lega a una regione enhancer vicino al gene RELA, che codifica la subunità chiave di NF‑κB, p65. In assenza di SPT6, più p65 si lega sia a questo enhancer sia al promotore di RELA, creando un circuito di retroazione positiva: p65 aumenta l’attività del proprio gene, che a sua volta potenzia ulteriormente l’espressione genica infiammatoria.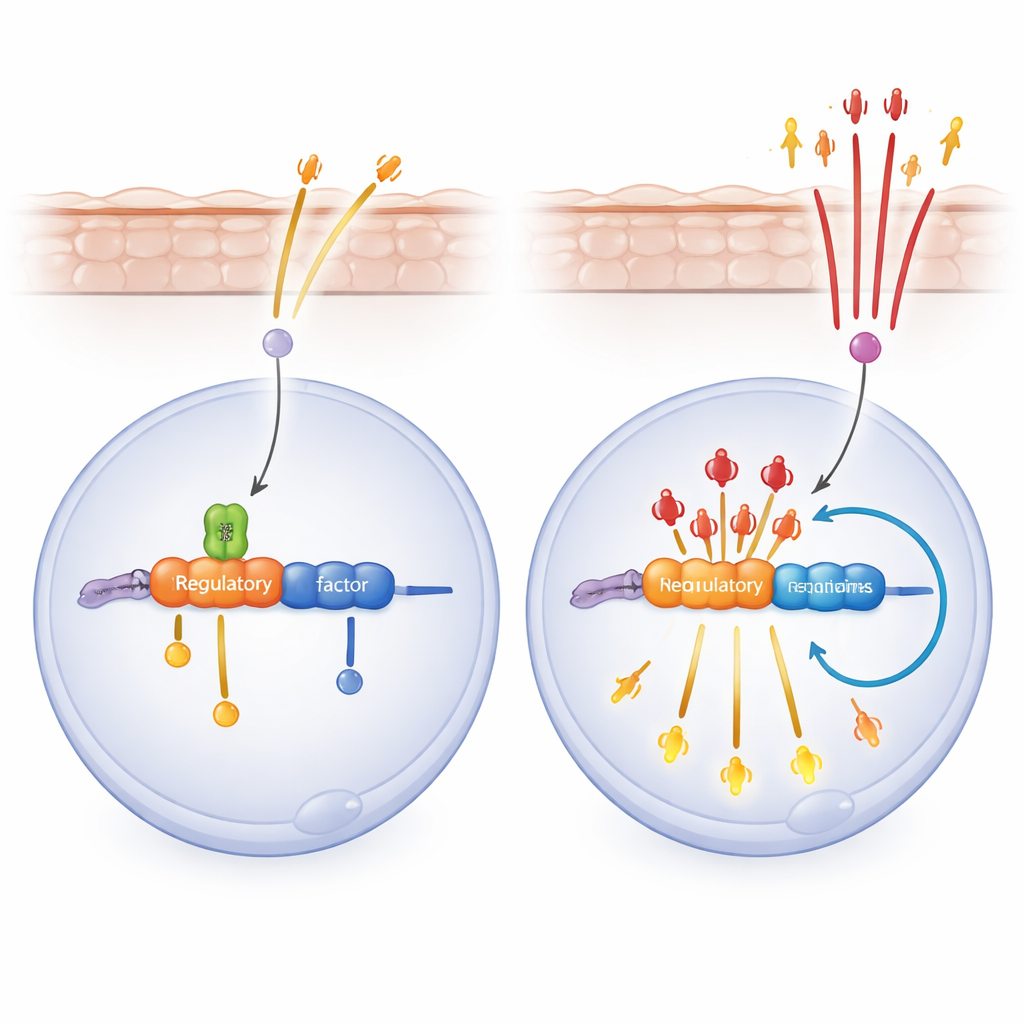
Cosa significa per la comprensione e il trattamento delle malattie cutanee
Per un lettore non esperto, il messaggio è che la pelle è naturalmente predisposta a innescare l’infiammazione, ma rimane silente solo perché freni interni come SPT6 tengono costantemente la risposta sotto controllo. Quando SPT6 viene rimosso dai cheratinociti basali, queste cellule si iperdifferenziano, inviano segnali di stress più forti e trascinano il tessuto verso una malattia simile alla psoriasi e una scarsa riparazione delle ferite, il tutto senza un’infezione evidente. Dimostrando che SPT6 limita un loop di retroazione NF‑κB al gene RELA, questo lavoro mette in luce un punto di controllo preciso che potrebbe essere mirato per calmare l’infiammazione cutanea cronica preservando la capacità dell’organismo di combattere minacce reali.
Citazione: Sun, Y., Xu, S., Wang, D. et al. SPT6 maintains epidermal homeostasis by inhibiting an NF-κB-positive feedback loop to prevent excessive inflammation. Cell Mol Immunol 23, 471–490 (2026). https://doi.org/10.1038/s41423-026-01410-1
Parole chiave: infiammazione della pelle, psoriasi, cheratinociti, segnalazione NF-kappaB, guarigione delle ferite