Clear Sky Science · pl
Celowane na ITK przebudowanie odporności poprawiło skuteczność terapii komórkami CAR-T anty-CD19
Sprawienie, by komórki walczące z rakiem działały dłużej
Terapia komórkami CAR-T zrewolucjonizowała leczenie niektórych nowotworów krwi, przekształcając własne komórki odpornościowe pacjenta w wyspecjalizowanych łowców komórek nowotworowych. Mimo to wielu pacjentów doświadcza nawrotu choroby, ponieważ te zmodyfikowane komórki szybko się męczą i zanikają. W tym badaniu zadano proste, ale istotne pytanie: czy można dać komórkom CAR-T rodzaj „wzmocnienia wytrzymałości immunologicznej”, aby działały dłużej i skuteczniej eliminowały nowotwór?
Dlaczego wzmocnione komórki T mają znaczenie
Komórki CAR-T to spersonalizowane białe krwinki rozpoznające markery na komórkach nowotworowych, takie jak CD19 występujący w wielu chłoniakach i białaczkach komórek B. Po początkowo imponującym ataku te komórki często zwalniają w nieprzyjaznym mikrośrodowisku guza. Wchodzą w wyeksploatowany stan nazywany wyczerpaniem, w którym dzielą się mniej, wydzielają mniej toksycznych cząsteczek i przestają skutecznie zabijać komórki nowotworowe. Badacze skupili się na kluczowym wewnętrznym przełączniku w komórkach T — białku ITK, które przekazuje sygnały aktywacyjne. Wcześniejsze prace na zwierzętach sugerowały, że ciągłe nadmierne uruchamianie tego przełącznika przyczynia się do wypalenia. Tu zespół sprawdzał, czy stłumienie aktywności ITK przy pomocy wysoce selektywnego leku soquelitinibu może utrzymać komórki CAR-T zarówno silne, jak i odporne.
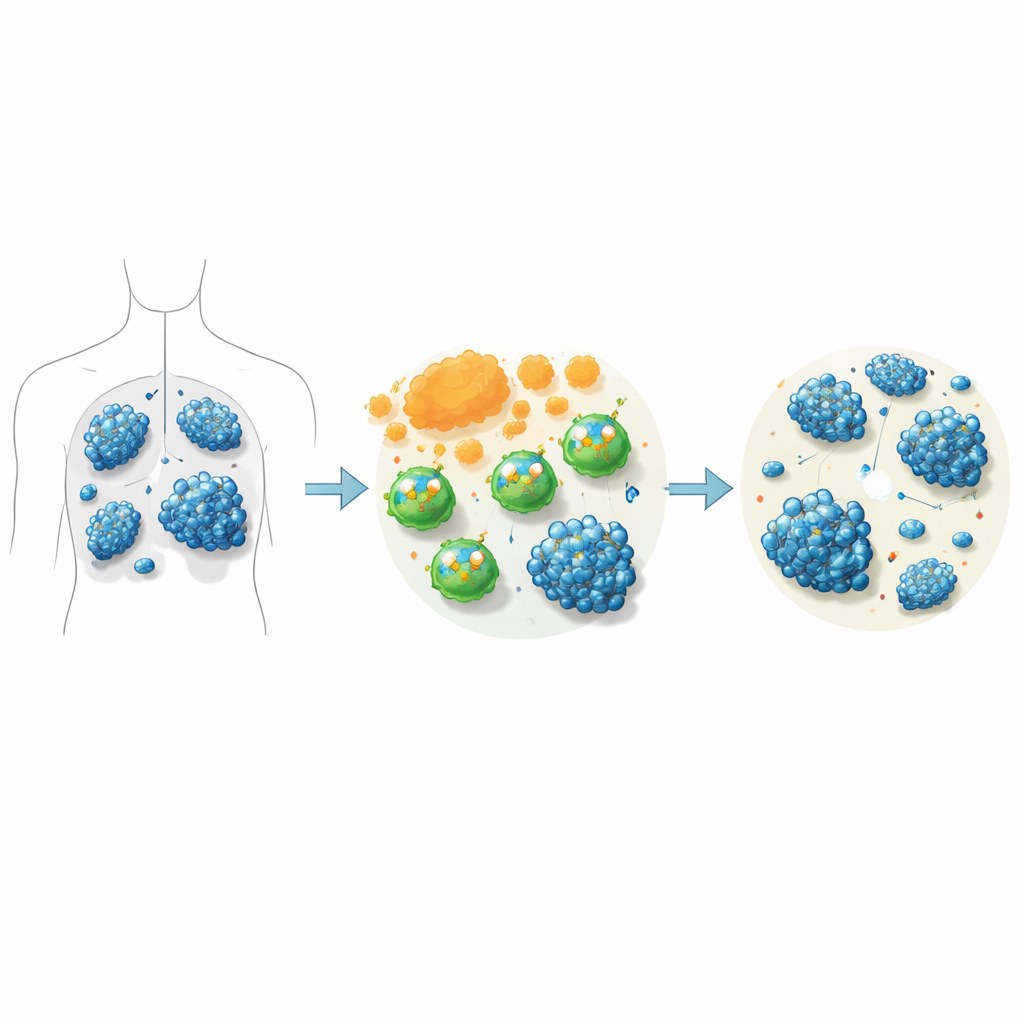
Przyciszanie sygnału, by wzmocnić atak
W eksperymentach laboratoryjnych naukowcy porównali standardowe komórki CAR-T skierowane przeciw CD19 z komórkami CAR-T, w których ITK został zablokowany genetycznie lub za pomocą soquelitinibu. Gdy te komórki zmieszano z ludzkimi komórkami chłoniaka, CAR-T z zablokowanym ITK zniszczyły więcej komórek nowotworowych. Wydzielały też wyższe poziomy kluczowych cząsteczek ataku, takich jak granzyme B, TNF-alfa i interferon-gamma, oraz wykazywały silniejsze oznaki aktywacji. Komórki CAR-T poddane działaniu soquelitinibu lepiej się namnażały przez tygodnie w hodowli, umierały rzadziej i szczególnie zwiększały wzrost oraz zdolność zabijania podpopulacji CD8, głównych „żołnierzy” bezpośrednio eliminujących komórki nowotworowe.
Przebudowa przeciążenia komórek T
Istotnym osiągnięciem tej pracy jest wykazanie, że hamowanie ITK robi więcej niż krótkotrwale pobudzić komórki CAR-T; przebudowuje programy kontrolujące wyczerpanie i pamięć komórkową. Przy użyciu szczegółowego profilowania komórek i analizy ekspresji genów zespół odkrył, że soquelitinib zarówno obniżał poziomy kilku „hamulców” na powierzchni CAR-T, jak i tłumił wewnętrzne obwody genetyczne odpowiedzialne za przewlekłe zmęczenie. Markery takie jak PD-1, TIM3, LAG3, TIGIT i CD39, związane z wyeksploatowanymi komórkami T, były zmniejszone nawet po wielokrotnej ekspozycji na komórki nowotworowe. Równocześnie zwiększały się geny i białka związane z długowiecznymi, o cechach podobnych do komórek macierzystych lub pamięci — w tym TCF1 oraz molekuły związane z homingiem i przetrwaniem. W efekcie blokada ITK przesunęła komórki CAR-T z wyczerpanego, nadmiernie stymulowanego stanu w kierunku bardziej zrównoważonego, trwałego profilu zabójcy.
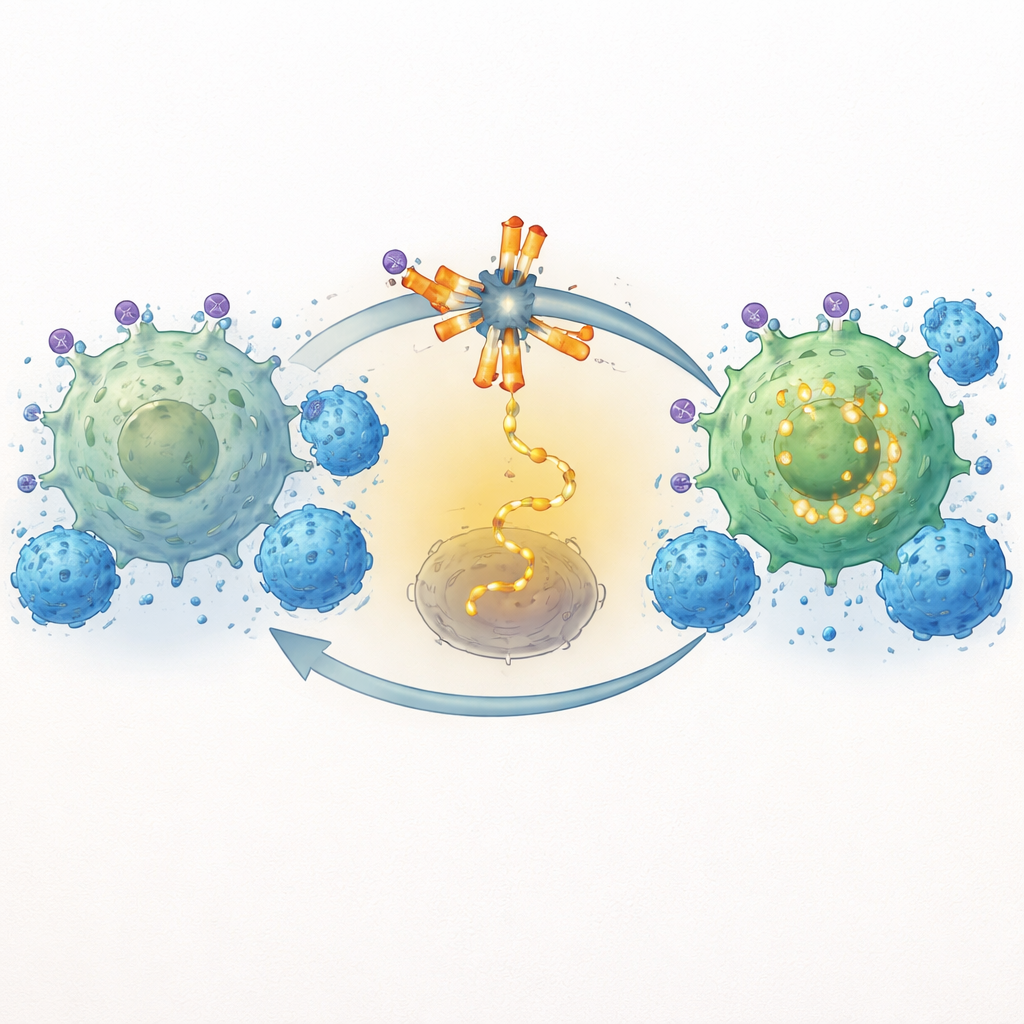
Dowód w modelach zwierzęcych
Aby sprawdzić, czy ta reprogramacja ma znaczenie in vivo, badacze przetestowali połączenie w myszach z agresywną ludzką białaczką. Wszystkie zwierzęta otrzymały komórki CAR-T przeciw CD19, ale tylko część dodatkowo otrzymywała codziennie soquelitinib. Grupa otrzymująca kombinację wykazała znacznie większy spadek obciążenia białaczką, mierzony obrazowaniem całego ciała, i przeżywała dłużej niż myszy leczone samymi komórkami CAR-T. Co ważne, sam soquelitinib nie hamował wzrostu guza, co wskazuje, że jego korzyść wynika z przebudowy odpowiedzi immunologicznej, a nie działania jako konwencjonalny lek cytotoksyczny. Wyniki te wspierają pomysł, że precyzyjne dostrojenie sygnalizacji komórek T, zamiast jej prostego wzmacniania, może dać skuteczniejszy i trwalszy atak na nowotwór.
Co to może oznaczać dla pacjentów
Dla osób z chłoniakami i białaczkami komórek B, a potencjalnie także innymi nowotworami, badanie wskazuje nową strategię: łączenie terapii CAR-T z inhibitorem ITK, aby zapobiegać wypaleniu układu odpornościowego. Poprzez umiarkowane osłabienie jednej ścieżki sygnałowej soquelitinib wygląda na środek pomagający komórkom CAR-T namnażać się, zachować funkcjonalność i opierać się wyczerpaniu, co prowadzi do silniejszej i dłużej utrzymującej się kontroli guza w modelach przedklinicznych. Choć konieczne będą badania kliniczne w celu potwierdzenia bezpieczeństwa i korzyści u pacjentów, praca sugeruje, że celowane „przebudowanie” układu odpornościowego może uczynić terapie CAR-T następnej generacji bardziej niezawodnymi, trwalszymi i być może rozszerzyć ich zastosowanie na nowotwory litych, które jak dotąd opierały się tej potężnej formie immunoterapii.
Cytowanie: Li, Z., Lv, L., Yao, X. et al. ITK-targeted immune remodeling enhanced the efficacy of anti-CD19 CAR-T cell therapy. Cell Death Discov. 12, 131 (2026). https://doi.org/10.1038/s41420-026-03004-2
Słowa kluczowe: terapia komórkami CAR-T, wyczerpanie komórek T, inhibicja ITK, chłoniak komórek B, immunoterapia nowotworów